癌は、細胞を制御するコントロールが壊れた結果である。 その破綻の原因には、必ず重要な遺伝子の変化が含まれている。 これらの変化は、しばしば突然変異、すなわち染色体のDNA配列の変化の結果である。 突然変異はほんの数塩基に影響する非常に小さな変化であることもあれば、染色体の構造に大きな変化をもたらす非常に大きな変化であることもあります。
小さな変異も大きな変異も細胞の挙動に影響を及ぼします。 重要な遺伝子の変異が組み合わさると、癌の発生につながることがあります。 このページでは、突然変異とがんの関係、さまざまな種類の突然変異、そしてそれらの原因について説明します。 このページのトピックに関する詳細な情報は、ほとんどの生物学の入門教科書にも記載されており、私たちはCampbell Biology, 11th editionをお勧めします。
- 突然変異と癌
- 遺伝性突然変異と癌
- 突然変異の種類
- 点突然変異
- 転座
- 遺伝子増幅
- 逆性。 欠失・重複
- 異数性
- 後成的変化
- 変異の原因
- 変異のまとめ
- 流れを知ろう。
変異とがん
がん細胞が示す異常な行動は、主要な制御遺伝子に生じた一連の変異の結果である。 より多くの遺伝子が傷つくにつれて、細胞は次第に異常になっていく。 多くの場合、DNA修復を司る遺伝子自体が損傷を受け、細胞はますます遺伝的混乱に陥りやすくなります。
以下は、染色体、遺伝子、DNAの関係を示すアニメーションです。 その細胞が分裂するとき、結果として生じる「娘」細胞は一定期間内に異なる変異を獲得し、異なる行動をとる可能性があります。 分裂や細胞死に対する抵抗力において優位に立った細胞は、集団を支配する傾向にあります。 このようにして、腫瘍細胞は、表象される細胞型の健康なバージョンには通常見られない、幅広い能力を獲得することができるのです。
現在までに研究されているほぼすべての種類のがんにおいて、正常で健康な細胞からがん細胞への移行は段階的な進行であり、多くの遺伝子変化が積み重なってがん細胞を作り出しているように思われます。 これらの変異は、癌遺伝子と癌抑制因子の両方で起こります。 これが、高齢者にがんが多い理由の一つです。 がん細胞を作るには、同じ細胞の中で一連の突然変異が起こる必要があります。 どの遺伝子も変異する可能性は非常に低いので、同じ細胞で複数の異なる変異が起こる可能性は本当に低いということになる。 このため、70歳の老人の細胞は、がん細胞を形成するのに必要な変化を蓄積する時間が長いのですが、子供の細胞は必要な遺伝子の変化を獲得している可能性が非常に低いのです。 もちろん、子どもでもがんになる人はいますが、高齢者の方がはるかに多いのです。 下のグラフは、米国における大腸がんの罹患率を年齢で表したものです。 このグラフは、国立がん研究センターから入手したものです。 2
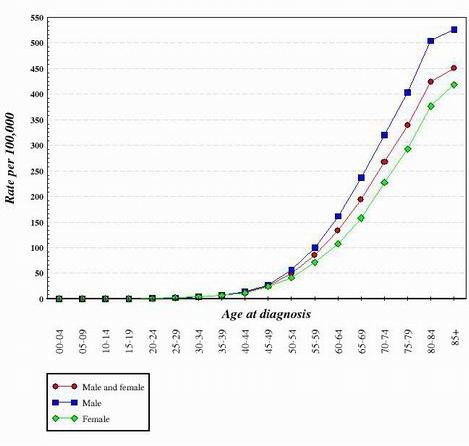
上に示したような曲線の形状を見ると、がん化する細胞を作るにはいくつかの遺伝子変化が必要であると結論付けられています。
研究室では、主要制御タンパク質を変更したり導入したりして腫瘍細胞を作る試みが行われています。 3
自然界では、突然変異は時間とともに細胞内に蓄積され、「正しい」遺伝子群が変異した場合、がんが発生する可能性があります。 2012年の研究では、健康な人の骨髄幹細胞は、加齢とともに多くの変異を蓄積していくことが示されました。 主要な遺伝子にあと少し変化が加わるだけで、がんが発生する可能性があるのです。 この結果は、「正常な」細胞とがん細胞は、多くの場合、それほど違いがないことを示唆している4
がんの遺伝的変異
さらに複雑なことに、がん細胞を作り出すのに必要な変化は、多くの異なる方法で達成できることが明らかになっている。 すべての癌は、成長し進行するために同じスペクトルの制御機能を克服しなければならないが、関係する遺伝子は異なる場合がある。 さらに、遺伝子が制御されなくなったり、失われたりする順番も様々です。 例えば、2人の異なる個体から得られた大腸がんは、結果(がん)が同じであっても、腫瘍抑制因子とがん遺伝子のセットが非常に異なっている可能性があります。 腫瘍の分子分類における現在の進歩は、任意の症例に関与する実際の遺伝子に基づく治療プロトコルの合理的な設計を可能にするはずである。 新しい診断検査では、何百、何千もの遺伝子をスクリーニングして、個人の腫瘍の個人化されたプロファイルを作成することができる。 この情報により、個人に合わせたがん治療が可能になるはずである。 これに関するより詳しい情報は、ゲノミクス/プロテオミクスのセクションをご覧ください。
制御不能な細胞増殖をもたらす遺伝的変化は、2つの異なる方法で獲得される可能性があります。 突然変異は何年もかけて徐々に起こり、「散発的」な癌の発症につながる可能性があります。 もう一つは、機能不全の遺伝子を受け継いで、特定の種類のがんを家族性で発症する可能性があります。 7110>
- 乳がん- BRCA1およびBRCA2遺伝子の変異型の遺伝は、既知の危険因子である。 乳癌患者の多く(ほとんどではないにしても)は、これらの遺伝子に検出可能な変化を持たないが、変異型を持っていると乳癌を発症する可能性が高くなる。
- 大腸がん- MSH2などのDNA修復遺伝子の欠陥は、遺伝性非ポリポーシス大腸がん(HNPCC)の素因となることが知られています。
- 網膜芽腫- Rb腫瘍抑制遺伝子の欠陥は、この目のがんや他のいくつかの種類のがんを引き起こすことが知られています。 この病気についての詳細は、Rbのセクションをご覧ください
これは既知の遺伝性がんの不完全なリストであり、さまざまな種類のがんの遺伝学が明らかになるにつれ、より多くの遺伝性がんが特定されることは間違いないでしょう。
このトピックに関する詳しい情報は、Robert A. Weinberg著『The Biology of Cancer』の第2章と第4章に記載されています。
突然変異の種類
タンパク質が作られる過程である翻訳は、転写の過程で作られたmRNAの「読み取り」に基づいて行われます。 遺伝子をコードするDNAに何らかの変化が生じると、生成されるmRNAに変化が生じます。 そして、変化したmRNAは、正常に機能しなくなったタンパク質の産生につながる可能性があります。 遺伝子のDNAに沿った1塩基の変化でさえ、まったく機能しないタンパク質につながる可能性があります。
Point Mutations
遺伝子の変化は、大きく2つのカテゴリーに分類することができます。 第一のカテゴリーは、DNA鎖に沿った1つまたは数個のヌクレオチドのみを変化させるものである。 リボソームがメッセンジャーRNA分子を読むとき、3つのヌクレオチドすべてが1つのアミノ酸として解釈されます。 この3文字のコードをコドンと呼びます。 英文に例えると、「The fat cat ate the rat」は6個のコドンを含んでいることになる。 突然変異による変化は、「The fat bat ate the rat.」とか「The fa.」とか「The fat oca tat her at…」といった具合になるのである。 タンパク質への影響は、変化が起こる場所と変化の種類によって異なります。
リボソームが読む3文字のコドンは、3つの方法のうちの1つで突然変異によって変化することがあります:
ナンセンス突然変異
新しいコドンによってタンパク質が早期に終了して、短くなりしばしば適切に機能しないかまったく機能しないタンパク質が作られるのです。
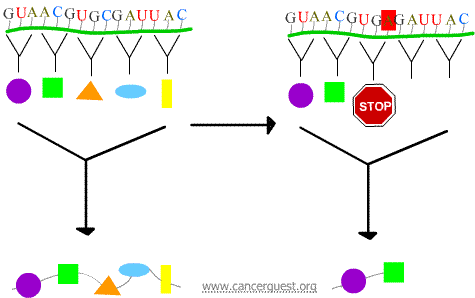
ミスセンス突然変異
新しいコドンによって、タンパク質に誤ったアミノ酸が挿入されてしまう。

フレームシフト変異
1または2塩基の損失または獲得により、影響を受けたコドンとそれに続くすべてのコドンが誤読されるようになる。
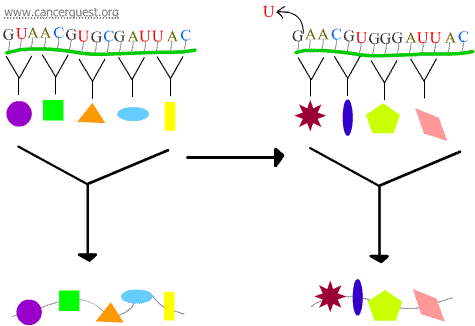
転写エラー
いくつかのDNA損傷は、RNAポリメラーゼによって「読む」ことができないヌクレオチドの修飾または小さなヌクレオチドのグループを生じます。 RNA ポリメラーゼ複合体がこのような場所に到達すると、間違ったものを入れてでも前進しようと、ヌクレオチドを追加して損傷を迂回することがあります。 5
転座
もうひとつの突然変異のカテゴリーは、より大量のDNAの変化を伴うもので、しばしば染色体レベルでの変化を伴います。 これらは転座と呼ばれ、染色体断片の切断と移動が関与しています。
すべての遺伝子が残っているため、あまり問題がないように見えますが、このプロセスによって、さまざまな方法で細胞の成長が制御される可能性があります。 遺伝子が新しい場所で適切に転写、翻訳されない可能性がある。
2. 遺伝子の移動により、その転写レベルが増加または減少する可能性がある。
一部の癌では、特定の転座が非常によく見られ、病気の診断に用いられることさえある。 転座は白血病やリンパ腫によく見られ、固形組織のがんではあまり確認されていません。 例えば、 慢性骨髄性白血病 (CML) 患者の 90% 以上に見られる 9 番染色体と 22 番染色体 の交換がその一例です。 この交換により、 22番染色体の短縮型が形成され、 発見された場所にちなんでフィラデルフィア染色 体と呼ばれます。 67
特定の転座にしばしば (または常に) 関連する他の癌には、バーキットリンパ腫、B 細胞リンパ腫、およびいくつかのタイプの白血病があります。
遺伝子増幅
この非常に珍しいプロセスでは、通常の DNA 複製プロセスが著しく損なわれます。 その結果、染色体のある領域のコピーが1つ作られる代わりに、多くのコピーが作られるのです。 その結果、染色体のその領域に位置する遺伝子のコピーが多数作られることになります。
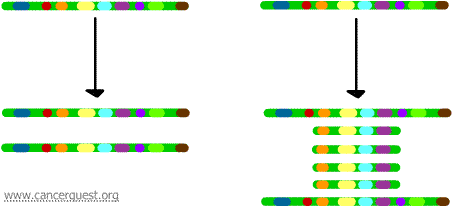
それぞれのコピーにある遺伝子が転写、翻訳され、下図のように増幅された遺伝子に対応するmRNAとタンパク質が過剰に生産されることがあります。
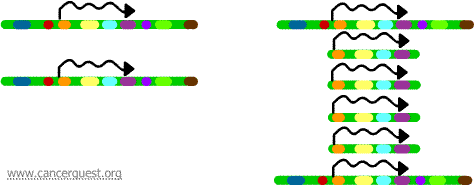
このプロセスは正常細胞では見られないが、がん細胞ではかなり頻繁に発生する。 増幅された領域に癌遺伝子が含まれている場合、その遺伝子の結果として過剰発現が起こり、細胞の成長が制御不能になることがあります。 例えば、様々な腫瘍におけるmyc遺伝子の増幅や、乳がんや卵巣がんにおけるErbB-2やHER-2/neu遺伝子の増幅がその例である。 HER-2/neu癌遺伝子の場合、臨床治療はタンパク質産物を過剰発現している細胞を標的として設計されている。
遺伝子増幅は、癌治療における最大の問題の一つである薬剤耐性にも寄与している。 薬剤耐性腫瘍は、化学療法剤の存在下でも増殖や転移を続けることがあります。 一般的に関与している遺伝子は、多剤耐性(multiple drug resistance)のMDRと呼ばれるものです。 この遺伝子の産物であるタンパク質は、細胞膜にあるポンプとして機能します。 化学療法剤を含む分子を細胞から選択的に排出することができる。
これについては、「薬剤耐性」のセクションでより詳しく説明します。
逆位、重複、および欠失
Inversions
これらの変化では、DNAセグメントが染色体から放出され、反対方向に再挿入されます。 前の例と同様に、この再配列は、癌遺伝子を活性化したり、癌抑制遺伝子を不活性化することによって、遺伝子発現の異常を引き起こします
重複/欠失
複製エラーにより、ある遺伝子または遺伝子群が染色体内で2回以上コピーされることがあります。 これは遺伝子増幅とは異なり、染色体外に遺伝子が複製されることはなく、何百回、何千回と複製されることはなく、1回だけ余分に複製されます。

異数性
異数性とは、染色体全体が失われたり増加したりする遺伝子の変化のことをいいます。 細胞分裂の過程で、複製された染色体が正確に娘細胞に分離されないことがあります。 その結果、染色体の数が多すぎたり、少なすぎたりする細胞が発生します。
下のアニメーションでは、2つの染色体のコピーが作られますが、細胞が分裂するときに、染色体は形成される2つの細胞(娘細胞)に均等に分配されないのです。 その結果、片方の細胞には染色体が多すぎ、もう片方には足りないのです。
がん細胞は非常に多くの場合、異数体です。 人間は通常46本の染色体を細胞内に持っていますが、癌細胞はそれよりも多くの、時には100本を超える染色体を持っていることがよくあります。 余分な染色体の存在は細胞を不安定にし、細胞分裂の制御を大きく狂わせます。 現在、すべての癌が異数体であるかどうかについては議論が続いています。
エピジェネティック変化
DNA配列の実際の変化に加えて、遺伝子発現は、配列を変えないDNAやクロマチンの変化によっても変化することがあります。 これらの変化は遺伝子内のDNAの配列を変えないので、エピジェネティックな変化と呼ばれる。 以下、2種類のエピジェネティックな変化について説明する。
メチル化
この変化では、DNA中の一部のヌクレオチドが塩基にメチル(-CH3)基が付加されることで修飾される。 DNAのメチル化は、DNAのその特定の領域の不活性化に関連している。 DNAの異常なメチル化パターンは、がん細胞で確認されています。
アセチル化
このエピジェネティックな変化では、DNAが巻かれているヒストンタンパク質が、アセチル(-CH3CHO)基の付加によって修飾されるようになる。 この変化により、DNAとヒストンの相互作用が緩み、遺伝子発現が増加する。
エピジェネティックな変化とがん治療の詳細
変異の原因
これまで見てきたように、がん細胞は遺伝子損傷の蓄積によって正常な前駆細胞から作り出されます。 その変化が誘発されるメカニズムは様々である。 広義には、遺伝子の変化(突然変異)の主体は主に以下に述べるカテゴリーに分類され、次項で詳しく説明します。
自然突然変異
自然突然変異。 DNA中の塩基(A、T、G、C)が、修復されない複製エラーやランダムな分子事象によって変化したり失われたりすることである。 例えば、DNAに含まれる正常な塩基であるシトシンからアミノ基が失われると、DNAには通常含まれない塩基であるウラシルが生成される。 この変化が検出されず、元に戻されないと、突然変異が起こる可能性があります。 時には、DNAの骨格と塩基の間の結合が切断された結果、塩基全体が失われることもあります。 これはDNA二重らせんに隙間を生じさせ、修復されなければ、次にDNAがコピーされるとき(すなわち複製時)に突然変異を引き起こす可能性があります。
誘発性突然変異
誘発性突然変異。 生物(または細胞)をさまざまな処理にさらすことで、突然変異を誘発することができます。 最も一般的なものは以下の通りである:
放射線-最初に知られた突然変異誘発物質の一つである放射線は、突然変異の強力な誘発物質である。 異なる種類の放射線は異なる種類の遺伝的変化を引き起こす。 紫外線(UV)は点突然変異を引き起こす。 X線はDNAの二重らせんを切断し、転座、逆位、その他の種類の染色体損傷を引き起こす可能性があります。 太陽光に含まれる紫外線を浴びると、皮膚がんになる可能性があると言われています。 なお、放射線のDNA損傷特性は、いくつかの異なる放射線ベースの癌治療に利用されています。
以下に示すのは、紫外線によって引き起こされる突然変異の一種です。 この例では、紫外線がDNA二重らせんに照射されることで、2つの塩基が結合してしまうのです。
もうひとつのタイプの放射線は、自然界に存在する放射性元素(ラドンやウランなど)または原子炉で発見(および創造)されたような人工的な発生源によって放射されるエネルギーです。 この種の放射線にはさまざまな種類があり、細胞や組織にさまざまな損傷を与える可能性があります。 放射線は直接DNAを損傷することもあれば、DNAや他の細胞構成要素を損傷する化学物質(すなわち活性酸素またはROS)の生成を引き起こすこともある。 第二次世界大戦中に日本に投下された原爆の生存者の分析では、被爆後まもなく白血病が大幅に増加し、その後数十年にわたって他の種類のがんが増加したことが示されています8
危険な量の放射性物質も原子力発電所から誤って放出されてきました。 チェルノブイリ原発からの放射性物質の偶発的な放出による放射線被ばくは、甲状腺がんやその他の悪性がんの増加と関連しています9
医療用画像診断機器(X線装置やCTスキャナーなど)も患者を放射線にさらすものです。 同様に、空港で飛行機の乗客が全身スキャンを受けることは、がんのリスクをもたらすとは考えられていません11。 1112
化学的突然変異誘発物質- 多くの異なる化学物質が突然変異を引き起こすことが知られています。 これらの化学物質は、DNAまたはDNAの構成要素に結合し、複製または転写のプロセスを妨害することによって効果を発揮する。 強力な変異原の例としては、タバコの煙に含まれる化学物質のベンゾ-a-ピレンや、不適切に保存された農産物に多く含まれる変異原のアフラトキシンがあります。
慢性炎症-慢性炎症は、免疫系の細胞による変異原性化学物質の生産によって、DNA に損傷を与える可能性があります。 例えば、肝炎ウイルスの感染によって引き起こされる長期の炎症が挙げられます。 ウイルスとがんについて詳しくはこちら
酸素ラジカル-ミトコンドリアで食物からエネルギーを取り込む際に、非常に反応性が高く、細胞膜やDNAそのものを損傷する可能性のある化学物質が生成されることがあります。 この活性酸素中間体(ROI)は、以下のように、細胞が放射線にさらされることによっても生成される可能性があります。
ROIの変異原性活性は、放射線や化学療法を含むいくつかの抗がん治療の活性と同様に、がんの発生に関連しています。 131415
異常な細胞分裂
有糸分裂の際に、複製された染色体を正確に2つの娘細胞に分割できないことがあり得ます。 この種のエラーは、異数性細胞の生成につながります。 この細胞は、遺伝子が欠落しているか、あるいはかなりの数の遺伝子を獲得していることになります。 この稀なプロセスは、無秩序な細胞分裂を起こしやすい細胞を作り出す可能性があります。
細胞が、そのタンパク質産物が分裂プロセスの「チェック」を担当している遺伝子に変異を有している場合、事態は急速に制御不能に陥り、各分裂の娘細胞はますます異常化する可能性があります。
変異原としてのウイルス
ウイルスは、がん患者のかなりの割合に関係していると考えられています。 ウイルスはさまざまな方法でがんを引き起こす可能性があり、ウイルスの種類によってその作用の仕方は微妙に異なるようです。 いくつかのウイルス(多くのレトロウイルスを含む)は、感染した細胞のゲノムに自分の遺伝子を挿入することによって突然変異を引き起こすことができます。 挿入された DNA は、影響を受ける遺伝子の活性を破壊したり変化させたりします。161718
ウイルスは、間接的な方法で突然変異を引き起こすこともあります。 一例として 肝炎ウイルスの感染は何年も続くことがある。 その間、体の防御システムは有毒な化学物質を生産することによって、ウイルスを排除しようとします。 これらの化学物質は、健康な「傍観者」である細胞にダメージを与え、癌につながる道を歩ませる可能性があります。 1920
多くの癌の発生においてウイルスが重要であるため、私たちはウイルスと癌を専門とするセクションを設けました。 トランスポゾンは、トランスポザーゼという酵素をコードしており、トランスポゾンをゲノム内の新しい場所に接合する働きをする(左下のトランスポゾンの模式図を参照)。トランスポゾンはバーバラ・マクリントックによって発見され、彼女はその業績でノーベル賞を受賞した2122 ヒトゲノムには、新しい場所に移動したり「ジャンプ」する能力を失ったトランスポゾンが数多く不活性化されている。 23
活性トランスポゾンの移動は突然変異を引き起こし、遺伝子の活性を変化させることがある。 トランスポゾンの移動(転座と呼ばれる)の目に見える例は、インドとうもろこしの穀粒の色である(右下参照)。 ヒトで活性化しているトランスポゾンは、がんをはじめとするヒトの病気に関与していると考えられている242526。


Mutation Summary
Genetic Change (Mutation) Introduction
- がん細胞が示す異常行動は、主要制御遺伝子(すなわちDNA修復遺伝子)の一連の変異の結果である。
- ほとんどのがんは、がん細胞となるために十分な変異を得た単一の先駆け細胞から発生すると考えられている。
DNA Mutations
- 遺伝子の変化は、1つまたはいくつかのヌクレオチドに影響を与える小さなもの(点突然変異)から、染色体または染色体の構造を変えてしまう非常に大きなものまであります。
- 点突然変異
- 翻訳とは、メッセンジャーRNA(mRNA)にある3つの塩基の「単語」(コドン)を読み取る酵素によって、タンパク質が作られることです。
- ナンセンス突然変異 – 新しい(突然変異)コドンは、タンパク質合成を早期に停止させます。
- ミセンス突然変異 – 変化したコドンは、タンパク質に誤ったアミノ酸を挿入します。
- フレームシフト突然変異 – mRNA中の1または2塩基の損失または増加は、コドンを誤って読むことを起こします。
- 染色体レベルの変化
- 転座-染色体断片の破損と(時には)交換
- 遺伝子増幅-異常な複製により染色体領域の複数のコピーが作られる。
- 逆位染色体 – DNAの断片が染色体から放出され、反対方向に再び挿入される。
- 複製/欠失 – 遺伝子や遺伝子群が完全に失われたり、染色体内で複数回コピーされたりすることがある。
- 異数性 – 染色体全体が失われたり増加したりする遺伝的変化。
- 自然突然変異は、修復されないDNAやランダムな分子事象により発生することがあります。
- 異数性はがん細胞で非常によく見られます。
エピジェネティック変化
- 遺伝子発現は、遺伝子配列を変えないDNAやクロマチンへの変化により変化させることが可能です。 例えば、DNAのメチル化やヒストンのアセチル化などがあります。
- メチル化-DNAの一部のヌクレオチドは、DNAのその領域の不活性化に関連するメチル基の付加によって修飾されます
- アセチル化-アセチル基の付加はDNAを緩め、遺伝子発現を増加させます。
誘発される突然変異
- 突然変異は、生物(または細胞)をさまざまな処理にさらすことによって誘発されます:
- 放射線 – 紫外線は点突然変異を、X線は複数の形態の損傷を引き起こします。
- 化学的変異原-DNAまたはDNAの構成要素に結合し、複製または転写プロセスを妨害することができる。
- 慢性炎症-免疫系の細胞による変異原性化学物質の生成によるDNA損傷
- 酸素ラジカル-細胞のエネルギー生産から生じ、DNAを損傷することができる。
その他の遺伝的変化
- 染色体の不正確な分割をもたらす異常な細胞分裂は、異数性を引き起こします。
- ウイルスはいくつかの異なる方法で遺伝子損傷を引き起こし、幅広い癌に関連します。
突然変異と癌
- 正常で健康な細胞から癌細胞への移行は、段階的に進行するようです。
- 癌発症にはいくつかの異なる癌遺伝子と腫瘍抑制因子における遺伝子の変化が必要です。
- すべてのがんは、成長し進行するために同じスペクトルの制御機能を克服しなければならないが、関与する遺伝子は異なる場合がある。
- がんの不均一性は、診断と治療を複雑にする。
- 特定のがん種の家族性の発症につながる機能不全遺伝子を受け継ぐ可能性があります。
Know the Flow: Mutation
Know the Flowは、あなたの知識を試すための対話型のゲームです。 遊び方:
- 右側の欄から適切な選択肢をドラッグして、左側のボックスに順番に並べてください。
- 終了したら、「チェック」をクリックして、いくつ正解したかを確認します。
- 不正解の場合は、「説明」をクリックしてプロセスに関する情報を確認します。
- もう一度挑戦するには、「リセット」を選択してやり直します。
Know the Flow: 突然変異プロセスの順番-
1
-
2
-
3
-
45
プロセス-
詳細はこちら細胞はDNA合成の過程にある
-
詳細はこちら染色体の領域の多くのコピーが作られる
もっと詳しく
増幅された遺伝子の転写 -
もっと詳しく増幅された遺伝子の転写
-
もっと詳しく鍵となる遺伝子が過剰生産されること。 タンパク質が薬剤耐性腫瘍の成長をもたらす
-
Learn moreDuplication Occurs
もう一度プレイ
- 1. Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). キャンベル・バイオロジー(第11版). Pearson.
- 2. 国立がん研究センター
- 3.ハーンWC、カウンターCM、ルンドバーグAS、ベイジャーバーゲンRL、ブルックスMW、ワインバーグRA.に代表される監視、疫学、およびエンドリザルト(SEER). “定義された遺伝的要素を持つヒト腫瘍細胞の作製” Nature 400: 464-468
- 4. Welch JS, Ley TJ, Link DC, Westervelt P, Walter MJ, Graubert TA, DiPersio JF, Ding L, Mardis ER, Wilson RKら: The origin and evolution of mutations in acute myeloid leukemia.急性骨髄性白血病における突然変異の起源と進化。 Cell, July 20, 2012
- 5. Brégeon D, Doetsch PW. 転写性突然変異誘発:腫瘍発生の原因と関与。 Nat Rev Cancer. 2011年3月;11(3):218-27。
- 6. Nowell PC, Hungerford DA. “正常および白血病のヒト白血球の染色体研究”. J Natl Cancer Inst (1960). 25: 85-100.
- 7. Rowley JD. “キナクリン蛍光とギムザ染色により同定された慢性骨髄性白血病における新しい一貫した染色体異常”。 ネイチャー(1973)。 243: 290-293.
- 8. 原爆被爆者における癌および非癌性疾患のリスク。 Radiat Prot Dosimetry. 2011年4月18日。
- 9. チェルノブイリ事故-疫学的観点から-. クリニカルオンコル(R Coll Radiol)。 2011;23(4):251-260. doi:10.1016/j.clon.2011.01.510 Mar 9.
- 10. Fazel R, Krumholz HM, Wang Y, Ross JS, Chen J, Ting HH, Shah ND, Nasir K, Einstein AJ, Nallamothu BK. 医療用画像処理による低線量電離放射線への被曝。 N Engl J Med. 2009年8月27日;361(9):849-57.
- 11. a. b. Mehta P, Smith-Bindman R. Airport Full-Body Screening.空港での全身スクリーニング。 空港での全身スクリーニング:そのリスクは? Arch Intern Med. 2011年3月28日。
- 12. Bagshaw M. 民間航空における宇宙線。 旅行医学感染症。 2008年5月、6(3):125から7。 Epub 2007 Nov 26.
- 13. Kang DH. “酸化ストレス、DNA損傷と乳がん”. AACN Clin Issues. (2002). 13:540-549
- 14. Athar M. “Oxidative stress and experimental carcinogenesis” (酸化ストレスと実験的発がん). インドJ.Exp.Biol. (2002). 40:656-667
- 15. マーネットLJ. “オキシラジカル、脂質過酸化、DNA損傷” (2002)181-182:219-222
- 16. Nair V. Retrovirus-induced oncogenesis and safety of retroviral vectors(レトロウイルスによる発癌とレトロウイルスベクターの安全性). Curr Opin Mol Ther. 2008 Oct;10(5):431-8.
- 17. Brady G, Macarthur GJ, Farrell PJ. エプスタイン・バー・ウイルスとバーキットリンパ腫. Postgrad Med J. 2008 Jul;84(993):372-7.
- 18. Ruprecht K, Mayer J, Sauter M, Roemer K, Mueller-Lantzsch N. Endogenous retroviruses and cancer(内在性レトロウイルスと癌). を参照。
- 19. Lupberger J, Hildt E. B型肝炎ウイルスによる発がん. World J Gastroenterol. 2007 Jan 7;13(1):74-81.
- 20. Castello G, Scala S, Palmieri G, Curley SA, Izzo F. HCV関連肝細胞癌。 慢性炎症から癌へ。 Clin Immunol. 2010年3月;134(3):237-50。 Epub 2009 Nov 11.
- 21. を参照)。 というものである。
- 22. また、そのような場合にも、「己の信念を貫く」ことが重要である。 Burns KH, Boeke JD. ヒトのトランスポゾンのテクトニクス。 Cell. 2012年5月11日;149(4):740-52。
- 24. Kozeretska IA, Demydov SV, Ostapchenko LI. 移動性遺伝因子とがん。 突然変異から遺伝子治療まで。 Exp Oncol. 2011 Dec;33(4):198-205.
- 25. Solyom S, Kazazian HH Jr. ヒトゲノムの可動要素:疾患への影響。 Genome Med. 2012年2月24日;4(2):12.
- 26. このような場合、「ヒトはどのように生きているのか? このように、レトロトランスポゾンがヒトゲノムの自然変異を誘発する。 Cell. 2010 Jun 25;141(7):1253-61.