ÚVOD
Stenóza proximálního úseku přední sestupné věnčité tepny (pAD) představuje zvláštní podskupinu ischemické choroby srdeční vzhledem k vysoce rizikovému profilu, který mají tyto léze samotné1,2 nebo v kontextu vícecívního onemocnění.3 Množství a kvalita ohroženého myokardu, které závisí na průchodnosti pAD, vyžaduje agresivnější terapeutický přístup. Ultrazvukové studie in vivo u tohoto typu lézí ukázaly, že postižení cév je převážně excentrické.4 To by vysvětlovalo horší výsledky dosažené po perkutánní transluminální koronární angioplastice (PTCA) u těchto lézí v důsledku fenoménu elastické retrakce. Různé studie porovnávaly léčebné strategie těchto lézí, v nichž byly obecně pozorovány lepší výsledky po intervenční léčbě (koronární revaskularizační operace se štěpem vnitřní mamární tepny nebo perkutánní revaskularizace oproti konvenční medikamentózní léčbě).5-12 Předkládaná studie hodnotí účinnost a dlouhodobou bezpečnost implantace stentu u tohoto typu lézí a byla provedena z důvodu nedostatku studií na toto téma v naší oblasti.
METODY
Studijní soubor
Do prospektivní nerandomizované klinické studie bylo zařazeno celkem 98 po sobě jdoucích pacientů odeslaných na naše pracoviště v období od dubna 1995 do dubna 1998. V tomto období bylo provedeno 1136 PTCA a studovaná skupina představuje 8,6 % všech intervenčních výkonů provedených v této době v naší laboratoři. Sledování bylo ukončeno v květnu 2000.
Kritéria pro zařazení a vyloučení
Pacienti, u nichž byla přítomna významná stenóza pAD (stenóza více než 70 % podle vizuálního odhadu) před první septální větví a větší diagonální větví, s průkazem ischemie v teritoriu závislém na pAD, byli považováni za způsobilé pro studii. Pacienti podstoupili plánovanou perkutánní balónkovou revaskularizaci a implantaci stentu. Pacienti odeslaní v průběhu akutního infarktu myokardu (AMI) byli vyloučeni, stejně jako léze s nevhodnou anatomií pro zákrok dle úsudku operatéra, zejména léze s chronickou okluzí a masivní kalcifikací. Všichni pacienti podepsali před provedením revaskularizace protokol o informovaném souhlasu. Do studijního souboru byli zařazeni všichni pacienti s lézemi pAD léčenými na našem pracovišti v tomto období.
Protokol výkonu (PTCA+implantace stentu)
Ve všech případech byla PTCA provedena cévním přístupem přes femorální tepnu a stent byl implantován (po dilataci balonku) jeho uvolněním při vysokém tlaku (12-14 atmosfér). Stenty Palmaz-Schatz a NIR (nejpoužívanější modely) byly na angioplastický balonek nasazeny ručně. V poslední fázi studie byly použity stenty, které byly předem namontovány na balonek. „Angiografický úspěch zákroku“ byl definován jako existence reziduálních lézí menších než 30 % na základě vizuálního hodnocení segmentu, do kterého byl implantován stent. „Depresivní ejekční frakce (EF)“ byla definována jako přítomnost EF menší než 50 % při vizuálním hodnocení. „Onemocnění více cév“ bylo definováno jako přítomnost významných koronárních lézí (stenózy více než 70 % podle vizuálního hodnocení) ve dvou nebo více cévách. Všichni pacienti dostávali léčbu inhibitory agregace krevních destiček kyselinou acetylsalicylovou po dobu neurčitou a tiklopidinem po dobu jednoho měsíce po angioplastice. Před zákrokem byl podán i.v. bolus 7500 až 10 000 IU heparinu v závislosti na hmotnosti pacienta, aby se dosáhlo doby aktivace parciálního tromboplastinu nad 300 s.
Protokol následného sledování
Všichni pacienti se účastnili každoročního klinického sledování formou osobního nebo telefonického rozhovoru. Všichni podstoupili vyšetření ke zjištění ischemie podle pokynů svých ošetřujících kardiologů. V případech s pochybnými výsledky testů nebo rozpory mezi klinickými příznaky a výsledky testů jsme nařídili nové testy k detekci ischemie (nové zátěžové testy nebo radionuklidové studie). Poslední návštěva proběhla osobně a byla provedena klinická anamnéza, fyzikální vyšetření a EKG. Pacienti, u nichž přetrvávala angina pectoris s klinickými kritérii závažnosti, podstoupili angiografické přehodnocení přímo v laboratoři. Angiografická restenóza byla definována jako přítomnost stenózy větší než 50 % v segmentu pAD léčeném implantací stentu.
Ve studijní skupině byla zaznamenána řada proměnných pro pozdější analýzu a stanovení prognostických faktorů klinického vývoje pacientů. Tyto proměnné byly:
— Klinické: věk, pohlaví, diagnóza před katetrizací, přítomnost diabetes mellitus, arteriální hypertenze, kouření, dyslipidémie. Vícečetné rizikové faktory byly považovány za existující, pokud byly spojeny tři nebo více klasických rizikových faktorů.
— Anatomické: přítomnost vícecívního onemocnění, dysfunkce levé komory.
— Procedura: délka a průměr stentu, počet použitých stentů, typ stentu a přítomnost ostiální léze.
Konečné příhody
Během hospitalizace a pozdějšího sledování byl zaznamenán výskyt závažných nežádoucích srdečních příhod (MACE) nebo závažných komplikací, definovaných jako: úmrtí srdečního původu, výskyt nového AMI a nutnost nové pAD revaskularizace. Zaznamenávala se nekardiální úmrtí a potřeba revaskularizace cév odlišných od pAD.
Statistická analýza
Různé proměnné byly shromážděny v databázi Microsoft Access® a analyzovány pomocí statistického programu SPSS®, verze 9.0.
. Kvalitativní proměnné jsou vyjádřeny v procentech a kvantitativní proměnné jako průměr ± směrodatná odchylka (SD). Aktuarické křivky přežití bez úmrtí, přežití bez srdeční smrti a přežití bez příhod byly odhadnuty Kaplanovou-Meierovou metodou. V jednorozměrné analýze byly jednotlivé uvedené klinické, angiografické a procedurální proměnné porovnány na základě přítomnosti nebo nepřítomnosti závažných nežádoucích příhod na konci sledování, kvantitativní proměnné byly porovnány pomocí Studentova t testu a kvalitativní proměnné pomocí Chí-kvadrát testu. Kromě toho byly křivky přežití bez příhod porovnány pomocí log-rank testu u proměnných, které vykazovaly tendenci k prezentaci příhod (PP P
VÝSLEDKY
Základní charakteristiky
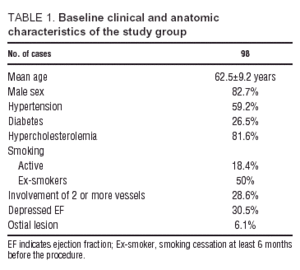
Klinické charakteristiky pacientů v době zařazení do studie a anatomické charakteristiky zjištěné při koronarografii jsou uvedeny v tabulce 1. V tabulce 1 jsou uvedeny základní charakteristiky pacientů v době zařazení do studie. Většina pacientů byla odeslána pro nestabilní anginu pectoris (87 pacientů s nestabilní anginou pectoris, 11 pacientů se stabilní námahovou anginou pectoris). Dvacet dva pacientů mělo 3 a více kardiovaskulárních rizikových faktorů; z nich 20 (91 %) bylo hypertoniků, 19 (86 %) diabetiků a 21 (95 %) mělo dyslipidemii, zatímco pouze 10 (55 %) bylo aktivních kuřáků. Sedmdesát jedna procent (71 %) pacientů mělo jedinou lézi pAD a u 70 % z nich nebyla při ventrikulografii prokázána komorová dysfunkce.
Procedura
Proměnné procedury jsou uvedeny v tabulce 2. V tabulce 2 jsou uvedeny proměnné, které se týkaly postupu. Sedmdesát sedm procent (77 %) pacientů mělo krátké léze pAD, což odráží procento použitých krátkých stentů (

Vývoj
Průměrná doba sledování byla 38 ± 11 měsíců, přičemž kratší než 24 měsíců byla pouze u 2 pacientů, kteří zemřeli (ve 2 a 9 měsících od zařazení). V průběhu studie nedošlo k žádné ztrátě ze sledování, jak je graficky znázorněno na obrázku 1. V průběhu studie až do jejího ukončení zůstalo 68 pacientů (69,4 %) bez anginy pectoris a během sledování se u nich neprojevila žádná MACE. Dvacet pět pacientů (25,5 %) mělo anginu pectoris a bylo odesláno na nové koronarografické vyšetření. U 7 pacientů byla pozorována angiografická restenóza, ale nebylo rozhodnuto o novém perkutánním nebo chirurgickém revaskularizačním výkonu (4 pacienti měli nepřemostitelné distální cévy a anatomické léze nepříznivé pro novou PTCA a další 3 měli restenózu menší než 70 % a adekvátní klinickou kontrolu antianginózními léky). Dvanáct pacientů vyžadovalo novou revaskularizaci cílové léze: 6 koronární operací a IMA bypassem 3, 6, 6, 9, 13 a 14 měsíců po implantaci stentu (u jednoho byla operace provedena po nové PTCA pAD pro časnou restenózu ve 3 měsících) a 6 novou PTCA mezi 5. a 34. měsícem sledování (v jednom případě byl stent odstraněn kvůli intrastentální restenóze). Dalších 7 pacientů s přetrvávající anginou pectoris bylo odesláno k nové revaskularizaci pomocí PTCA a implantaci stentu do jiných cév než do pAD, u 3 z nich byly ošetřeny 2 cévy (3 revaskularizace pravé koronární tepny, 3 střední přední sestupné a 4 obtokové marginální). Dva pacienti měli přední AMI (jeden němý) 2, resp. 4 měsíce po zákroku. Koronarografie nebyla později provedena, protože testy na reziduální ischemii byly negativní.
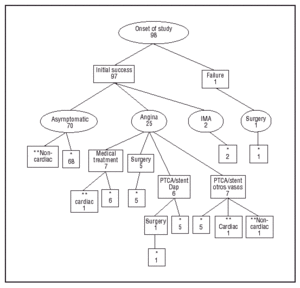
Obr. 1. Koronarografie. Schéma vývoje pacientů (*asymptomatičtí na konci studie, **smrt).
Pět úmrtí se vyskytlo, 2 kardiálního původu ve 2. a 38. měsíci od zařazení do studie a 3 nekardiálního původu (1 pro nádorové onemocnění ve 38. měsíci od zařazení do studie, 1 pro akutní břicho s krvácením do konečníku v 9. měsíci a 1 pro ischemickou cévní mozkovou příhodu ve 24. měsíci).
Podle Kaplan-Meierova testu byla pravděpodobnost, že po 60 měsících sledování zůstane pacient bez MACE, 83,7 % (obr. 2) a celková pravděpodobnost, že neutrpí kardiální nebo nekardiální úmrtí, byla 98 %, resp. 94,8 % (obr. 3).
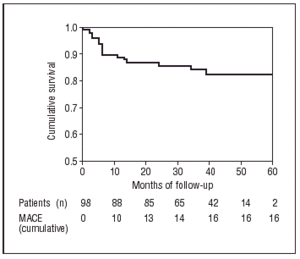
Obr. 2. Kaplan-Meierova křivka přežití bez závažných srdečních příhod.
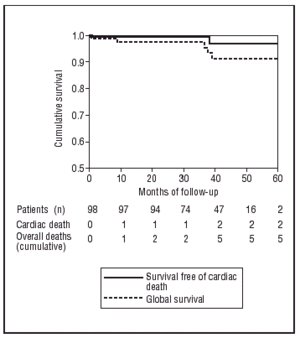
Obr. 3. Kaplan-Meierovy křivky přežití bez úmrtí a bez úmrtí srdečního původu.
Klinické, anatomické a procedurální proměnné a jejich vztah k případnému výskytu MACE ukazuje tabulka 3. Univariační analýza ukázala, že použití 2 stentů bylo spojeno s vyšším výskytem MACE (PP=,021) a interakce AHT-DM-dyslipidemie (OR=3,7; 95% CI, 1,3-10,3; P=,011). Ostiální stenózy (OR=3,7; 95% CI, 0,8-16,6; P=,09) vykazovaly větší tendenci k výskytu příhod.
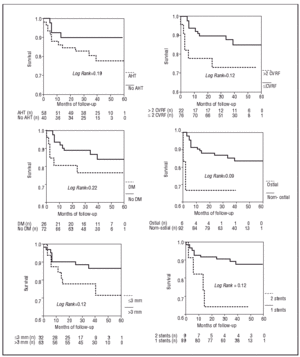
Obr. 4. Výskyt příhod. Kaplanovy-Meierovy křivky přežití bez závažných srdečních příhod v závislosti na přítomnosti různých klinických faktorů a postupu. CVRF označuje kardiovaskulární rizikové faktory.
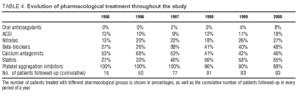
Farmakologická léčba, kterou pacienti během studie dostávali, je uvedena v tabulce 4. Kromě antagonistů vápníku a beta-blokátorů, které na konci studie užívalo 48 %, resp. 46 % pacientů, byly během sledování často užívány inhibitory agregace krevních destiček (kyselina acetylsalicylová a/nebo tiklopidin). Užívání statinů se výrazně zvýšilo, a to z 27 % na začátku sledování na 65 % při jeho ukončení.
DISKUSE
Dlouhodobé výsledky (průměrná a maximální doba sledování 38, resp. 60 měsíců) této prospektivní observační studie stenóz proximálního segmentu pAD léčených implantací stentu ukázaly, že zákrok měl vysokou míru úspěšnosti (98 %.9 %), nízkou míru nových revaskularizací (12,2 %), vysokou pravděpodobnost, že zůstane bez MACE (83,7 %), a nízkou mortalitu. Je třeba poznamenat, že velké procento pacientů mělo krátké, jednožilové léze a bez zhoršené funkce levé komory.
Srovnání s předchozími studiemi
Předchozí studie prokázaly, že intervenční léčba přináší větší prospěch než farmakologická medikamentózní léčba u závažného onemocnění pAD nebo jednožilové ischemické choroby srdeční.5,6 Nicméně srovnání dvou hlavních revaskularizačních technik (PTCA a IMA štěp) ukazuje větší výskyt nových revaskularizací ve skupině léčené PTCA, větší potřebu antianginózních léků a horší toleranci zátěže, přičemž míra reinfarktů a mortality je v obou skupinách podobná.4,7-12 Tento vyšší výskyt nových revaskularizací po PTCA je způsoben fenoménem restenózy, který se vyskytuje především v prvním roce po PTCA.13,14 Výskyt restenózy po izolované PTCA se v různých sériích pohybuje od 40 % do 66 %. Mezi faktory favorizující restenózu patří přítomnost proximálních lézí a postižení descendentní přední koronární tepny.15 Zavedení implantace stentů tyto výsledky jednoznačně změnilo a snížilo riziko restenózy téměř o polovinu,9,16-19 při velmi nízkém výskytu bezprostředních komplikací a vysoce příznivém krátkodobém a střednědobém klinickém vývoji (podobném tomu, kterého bylo dosaženo u IMA graftů s urgery). Předchozí studie prokázaly četnost selhání implantátu u stentů, které se na balonek nasazují ručně, v rozmezí 1,5-6,9 % u stentu Palmaz-Schatz a 1,5-3,1 % u stentu NIR.20,21 Nejnovější studie stentů druhé generace, například registr SPORT-NIR,22 uvádějí četnost selhání implantátu pouze 0,4 %. V naší studii došlo pouze k jednomu selhání, a to při implantaci stentu Palmaz-Schatz, který byl na angioplastický balonek nasazen ručně. Tato 1% míra selhání se shoduje s výsledky uváděnými v předchozích studiích.
Míra restenózy a nutnosti nové revaskularizace stentu se v různých sériích liší od 19 % do 31 %.10,16,19,23 Naše výsledky potvrzují, že k novým revaskularizacím pAD může dojít až dva a půl roku po zákroku, ačkoli většina reintervencí proběhla během prvních 12 měsíců po implantaci stentu (66,6 % případů). Zjistili jsme výskyt nových revaskularizací pAD ve výši 12,2 %, ačkoli skutečný výskyt významné restenózy a předčasnost jejího vzniku v našem souboru není znám, protože jsme pacienty systematicky nehodnotili pomocí angiografie.
Prediktory vývoje
Z analyzovaných faktorů bylo pouze použití dvou stentů během zákroku nezávislým rizikovým faktorem pro méně příznivý klinický vývoj, což se shoduje se zprávou skupiny Bauters et al.24
Faktory, které tradičně naznačují horší prognózu po implantaci stentu, jako je DM, vícecívní onemocnění, hypertenze nebo dysfunkce levé komory při dlouhodobém sledování25 , se v univariační analýze nepotvrdily. V případě DM bylo zjištěno, že restenóza je zásadně způsobena procesem nadměrné intimální hyperplazie ve srovnání s nediabetickými pacienty,26 u nichž se tento proces vyvíjí méně agresivně. Tento jev se projevuje vyšší mírou restenózy a potřebou nových revaskularizačních zákroků.27 Z 23 diabetických pacientů v naší studii byla většina (20 z 23) pacientů nezávislá na inzulínu, což může vysvětlovat, proč DM nebyl nezávislým prediktorem, protože nedávné studie prokázaly rozdíl ve vývoji propustnosti stentu v závislosti na typu diabetu. Prognóza je horší u DM závislého na inzulínu.28,29 Nicméně v multivariační analýze byla zjištěna souvislost DM, AHT a dyslipidemie s horším klinickým vývojem. To ukázalo, že ačkoli tyto faktory nejsou jednotlivě jasně spojeny s prognózou (přinejmenším vzorky o velikosti zde zkoumané), souběh faktorů u pacienta je třeba považovat za predikci méně příznivého vývoje, jak k tomu dochází u aterosklerotického onemocnění obecně.
Po celou dobu sledování se intenzivně užívala medikace, což bylo v zásadě způsobeno vysokou prevalencí tradičních kardiovaskulárních rizikových faktorů ve studované populaci, jako je hypercholesterolemie a AHT, a mnohočetným onemocněním, které se projevilo v době zařazení (31 %) a v průběhu evoluce (u 7 pacientů byla přítomna progrese ischemické choroby srdeční vyžadující revaskularizaci dalších cév).
Klinické důsledky
Výsledky naší studie potvrzují bezpečnost implantace stentu u lézí zahrnujících pAD a dobrou dlouhodobou klinickou odpověď, která u některých pacientů dosáhla 5 let sledování. Získané údaje o přežití a absenci MACE se shodují s předchozími studiemi implantace stentu u pAD30 a jsou srovnatelné s údaji uvedenými v jiných studiích, v nichž byla provedena koronární revaskularizace s operací IMA štěpu.7,31
V klinické praxi8,32 musí být rozhodnutí o volbě operace IMA bypassu oproti PTCA a implantaci stentu učiněno individuálně u každého pacienta, s přihlédnutím k názoru pacienta po obdržení informací o obou terapeutických alternativách, jejich výsledcích a rizicích a s ohledem na perkutánní alternativu jako první volbu v případech s příznivou koronární anatomií a u pacientů, u nichž lze předpokládat potřebu budoucích revaskularizací (např, mladí pacienti).
Omezení studie
Hlavním omezením studie byla absence randomizace, která znemožnila přímou srovnávací analýzu s jinými revaskularizačními strategiemi. Skutečnost, že během sledování nebyla systematicky prováděna koronární arteriografie, nám neumožňuje určit skutečnou míru angiografické restenózy ve studijní skupině. Použitá technologie byla účinná od roku 1995. Použití nových materiálů a konstrukcí u stentů novější generace a nových antiagregačních režimů s antagonisty destičkových receptorů IIb-IIIa by mělo zlepšit krátkodobé i dlouhodobé výsledky. Zdá se však, že výsledky získané s těmito látkami v naší studii nepodporují jejich všeobecné použití při implantaci stentů vzhledem k jejich vysokému poměru nákladů a přínosů.
ZÁVĚRY
Léčba stenózy proximálního úseku přední sestupné koronární tepny implantací stentu je bezpečná u pacientů s příznivou koronární anatomií pro tento výkon. Procento komplikací je nízké a při delším sledování, které v některých případech v naší studii činí 5 let, je doprovázeno nízkým výskytem nových revaskularizačních výkonů a vysokou mírou přežití.
PODĚKOVÁNÍ
Rádi bychom vyjádřili upřímnou vděčnost dr. V. Climentovi a J. Sánchezovi z oddělení kardiologie, respektive preventivní medicíny, Hospital General Universitario of Alicante za jejich podporu a vedení při přípravě tohoto článku.