Po zjištění existence jádra se nyní můžete zabývat experimentálními důkazy jeho velikosti, počínaje Rutherfordovým experimentem.
Shrnutí lekce
- Diskuse a pracovní příklad: Velikost jádra (15 minut)
- Diskuse: Velikost atomu a jádra (10 minut)
- Dotaz pro studenty: Síly a nejtěsnější přiblížení (30 minut)
- Diskuse: (5 minut)
- Diskuse: Atomové číslo a náboj jádra (5 minut)
- Diskuse: Atomové číslo a náboj jádra (5 minut): Horní hranice velikosti jádra (30 minut)
- Diskuse: Hádanka pro příští hodinu (5 minut)
Diskuse a pracovní příklad: Velikost jádra
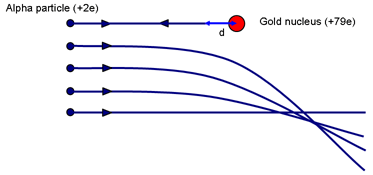
Přemýšlením o Rutherfordově experimentu si můžete udělat představu o možné velikosti jádra. Zeptejte se: Jaký parametr dopadu povede k tomu, že se částice dostane nejblíže k jádru? (Čelní srážka s p = 0.)
Princip zachování energie se používá k výpočtu vzdálenosti nejtěsnějšího přiblížení jako míry pro velikost jádra. Pochopení následujícího výpočtu závisí na tom, zda se studenti zabývali elektrickým potenciálem a polem. Případně poslouží jako dobré opakování.
Epizoda 522-1: Rozptyl částic alfa – vzdálenost nejtěsnějšího přiblížení (Word, 29 KB)
Epizoda 522-2: Vzdálenost nejtěsnějšího přiblížení (Word, 107 KB)
Když se částice α dostane na okamžik do klidu (poté, co vyšplhala co nejdále po elektrostatickém kopci), vykoná se práce proti odpudivé síle od jádra. Kinetická energie α je uložena v poli kolem jádra. Když je rychlost nulová, veškerá energie je nyní uložena v poli.
Pokud se částice α na okamžik zastaví, když je ve vzdálenosti d od (středu) jádra s nábojem Ze, energie v poli je:
Eα = 14πε0 2e Zed
To se rovná počáteční kinetické energii částice α. Rutherford použil zdroj α, který mu dala madam Curie. Energie α byla ~ 7,7 MeV.
Pro zlato platí, že Z = 79. Řešením získáme d ~ 3 × 10-14 m. Porovnejte to s průměrem atomů zlata ~ 3 × 10-10 m. Jádro je tedy nejméně 10 000krát menší než atom. Je důležité zdůraznit, že tento výpočet udává horní hranici velikosti jádra zlata; nemůžeme říci, že se částice alfa dotýká jádra; energičtější α by se mohla dostat ještě blíže.
Atom je většinou prázdný (proto většina as prošla přímo – případné elektrony by těžko překážely relativně masivní vysoké rychlosti α).
Diskuse: Vyzvěte studenty, aby navrhli zmenšený model atomu a jádra
. Například: pokud by jádro mělo průměr 1 mm, atom by byl 10 000krát větší neboli 10 m v průměru. Vyberte vhodnou pozici pro jádro o velikosti 1 mm (malé kuličkové ložisko nebo kulička Blu-tac). Udělejte krok 5 m (pět velkých kroků) k okraji atomu, kde jsou elektrony. Poznámka: Učebnicová schémata atomu s jádrem nejsou nakreslena v měřítku.
Přesnou představu podpoříte tím, že necháte některého studenta postavit se jako jádro, odhadnete jeho obvod (40 cm?) a zeptáte se, kde by musel stát jiný student, aby byl na okraji atomu. 104 × 40 cm = 4000 m}, takže poloměr tohoto atomu je 2 km! Ověřte si na místní mapě, abyste našli pojmenované místo, které studenti poznají a které je vzdálené 2 km.
Další upevnění: V pevném tělese, kde jsou atomy těsně u sebe, je vzdálenost mezi sousedními jádry ~ velikost atomu, tj. odpovídá tomu, že dva studenti stojí 4 km od sebe!
Je tedy docela s podivem, že vůbec nějaký zasáhl jádro. Obě mají podobnou velikost. Plocha průřezu představovaná jádrem ~radius2, tedy ~1 × 10-28 m2}.
Ptejte se: Jak byste očekávali, že bude počet odražených jako záviset na tloušťce kovové fólie obsahující cílová jádra? (Představte si atomy zlata ve vrstvách, šance na odraz roste s tloušťkou, ale absorpce na cestě dovnitř nebo zpět ze stále tlustší fólie nakonec zabrání dalšímu nárůstu odraženého a detekovaného počtu.
Velmi vám pomůže, když si studenti vzpomenou na následující řády:
Průměr atomového jádra ~ 10 -14m
Průměr atomu ~ 10 -10m
Dotaz pro studenty: Síly a nejtěsnější přiblížení
Epizoda 522-3: Rutherfordův rozptyl: (Word, 82 KB)
Epizoda 522-4: Směry sil: Rutherfordův rozptyl: (Word, 83 KB)
Diskuse: Energie a nejtěsnější přiblížení:
Rutherford použil svá data ke zjištění náboje terčového jádra zlata. Další pokusy o zjištění náboje Cu, Ag a Pt fólií daly:
| Atomové číslo | Rozptylový pokus | |
| Cu | 29 | 29.3 × e |
| Ag | 47 | 46.3 × e |
| PT | 78 | 77,4 × e |
Elektrický náboj jádra je tedy dán atomovým číslem × e, tedy Z e. S jednou výjimkou (vodík, H-1) je Z vždy menší než atomové hmotnostní číslo. Co tedy vysvětluje tento rozdíl? Atom musí být elektricky neutrální. Rutherford navrhl neutron.
Diskuse: Připomeňme si, že Rutherfordova analýza udává horní mez velikosti na jádře (d ~ 1 α energie částic). Velikost, kterou naměříte, závisí na energii částice α, kterou použijete. Potřebujeme tedy jiný přístup ke zjištění velikosti jádra zlata. Napadá vás lepší částice pro zkoumání velikosti jádra? (Neutron – protože je nenabitý, dostane se blíž.)
Jinou technikou je hluboký nepružný rozptyl elektronů. Vraťte se zpět, pokud jste se již zabývali vlnovou povahou částic (de Broglieho vlny λ = hp), nebo toto téma můžete v případě potřeby vložit sem. Difrakční aparatura elektronů má základní podobnost s rozptylem částic. Elektrony jsou vystřelovány na tenkou vrstvu – v tomto případě grafitu.
Rutherford měl štěstí, že de Broglieho vlnová délka částic α (kterou neznal) byla poměrně malá a coulombovské odpuzování se zastaví, když se příliš přiblíží – jinak by difrakční efekty zmátly data! (Zkuste si výpočet, pokud jste se již zabývali λ = hp.)
Epizoda 506-2: Interpretace elektronových difrakčních obrazců (Word, 30 KB)
Epizoda 522-5: Interpretace elektronových difrakčních obrazců: Hluboký nepružný rozptyl (Word, 56 KB)
Epizoda 522-6: Elektrony měří velikost jader (Word, 42 KB)
Diskuse: Hádanka pro příští hodinu
Rutherfordův model má jeden zásadní problém. Zeptejte se své třídy: Jak může být atom s centrálním jádrem stabilní – proč se nezhroutí? Podle klasické elektrodynamiky by elektrony měly při obíhání vyzařovat záření a spirálovitě se stáčet dovnitř.
(Je dobré nechat třídu s hádankou pro příští hodinu)
Stáhněte si tento díl
.