US Pharm. 2018;43(12):HS-2-HS-6.
ABSTRACT: Gastrointestinale blødninger (GIB’er) er en betydelig kilde til hospitalsindlæggelser i USA. GIB’er kategoriseres i to typer: øvre GI-blødninger og nedre GI-blødninger. Hver type kan vise sig med forskellige kendetegn og kræver forskellig behandling. Øvre GIB er afhængig af endoskopisk behandling og kan have gavn af forskellige farmakologiske behandlinger i specifikke scenarier, f.eks. protonpumpehæmmere og makrolider. Behandlingen af nedre GIB er fokuseret på koloskopi og mekanisk behandling af blødninger med ringe farmakologisk intervention. Farmaceuter kan yde effektiv service til disse patienter på flere forskellige punkter i patientplejen.
Gastrointestinale blødninger (GIB) er et relativt almindeligt medicinsk problem, der forårsager en betydelig del af morbiditet, hospitalsindlæggelser og endda dødelighed årligt i USA. Den rå estimerede rate af hospitalsindlæggelser sekundært til enhver form for GIB i USA anslås at være ca. 375 pr. 100.000 pr. år.1-3 For akutte GIB-hændelser identificerer nogle undersøgelser en 30-dages dødelighed på helt op til 14 %, mens andre rapporterer et interval på mellem 6 % og 10 % pr. år, med stigende rater hos patienter med stigende alder og et større antal associerede underliggende komorbiditeter.4-7 Det anslås, at der årligt bruges mere end 2,5 milliarder dollars til behandling af GIB på hospitalet.8
Givet karakteren af GIB er det vigtigt at differentiere sygdomstilstanden, da blødningens placering kan diktere både præsentation og behandling (TABELLER 1-3). Historisk set har man skelnet mellem øvre GIB (UGIB)og nedre GIB (LGIB) ud fra blødningens placering i forhold til ligament of Treitz.9,10 Med denne definition kategoriseres blødning proximalt i forhold til ligament of Treitz som en UGIB, mens blødning distalt i forhold til ligament of Treitz kategoriseres som en LGIB. Selv om der findes andre definitioner i en del litteratur, er denne definition generelt etableret i de fleste praksisser.11,12



Ved præsentation er udredningen af enhver formodet GIB indledningsvis ens, uanset hvor blødningen stammer fra. Umiddelbar evaluering bør fokusere på patientens hæmodynamiske stabilitet. Denne prioritet er blevet veletableret i andre hæmoragiske modeller og gælder fortsat i tilfælde af GIB.16-18 Fysisk vurdering af blodtryk, hjertefrekvens og ortostatisk status bør udføres, og der bør gives genoplivning efter behov. Denne genoplivning bør begynde med intravenøse væsker, men kan også kræve transfusioner af pakkede røde blodlegemer.
Den supplerende vurdering af patienter, der præsenterer sig med GIB, bør omfatte en fokuseret patienthistorie med henblik på at identificere blødningens art, varighed og potentielle kilde samt laboratorieundersøgelser (CBC, BMP, koagulationsundersøgelser).17,18 Når disse patienter vurderes ud fra et apotekersynspunkt, er det vigtigt at notere enhver nuværende eller nylig brug af medicin, der kan øge risikoen for blødning, herunder midler som ikke-steroide antiinflammatoriske lægemidler, trombocythæmmende midler og/eller antikoagulanter. Tidlig identifikation af disse faktorer kan bidrage til at fremskynde både diagnosen og et passende behandlingsrespons.
Risikovurdering og -stratificering er klinisk nyttig for at hjælpe med at skelne mellem patienter med høj og lav risiko for negative resultater.17,18 Ved at stratificere patienterne i evaluerede risikogrupper kan der træffes en indledende informeret beslutningstagning. Specifikt kan stratificering give indsigt i faktorer som f.eks. tidspunktet for endoskopi eller koloskopi, nødvendigt plejeniveau og tidspunktet for udskrivelse. Der findes forskellige etablerede værktøjer til hjælp til vurdering af individuel risiko.
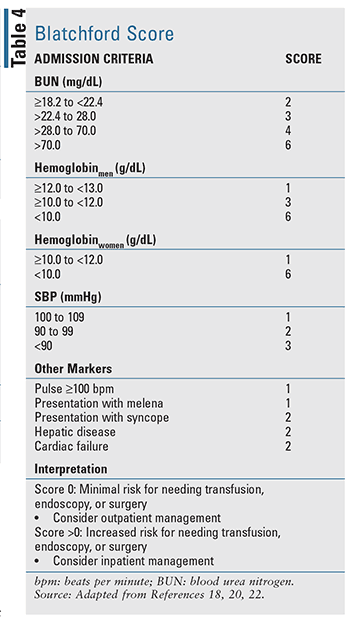
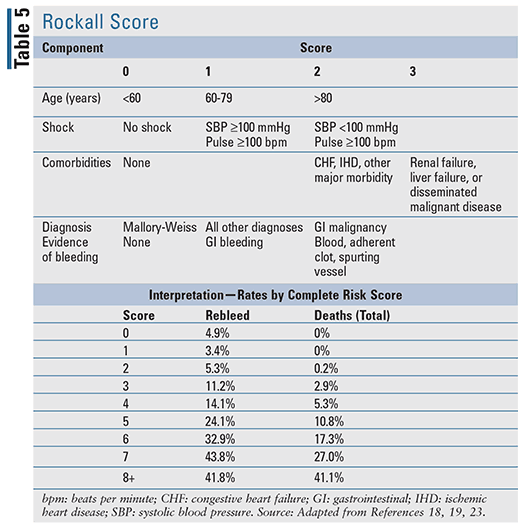
For patienter med akut UGIB er der udviklet flere kliniske forudsigelsesværktøjer, herunder to velvurderede værktøjer, der er citeret i evidensbaserede retningslinjer: Blatchford-score (TABEL 4) og Rockall-score (TABEL 5).17-20 Rockall-score anvender kliniske data umiddelbart ved præsentationen.19 Faktorer, der vurderer blødningens sværhedsgrad, såsom systolisk blodtryk og hjertefrekvens, vurderes sammen med patientkarakteristika, såsom alder og komorbide tilstande, hvilket resulterer i et værktøj til vurdering af prognostiske resultater og potentielt dødelighed. Tilsvarende bruger Blatchford-score både kliniske og laboratoriedata til at hjælpe med at forudsige risikoen for indgreb og dødelighed.20 For akut LGIB er de tilgængelige prognostiske regler til vurdering af risiko begrænsede og mindre validerede sammenlignet med UGIB.22
Farmakoterapi af øvre GI-blødninger
Protonpumpehæmmere (PPI’er) er den lægemiddelklasse, der er mest forbundet med behandling af UGIB. Hos en UGIB-patient kan mavesyre hæmme trombocytaggregation og svække den potentielle koagulation, hvilket fører til en forringelse af blødningsophør. For at hæmme denne proces kan hæmning af mavesyreudskillelsen, der har til formål at hæve mavens pH-værdi til 6 eller højere, bidrage til at stabilisere blodpropper og forbedre de kliniske resultater.24
PPI’er er unikke, idet de har potentiel anvendelse både før og efter endoskopi. I forbindelse med præ-endoskopi danner retningslinjerne ikke konsensus om deres anvendelse, men de kan mindske andelen af patienter med høj risiko for stigmata for blødning på tidspunktet for proceduren.25 På trods af potentielle fordele i denne population tyder evidensen på, at brugen af PPI ikke påvirker genblødning, nødvendig kirurgi eller dødelighed, hvilket fører til en vis klinisk kontrovers om deres anvendelse. Patienter, for hvem endoskopi ikke kan udføres eller vil blive forsinket, har imidlertid vist et potentielt fald i risikoen for genblødning ved brug af PPI. Beviserne tyder på, at PPI’er reducerer forekomsten af højrisikostigmata for blødning på tidspunktet for endoskopi, men påvirker ikke genblødning, nødvendig kirurgi eller mortalitet.17,26 Postendoskopisk behandling kan PPI’er anvendes både akut og kronisk.17
Kontinuerlig infusion versus intermitterende PPI
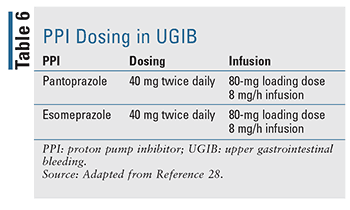
Den hensigtsmæssige dosering og administration af PPI er blevet nøje evalueret i de seneste år (TABEL 6). En bolus IV-dosis efterfulgt af infusion var længe det normale behandlingsforløb og er fortsat den foretrukne behandling i de aktuelt tilgængelige retningslinjer, men data tyder på, at to gange daglig IV-bolusdosering ikke er bedre med hensyn til resultater for genblødning, mortalitet og længde af hospitalsophold.17,27 Nyere litteratur har vist, at intermitterende PPI-anvendelse ikke var bedre og giver en klar fordel med hensyn til lægemiddeldosis, omkostninger og ressourceudnyttelse. Forfatterne foreslår, at retningslinjerne opdateres til at anbefale intermitterende PPI-behandling ved endoskopisk behandlet GIB.27 I praksis foretrækker mange institutioner nu intermitterende dosering for at mindske ressourceforbruget og de samlede omkostninger.
Intravenøs PPI versus intravenøs H2-antagonister
I betragtning af, at H2-antagonister (H2A’er) anvendes med samme hensigt i andre sygdomstilstande, er deres anvendelse i UGIB blevet undersøgt sammen med PPI’er. En metaanalyse fra 2015, der evaluerede de to klasser i forbindelse med UGIB, viste, at mens forskellen i mortalitet blev fundet ikke-signifikant, viste resultater som f.eks. recidivblødningsfrekvens og modtageoperationsfrekvens en klar fordel for PPI’er. Dette underskud skyldes sandsynligvis H2A’ernes underlegenhed med hensyn til at opretholde gastrisk pH over 6,0, den omtrentlige pH-værdi, hvor koagulationsprocesser kan fungere.29
Makrolider
I et forsøg på at forbedre visualiseringen under endoskopi og dermed mindske behovet for gentagen endoskopi, anvendes IV erythromycin, et antimikrobielt makrolid, der også fungerer som et prokinetisk middel, almindeligvis. En enkelt dosis på 250 mg eller 3 mg/kg tolereres generelt godt.17,30 En metaanalyse fra 2016 konkluderede, at brug af erythromycin før endoskopi signifikant reducerede behovet for anden endoskopi og længden af hospitalsopholdet, og derfor bærer det en anbefaling om at blive brugt i retningslinjerne fra European Society of Gastrointestinal Endoscopy.30,31
Det er rimeligt at spørge sig selv, om den mulige fordel er en klasseeffekt eller specifik for erythromycin. Azithromycin, et generelt mere almindeligt anvendt makrolid, er blevet evalueret og synes at være et ikke-inferior alternativ til erythromycin. Azithromycin kan have nogle logistiske fordele, såsom at det ikke kræver rekonstitution og generelt større tilgængelighed på grund af dets anvendelse i empirisk pneumonibehandling.32
H pylori Behandling
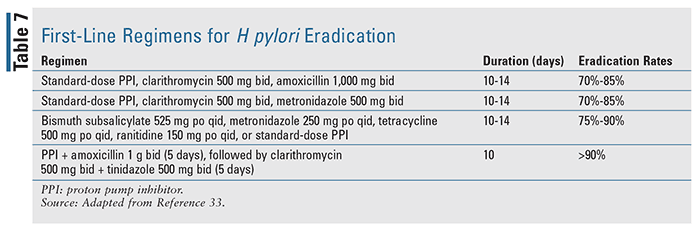
Patienter, der diagnosticeres med blødning i forbindelse med Helicobacter pylori-infektion, bør behandles via guideline-baseret eradikationsbehandling med det mål, at infektionen skal være fuldstændig opløst.17 Den tilgængelige litteratur viser, at eradikation af H pylori er betydeligt mere effektiv end antisekretorisk behandling alene hos patienter med UGIB. Førstelinjestyringsregimer til H pylori eradikation er beskrevet i TABEL 7 baseret på American College of Gastroenterology’s retningslinjer for håndtering af H pylori-infektion.33 Når infektionen er løst, behøver denne patientgruppe typisk ikke at modtage vedligeholdende antisekretorisk behandling, medmindre de har brug for ikke-steroide antiinflammatoriske lægemidler eller antitrombotisk behandling, hvormed langvarig antisekretorisk behandling er nødvendig, da brugen heraf kan øge risikoen for genblødning betydeligt.17,18
Behandlingsoversigt
Efter den indledende vurdering og risikostratificering, og når patienten er hæmodynamisk stabil, er koloskopi forud for kolonrensning den indledende diagnostiske procedure for de fleste patienter, der præsenterer sig med en LGIB.21 Håndtering af LGIB omfatter for det meste ikke-farmakologiske interventioner; der er dog stadig muligheder for farmaceuter til at blive involveret i patientplejen.
PPI-anvendelse ved LGIB
I modsætning til UGIB viser den tilgængelige litteratur, der evaluerer PPI-anvendelse ved LGIB, ingen fordele. Forsøg, der evaluerer UGIB og LGIB, har vist, at mens PPI’er ikke viser bedre resultater ved LGIB, kan de faktisk øge risikoen for LGIB.34 De teoretiserede mekanismer for denne øgede risiko fokuserer ofte på mulige ændringer i mikrobiotaen og kan således potentiere den mulige risiko fra NSAID’er. Disse resultater har vist sig at være kontroversielle; de giver dog bevis for, at patienter med LGIB ikke har gavn af PPI-behandling. Denne potentielle risiko bør vurderes omhyggeligt hos patienter, især dem med risiko for UGIB, da det kan være nødvendigt at foretage en omhyggelig vurdering af risiko kontra fordel.34
Apotekerens rolle
Apotekere fra mange specialer er i en unik position til at bistå i behandlingen og håndteringen af GIB-patienter. Ambulante farmaceuter er i en fortrinlig position til proaktivt at holde øje med potentielle risikofaktorer hos patienterne, herunder højdosis NSAID og antikoagulantia, og reducere risikoen for GIB i frontlinjen. Desuden kan de yde vigtig rådgivning og dosisoptimering til patienter både før og efter en GIB-diagnose. På samme måde kan kliniske farmaceuter på hospitaler også spille en stor rolle i forbindelse med GIB-behandling. De kan være i stand til at hjælpe på flere områder under den indledende evaluering og behandling. Den indledende medicinafstemning kan afsløre detaljer, der er relevante for diagnosen og behandlingen af patienterne, f.eks. identifikation af ambulant brug af NSAID eller antikoagulantia. Farmaceuter kan også give anbefalinger til sundhedsteamet om, hvilke lægemidler der kan være til gavn i hvert enkelt GIB-tilfælde.
1. El-Tawil A. Tendenser vedrørende gastrointestinal blødning og dødelighed: Hvor står vi? World J Gastroenterol. 2012;18(11):1154-1158.
2. Zhao Y, Encinosa W. Hospitalsindlæggelser for gastrointestinal blødning i 1998 og 2006. Statistical Brief #65. Healthcare Cost and Utilization Project (HCUP) statistical briefs. December 2008.
3. Whelan CT, Chen C, Kaboli P, et al. Upper versus lower gastrointestinal bleeding: a direct comparison of clinical presentation, outcomes, and resource utilization. J Hosp Med. 2010;5(3):141-147.
4. Wilcox CM, Cryer BL, Henk HJ, et al. Mortalitet forbundet med gastrointestinale blødningshændelser: sammenligning af kortvarige kliniske resultater for patienter indlagt for øvre GI-blødning og akut myokardieinfarkt i en amerikansk managed care-situation. Clin Exp Gastroenterol. 2009;2:21-30.
5. Garcia Rodriguez LA, Ruigómez A, Hasselgren G, et al. Sammenligning af dødelighed som følge af mavesårblødning mellem patienter med eller uden mavesår som forstadie. Epidemiology. 1998;9(4):452-456.
6. Wilcox CM, Clark WS. Årsager til og udfald af øvre og nedre gastrointestinale blødninger: Grady Hospital experience. South Med J. 1999;92:44-50.
7. Yavorski RT, Wong RK, Maydonovitch C, et al. Analyse af 3 294 tilfælde af øvre gastrointestinal blødning i militære medicinske faciliteter. Am J Gastroenterol. 1995;90:568-573.
8. Johanson JF. At bremse omkostningerne ved GI-blødninger. Am J Gastroenterol. 1998;93:1384-1385.
9. Scottish Intercollegiate Guidelines Network (SIGN). Håndtering af akut øvre og nedre gastrointestinal blødning. September 2008. www.sign.ac.uk/assets/sign105.pdf.
10. Kim, SK, Cho CD, Cho CD, Wojtowycz AR. Treitz-ligamentet (duodenums suspensionsligament): anatomisk og radiografisk korrelation. Abdom Imaging. 2008;33:395-397.
11. Matthew B, et al. Diagnosticering af gastrointestinal blødning: en praktisk vejledning for klinikere. World J Gastrointest Pathophysiol. 2014;5(4):467-478.
12. Raju GS, et al. American Gastroenterological Association (AGA) Institute medical position statement on obscure gastrointestinal bleeding. Gastroenterology. 2007;133(5):1694-1696.
13. Tielleman T, Bujanda D, Cryer B, et al. Epidemiologi og risikofaktorer for øvre gastrointestinal blødning. Gastrointest Endosc Clin N Am. 2015;25(3):415-428.
14. Rodriguez-Hernandez H, Rodríguez-Morán M, González JL, et al. Risikofaktorer forbundet med øvre gastrointestinal blødning og med dødelighed. Rev Med Inst Mex Seguro Soc. 2009;47(2):179-184.
15. Strate L. Lower GI bleeding: epidemiology and diagnosis. Gastroenterol Clin North Am. 2005;34(4):643-664.
16. Cocchi MN, Kimlin E, Walsh M, et al. Identifikation og genoplivning af traumepatienter i chok. Emerg Med Clin N Am. 2007;25:623-642.
17. Laine L, Jensen DM. Håndtering af patienter med blødning fra mavesår. Am J Gastroenterol. 2012;107:345-360.
18. Siau K, Chapman W, Sharma N, et alBehandling af akut øvre gastrointestinal blødning: en opdatering for den almene læge. J R Coll Physicians Edinb. 2017;47:218-230.
19. Rockall T, Logan R, Devlin H, et al. Risikovurdering efter akut øvre gastrointestinal blødning. Gut. 1996;38:316-321.
20. Blatchford O, Murray W, Blatchford M. A risk score to predict need for treatment for uppergastrointestinal haemorrhage. Lancet. 2000;356:1318-1321.
21. Recio-Ramirez, JM, Sánchez-Sánchez Mdel P, Peña-Ojeda JA, et al. Glasgow-Blatchford-scoreens prædiktive evne til risikostratificering af øvre gastrointestinale blødninger på en akutmodtagelse. Revista Española de Enfermedades Digestivas. 2015;107(5):262-267.
22. Strate L, Grainek IM. ACG Clinical Guideline: Behandling af patienter med akut nedre gastrointestinal blødning. Am J Gastroenterol. Forudgående onlinepublikation 1. marts 2016. 2016;111:459-474.
23. Bessa X, O’Callaghan E, Balleste B, et al. Anvendeligheden af Rockall-score hos patienter, der gennemgår endoskopisk behandling for øvre gastrointestinal blødning. Dig Liver Dis. 2006;38:12-17.
24. Chaimoff C, Creter D, Djaldetti M. Effekten af pH på trombocytaktiviteter og koagulationsfaktoraktiviteter. Am J Surg. 1978;136(2):257-259.
25. Sreedharan A, Martin J, Leontiadis GI, et al. Behandling med protonpumpehæmmere indledt før endoskopisk diagnose ved øvre gastrointestinal blødning. Cochrane Database Syst Rev. 2010(7):CD005415.
26. Leontiadis GI , Sharma VK , Howden CW. Protonpumpehæmmerbehandling ved blødning af mavesår: Cochrane-samarbejdets metaanalyse af randomiserede kontrollerede forsøg. Mayo Clin Proc. 2007;82:286-296.
27. Sachar H, Vaidya K, Laine L, et al. Intermitterende vs. kontinuerlig behandling med protonpumpehæmmere ved højrisikoblødning af mavesår: en systematisk gennemgang og metaanalyse. JAMA Intern Med. 2014;174(11):1755-1762.
28. Cheng H, Sheu B. Intravenøse protonpumpehæmmere til peptisk ulcusblødning: kliniske fordele og begrænsninger. World J Gastrointest Endosc. 2011;3(3):49-56.
29. Zhang YS, Li Q, He BS, et al. Behandling med protonpumpehæmmere vs. behandling med H2-receptorantagonister for øvre gastrointestinal blødning efter endoskopi: en meta-analyse. World J Gastroenterol. 2015;21(20):6341-6351.
30. Rahman R, Nguyen D, Sohail U, et al. Pre-endoskopisk erythromycinadministration ved øvre gastrointestinal blødning: en opdateret metaanalyse og systematisk gennemgang. Ann Gastroenterol. 2016,29:312-317.
31. Gralnek IM, Dumonceau JM, Kuipers EJ, et al. Diagnosticering og behandling af ikke-variceal øvre gastrointestinal blødning: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoskopi. 2015;47:1-46.
32. Issa D, Solomon S, Di Pace B, et al. A Comparison of Azithromycin to Erythromycin Infusions in Improving Visualization of Endoscopy for Upper Gastrointestinal Bleeding (En sammenligning af azithromycin til erythromycin-infusioner til forbedring af visualisering af endoskopi for øvre gastrointestinal blødning). Verdenskongres på ACG2017. Session 2A.
33. Chey WD, Wong BC. Udvalget for praksisparametre fra American College of Gastroenterology. American College of Gastroenterology guideline on the management of Helicobacter pylori infection. Am J Gastroenterol. 2007; 102:1808-1825.
34. Luée A, Lanas A. Protons pumpehæmmerbehandling og nedre gastrointestinale blødninger: afvejning af risici og fordele. World J Gastroenterol. 2016;22(48):10477-10481.