Fotoheterotrofer genererer ATP ved hjælp af lys på en af to måder: de bruger et bakterioklorofylbaseret reaktionscenter, eller de bruger en bakteriorhodopsin. Den klorofylbaserede mekanisme svarer til den, der anvendes i fotosyntesen, hvor lys exciterer molekylerne i et reaktionscenter og forårsager en strøm af elektroner gennem en elektrontransportkæde (ETS). Denne strøm af elektroner gennem proteinerne får hydrogenioner til at blive pumpet over en membran. Den energi, der er lagret i denne protongradient, bruges til at drive ATP-syntesen. I modsætning til i photoautotrofer flyder elektronerne kun i en cyklisk bane: Elektroner, der frigives fra reaktionscentret, flyder gennem ETS og vender tilbage til reaktionscentret. De anvendes ikke til at reducere nogen organiske forbindelser. Lilla ikke-svovlbakterier, grønne ikke-svovlbakterier og heliobakterier er eksempler på bakterier, der udfører dette skema for fotoheterotrofi.
Andre organismer, herunder halobakterier og flavobakterier og vibrios, har lilla-rhodopsin-baserede protonpumper, der supplerer deres energiforsyning. Den arkæale version kaldes bakteriorhodopsin, mens den eubakterielle version kaldes proteorhodopsin. Pumpen består af et enkelt protein, der er bundet til et A-vitaminderivat, retinal. Pumpen kan have accessoriske pigmenter (f.eks. carotenoider), der er knyttet til proteinet. Når lys absorberes af retinalmolekylet, isomeriseres molekylet. Dette får proteinet til at ændre form og pumpe en proton gennem membranen. Brint-iongradienten kan derefter bruges til at generere ATP, transportere faste stoffer gennem membranen eller drive en flagellarmotor. En bestemt flavobakterie kan ikke reducere kuldioxid ved hjælp af lys, men bruger energien fra sit rhodopsinsystem til at binde kuldioxid gennem anaplerotisk fiksering. Flavobakterien er stadig en heterotrof, da den har brug for reducerede kulstofforbindelser for at leve og ikke kan leve af lys og CO2 alene. Den kan ikke udføre reaktioner i form af
n CO2 + 2n H2D + fotoner → (CH2O)n + 2n D + n H2O,
hvor H2D kan være vand, H2S eller en anden forbindelse/forbindelser, der leverer de reducerende elektroner og protoner; 2D + H2O-parret repræsenterer en oxideret form.
Det kan imidlertid fiksere kulstof i reaktioner som:
CO2 + pyruvat + ATP (fra fotoner) → malat + ADP +Pi
hvor malat eller andre nyttige molekyler ellers opnås ved at nedbryde andre forbindelser ved
kulhydrat + O2 → malat + CO2 + energi.
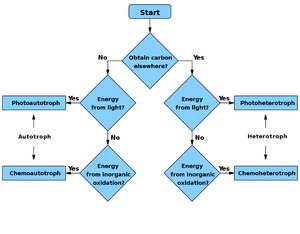
Denne metode til kulstoffiksering er nyttig, når reducerede kulstofforbindelser er knappe og ikke kan spildes som CO2 under interkonverteringer, men energi er rigeligt i form af sollys.