Hvad er PGS, præimplantationsgenetisk screening?
- PGS, præimplantationsgenetisk screening, henviser til at fjerne en eller flere celler fra et in vitro befrugtet embryo for at teste for kromosomal normalitet.
- PGS screener embryoet for normalt kromosomtal
- Mennesker har 23 par kromosomer – i alt 46
- Det giver problemer at have et ekstra kromosom eller et manglende kromosom
- Et eksempel er Downs syndrom, som har et ekstra kromosom nummer 21. Dette bør påvises ved PGS.
- PGS tester ikke for en specifik sygdom som f.eks. cystisk fibrose. Denne proces kaldes PGD (preimplantationsgenetisk diagnose).
Mange menneskelige embryoner er kromosomalt unormale
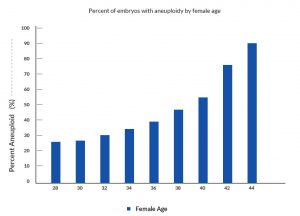
Flere undersøgelser har vist, at overordnet set er omkring 50 % af de menneskelige præimplantationsembryoner fra IVF kromosomalt unormale. Andelen af abnormiteter påvirkes i høj grad af kvindens alder, som det fremgår af nedenstående graf. Kromosomer i æg fra ældre kvinder har en signifikant øget rate af abnormiteter.
Hvad skal man gøre, hvis det første IVF-forsøg mislykkes
Problemer tidligere med aneuploidiescreening af IVF-embryoner
IVF og PGS for aneuploidi (et unormalt antal kromosomer) har været anvendt på nogle klinikker i USA siden midten af 1990’erne. Undersøgelser viste imidlertid, at udførelse af embryobiopsi på dag 3 og udførelse af den genetiske analyse ved hjælp af FISH-teknologi (fluorescerende in situ hybridisering) ikke resulterede i en forøgelse af patientens chance for at få en vellykket IVF-cyklus.
Der var 2 hovedproblemer med denne fremgangsmåde.
I nogle tilfælde vil kvinderne efter gentagne gange, hvor det ikke lykkedes at implantere nogen embryoner med IVF, sige;
- FISH-teknologien så normalt kun på 5 kromosomer ud af 23. Derfor ville FISH-testen overse mange kromosomale abnormiteter. Dette resulterede i, at unormale embryoner blev overført, efter at screeningstesten kom tilbage “normal”.
- Biopsierne på dag 3 fjernede en celle (eller 2 celler) fra et embryo med 6 til 10 celler. Dette krævede, at der blev lavet et relativt stort hul i embryoets skal og derefter fjernet en betydelig procentdel af embryoets “biomasse” (en sjettedel til en tiendedel af det fjernede eller mere).
Den seneste udvikling giver mulighed for bedre IVF-succesrater efter aneuploidiescreening
Fremskridtene på området har ført til anvendelse af forbedrede genetiske teknologier, der gør det muligt at vurdere alle 23 kromosompar.
Der findes i øjeblikket 4 teknologier, der kan anvendes til vurdering af normalitet af alle 23 kromosomer:
- Næste generations sekventering (NGS)
- Array Comparative Genomic Hybridization (aCGH)
- Single nucleotide polymorphism microarrays (SNP)
- Kvantitativ real time polymerase chain reaction (qPCR)
Comparative Genomic Hybridization (ofte benævnt CGH, eller aCGH) er en mikroarray-teknologi, der nu ofte anvendes i stedet for den ældre og langt mindre omfattende FISH. Med microarray CGH sammenlignes det faktiske DNA i embryoet med en kendt normal DNA-prøve ved hjælp af tusindvis af specifikke genetiske markører. Dette giver et mere nøjagtigt resultat med langt færre falske normale eller falske unormale resultater.
Nogle undersøgelser har fastslået, at fejlprocenten ved brug af array CGH-teknologi er ca. 2 %. FISH har en fejlprocent på ca. 5-10 %. Derudover ville mange andre unormale embryoner blive rapporteret af FISH som normale, fordi abnormiteten var i et kromosom, der ikke var en del af det anvendte FISH-panel.
Næste generations sekventering (NGS) er en nyere teknologi, som i stigende grad er blevet anvendt til testning af IVF-embryoner siden ca. 2015. NGS synes at være bedre til at detektere mindre segmentale ændringer sammenlignet med aCGH. Det menes også at være bedre til at detektere delvis aneuploidie og små ubalancerede translokationer. Mosaicisme er sandsynligvis mere sandsynligt at blive opdaget ved hjælp af Next Generation Sequencing.
Forbedringer i embryobiopsi-teknikker
Trophectodermbiopsi foretages på blastocyststadiet på dag 5 og 6. På dette stadium er der mange flere celler til stede i embryonet. Dette gør det muligt at fjerne flere celler fra trophectodermen (forstadier til placenta). De indre masseceller (forstadier til fosteret) kan efterlades uforstyrret under biopsien.
Med trophectoderm-biopsi afskæres der ca. 5 celler til genetisk undersøgelse. Dette svækker ikke embryoet væsentligt, da det har ca. 70-150 celler på dette stadium.
Kombinationen af disse to modifikationer (avanceret genetik og trophectoderm biopsi) har ført til væsentligt forbedrede succesrater for graviditet for patienter, der ønsker at benytte PGS til deres IVF-behandling.
Nogle klinikker i USA har brugt trophectoderm biopsi og de nyere genetiske teknologier til at screene embryoner hos nogle IVF-patienter. De resultater, der er set i nogle IVF-programmer (herunder vores), har været meget lovende.
- Vi ser væsentligt forbedrede igangværende graviditetsrater hos patienter, der får foretaget trophectodermbiopsi på blastocyststadiet med efterfølgende nedfrysning af deres embryoner.
- En cyklus med frosset optøet overførsel udføres, efter at resultaterne af kromosomanalysen er kommet tilbage
Problemer med livmoderens modtagelighed
Der er nogle interessante spekulationer om, at livmoderslimhinden kan være mindre modtagelig under en stimuleret cyklus sammenlignet med den kontrollerede eller “kunstige” embryoerstatningscyklus.
- Nogle fertilitetslæger mener, at overførsel af embryoner i en kontrolleret cyklus (ved hjælp af frosne embryoner) giver en højere graviditetsrate end i en “frisk” cyklus
- Dette er endnu ikke blevet nøje undersøgt med flere kontrollerede kliniske forsøg
- Den forbedrede succesrate, der ses efter blastocystbiopsi og omfattende kromosomanalyse skyldes hovedsageligt fordelen ved at overføre kromosomalt normale embryoner
- Hos nogle kvinder er der en vis yderligere fordel ved at overføre embryon(er) i en frossen optøet cyklus i stedet for i en stimuleret cyklus
Hvilke par bør vi tilbyde aneuploidiescreening til?
- Dette er i øjeblikket et spørgsmål under udvikling inden for reproduktionsmedicin
- Nogle potentielle kandidater kunne være:
- Kvinder over (ca.) 35 år, der foretager IVF
- Patienter i alle aldre, der har fejlet flere IVF-cyklusser. De ønsker svar på, hvorfor de mislykkes. De ønsker også at vide, hvad de skal gøre for at forbedre deres chancer for at få et barn. PGS giver nogle gange svar.
- PGS kan også give en “udrensning” af de unormale embryoner. Hvis f.eks. ét embryon ud af seks er kromosomalt normalt, og fem ud af seks er unormale – så overfører vi det ene normale embryon og skulle have en meget god chance for at få et barn.
- Par med tilbagevendende aborter
- Alle, der ønsker at bruge denne teknologi til at screene deres embryoner med henblik på at overføre et, der testes som kromosomalt normalt – og derfor har en høj chance for at implantere og lave et barn
Kostpris for PGD – PGS
Et andet spørgsmål er omkostningerne. PGD-omkostningerne i USA varierer fra ca. 3.000 til 9.000 dollars plus alle andre tilknyttede IVF-omkostninger. Der er PGD-relaterede omkostninger forbundet med selve embryobiopsiproceduren, og der er også omkostninger forbundet med det genetiske laboratorium, der udfører kromosomanalyse af cellerne.
- For at foretage PGD skal man først foretage IVF (og betale for) de almindelige IVF-omkostninger
- Dernæst er der udgifterne til biopsien og den genetiske analyse af cellerne
- Der kan der være yderligere gebyrer for den frosne embryooverførselscyklus, der foretages, efter at genetikresultaterne er kommet tilbage
PGD-omkostninger på vores center
Hvilke er de bedste PGD-klinikker?
Generelt vil de bedste klinikker til PGD eller PGS være de klinikker med de bedste IVF-succesrater. Det er afgørende at have et fremragende dyrkningssystem for at få et maksimalt antal kvalitetsblastocyster til biopsi.
Også er de færdigheder, der fører til høje succesrater med IVF, de samme færdigheder, der gør det lettere at udføre blastocystdyrkning, trophectodermbiopsi, blastocystvitrifikation (nedfrysning) og vellykkede frysetøede overførselscyklusser.
- Kontroller CDC- og SART-siderne for at finde en IVF-klinik i dit område med en god mængde sager og høje succesrater.
- Sørg for, at de har udført trophectoderm biopsier
- Og kom bare til vores klinik for IVF og PGD