Introduction
Chronic kidney disease (CKD) is highly prevalent worldwide. Kiinassa lähes yhdellä kymmenestä ihmisestä on jonkinasteinen munuaisten toimintahäiriö, yhteensä lähes 150 miljoonaa potilasta (1). Anemia ja sekundaarinen hyperparatyreoosi ovat kaksi yleisintä CKD:hen liittyvää komplikaatiota (2, 3). Itse asiassa on raportoitu, että lähes 90 prosenttia pitkälle edennyttä CKD:tä sairastavista potilaista (jotka luokitellaan CKD-vaiheisiin 4 ja 5) kärsii anemiasta (4). Anemian puhkeamisen ja vakavuuden on osoitettu korreloivan hyvin glomerulussuodatusnopeuden laskun kanssa (4). Anemian varhainen tunnistaminen, arviointi ja hoito voivat vähentää sairastuvuutta ja kuolleisuutta sekä parantaa elämänlaatua CKD-potilailla.
Sekundaariselle hyperparatyreoosille on ominaista seerumin kohonnut parathormonipitoisuus (PTH). Liiallinen PTH voi heikentää erytropoieesia kohdistamalla suoran toksisen vaikutuksen erytroidi progenitorisoluihin ja epäsuoran vaikutuksen luuytimen fibroosin indusoitumisen kautta (5, 6). Lisäksi uremiapotilaiden alhainen hemoglobiinipitoisuus on saattanut johtua korkean PTH-pitoisuuden aiheuttamasta erytrosyyttien osmoottisen haurastumisen lisääntymisestä (7). PTH:n ja hemoglobiinipitoisuuden välillä on todettu olevan käänteinen korrelaatio (8-10). Meytes ym. havaitsivat, että PTH-pitoisuudet, jotka olivat 7,5-30 U/ml, mikä on verrattavissa seerumin PTH-pitoisuuksiin uremisilla potilailla, aiheuttivat merkittävän burst forming unit-erythroid (BFU-E) -kasvun estymisen hiiren luuydinviljelmissä, mikä viittaa mahdolliseen reittiin, jonka kautta liiallinen PTH voi olla osallisena uremian anemian synnyssä (11).
Eryytropoieesia stimuloivista aineista (ESA) on tullut CKD-potilaiden anemian hoidon tunnusmerkki, ja ne ovat dialyysipotilaiden yleisimmin määrätty lääkitys, jonka käyttöaste Kiinassa on >95 % (1). Ensimmäinen ihmisen rekombinantti erytropoietiini, epoetiini alfa, sai myyntiluvan Yhdysvalloissa vuonna 1988 (12). Epoetiini-alfa ja epoetiini-beta ovat lyhytvaikutteisia ja kustannustehokkaita terapeuttisia aineita, ja niitä annetaan – yhdestä kolmeen kertaa viikossa useimmille CKD-potilaille. Niiden annostus kuitenkin kasvaa, kun annosteluväliä pidennetään hemoglobiinin tavoitetason saavuttamiseksi tai ylläpitämiseksi. Epiao® (3 000 μ/tuubi) on Kiinassa laajalti käytetty Epoetiini-alfa-valmiste, kun taas Recormon® (2 000 μ/tuubi) on Euroopassa yleisemmin käytetty Epoetiini-beta-valmiste, jota on käytetty Kiinassa noin neljä vuotta.
Viimeaikaisista kliinisistä tutkimuksista saadut tulokset ovat osoittaneet, että korkeisiin hemoglobiinitavoitteisiin yltävät annokset ovat herättäneet huolta lisääntyneestä kuolemanriskistä tai haitallisista lopputuloksista, kuten tromboembolisista tapahtumista ja aivohalvauksesta (13-16). Andrews ja muut havaitsivat, että lisääntynyt annostelutaajuus suurilla annoksilla lisäsi tromboottisten toksisuuksien esiintyvyyttä verrattuna eläimiin, joita annosteltiin harvemmin pienemmissä annosryhmissä, vaikka hematokriitti oli kaikissa ryhmissä yhtä korkea (17), mikä viittaa siihen, että korkea hematokriitti ei ole ainoa syyllinen tekijä, joka johtaa ESA-valmisteisiin liittyviin toksisuuksiin, vaan se liittyy myös annostasoon, annostelutaajuuteen ja annostelun kestoon. Näin ollen korkeasta hematokriitistä riippumattomiin ESA:han liittyviin toksisuuksiin on kiinnitettävä erityistä huomiota.
Tällä hetkellä on saatavilla vain vähän tietoa ESA-lääkkeiden annoksen ja PTH:n välisestä mahdollisesta yhteydestä uremisilla potilailla, joita pidetään säännöllisessä hemodialyysissä. Tämän retrospektiivisen tutkimuksen tarkoituksena oli tutkia ESA-lääkkeiden annoksen ja ehjän PTH:n (iPTH) pitoisuuksien välistä yhteyttä hemodialyysipotilailla sairaalamme tietokonetietokantajärjestelmässä olevien kliinisten tietojen perusteella.
Aineisto ja menetelmät
Potilaat ja menetelmät
Tämä retrospektiivinen kohorttitutkimus suoritettiin helmikuusta 2015 toukokuuhun 2015 Xiamenin Zhongshan-sairaalassa, Xiamenin yliopistossa, Kiinassa. Tähän tutkimukseen osallistui ureemisia potilaita, jotka olivat vähintään 3 kuukautta ylläpidetyssä hemodialyysissä ja jotka käyttivät ESA-lääkkeitä anemian hoitoon. Potilaat, jotka täyttivät seuraavat kriteerit, suljettiin tutkimuksen ulkopuolelle: (1) ikä <18 vuotta; (2) potilaat, joilla oli aktiivinen infektio, pahanlaatuinen sairaus, raudanpuuteanemia (määritelty ferritiininä <100 ng/ml ja saturaationa <20 %) tai aktiivinen verenvuoto 3 kuukauden kuluessa; (3) potilaat, joiden tiedot olivat puutteelliset. Tukikelpoiset potilaat luokiteltiin kahteen ryhmään käytetyn ESA:n perusteella: Recormon-ryhmä ja Epiao-ryhmä.
Tietojen keruu
Tiedot saatiin Xiamen Zhongshan -sairaalan Jinshida-tietokantajärjestelmästä, joka koodasi uudelleen 376 hemodialyysipotilaan kliiniset tiedot. Seuraavat tiedot kerättiin: ikä, sukupuoli, kuivapaino, ensisijaisten sairauksien diagnoosi, veren ureatyppi (BUN), seerumin kreatiniini (Scr), hemoglobiini, kalsium, fosfori, albumiini, iPTH, seerumin ferritiini, transferriinisaturaatio ja ESA-lääkkeiden annostus. Nämä tiedot mitattiin hemodialyysipäivän aamuna (ennen dialyysiä). Kidney Disease Improving Global Outcomes (KDIGO) -ohjeiden mukaisesti normaaliksi hemoglobiinipitoisuudeksi määriteltiin 110-130 g/l uremisilla potilailla, joiden hemodialyysia ylläpidettiin (8). Seerumin kalsiumin ja fosforin viitearvoiksi määriteltiin 2,1-2,54 mmol/l ja 1,1-1,78 mmol/l (18). Potilaat luokiteltiin edelleen iPTH-tasojen perusteella: 150, 300, 600 ja 1 500 pg/ml (19, 20).
Tutkimuksen etiikka
Tämä tutkimus toteutettiin analysoimalla sairaalamme sähköisestä potilastietojärjestelmästä saatuja retrospektiivisiä tietoja. Xiamenin yliopiston Zhongshanin sairaalan eettinen komitea hyväksyi ihmistutkimusta koskevan tutkimuspöytäkirjan. Kaikilta tutkittavilta saatiin kirjallinen tietoinen suostumus.
Tilastollinen analyysi
Tilastollinen analyysi suoritettiin SPSS for Windows -ohjelmiston versiolla 17.0. Tiedot ilmaistiin prosentteina tai keskiarvona ± keskiarvon keskivirhe (SEM). Demografisia tietoja ja laboratoriomittauksia ryhmien välillä verrattiin Pearsonin khiin neliö -testillä, Fisherin tarkalla testillä tai Yaten jatkuvuuden korjauksella. P-arvoa <0,05 pidettiin tilastollisesti merkitsevänä.
Tulokset
Säännöllistä hemodialyysiä saavien ureemisten potilaiden ominaisuudet
Tutkimukseen otettiin mukaan yhteensä 240 säännöllistä hemodialyysiä saavaa ureemista potilasta. Potilaiden perusominaisuudet on esitetty taulukossa 1. Recormon- ja Epiao-ryhmien välillä ei ollut merkittäviä eroja iässä, sukupuolessa, kuivapainossa, perussairauksissa, BUN:ssa, Scr:ssä, hemoglobiinissa, seerumin fosfaatissa, kalsiumissa, albumiinissa, seerumin ferritiinissä ja transferriinisaturaatiossa (taulukko 1, P > 0.05).

Taulukko 1. Potilaat, jotka olivat altistuneet ureatyremiselle. Potilaiden perusominaisuudet.
Kaikkien tutkittavien keskimääräinen hemoglobiinitaso oli 103,15 ± 1,07 g/l. Potilaita, joiden hemoglobiiniarvot olivat välillä 110-130 g/l, oli 30,4 % (n = 84). Anemia jaettiin hemoglobiinipitoisuuden perusteella viiteen luokkaan anemian vaikeusasteen mukaan (21, 22): hemoglobiinipitoisuus <60 g/L (2,1 %, n = 5), hemoglobiinipitoisuus ≥60 ja <90 g/L (21,7 %, n = 52), hemoglobiinipitoisuus <90 ja <110 g/L (38.7 %, n = 93), hemoglobiinitaso ≥110 ja <130 g/L (30,4 %, n = 73) ja hemoglobiinitaso ≥130 g/L (7,1 %, n = 17).
Anemian asteen ja iPTH:n välinen suhde
Analysoitiin anemian eri asteiden ja iPTH:n välistä yhteyttä. Tulokset osoittivat, että hemoglobiinitaso oli negatiivisesti yhteydessä iPTH:hen (kuva 1A; taulukko 2; P < 0,05). Anemian ja seerumin kalsium- tai fosforitason välillä ei kuitenkaan havaittu merkittävää yhteyttä (kuva 1B; taulukko 2; P > 0,05 molemmille).
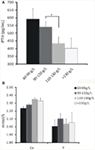
KUVIO 1. Anemian ja seerumin kalsium- tai fosforitason välinen yhteys. Hemoglobiinipitoisuuksien ja iPTH:n, seerumin kalsium- tai fosforipitoisuuksien välinen suhde. (A) Hemoglobiinipitoisuus kasvoi, kun iPTH-taso laski stratifikaation mukaan. (B) Hemoglobiinipitoisuuden ja seerumin kalsium- tai fosforitason välillä ei havaittu merkittävää yhteyttä. Tiedot laskettiin t-testillä. *P < 0.05.

Taulukko 2. Vertailun tulokset. Seerumin kalsium-, fosfori- ja iPTH-pitoisuuksien mittaukset hemoglobiiniarvojen perusteella osituksittain.
Potilailla, joiden iPTH-pitoisuus oli 150-300 pg/ml, oli korkeimmat hemoglobiini-, seerumin ferritiini- ja transferriinisaturaatiotasot
Kun iPTH-pitoisuus oli 150-300 pg/ml:n sisällä, hemodialyysipotilailla oli korkeimmat keskimääräiset hemoglobiini-, seerumin ferritiini- ja transferriinisaturaatiotasot; jotka olivat 106.25 g/L, 248,98 μg/L ja 30,97 % (kuva 2).
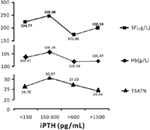
Kuva 2. Potilailla, joiden iPTH-pitoisuus oli 150-300 pg/ml, oli korkeimmat hemoglobiini-, seerumin ferritiini- ja transferriinisaturaatioarvot. Tiedot on ilmaistu prosentteina tai keskiarvona ± SEM.
Vertailu Recormonin ja Epiaon välillä anemian hoidossa
Potilailla, joita hoidettiin Recormonilla ja Epiaolla, oli samankaltaiset hemoglobiinipitoisuudet (103,54 ± 1,72 g/l, n = 98 vs. 102,59 ± 1,38 g/l, n = 142, P > 0,05; Kuva 3A). Recormon-annos (3 853,66 ± 225,13 μ/viikko, n = 98) anemian hoidossa oli kuitenkin merkittävästi pienempi kuin Epiao (7 083,33 ± 264,93 μ/viikko, n = 142, P < 0,05; Kuva 3B, Taulukko 1).
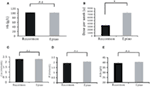
KUVIO 3. Anemian hoito. Recormonin ja Epiaon vertailu anemian hoidossa. (A) Recormonilla ja Epiaolla hoidettujen potilaiden hemoglobiiniarvot olivat samanlaiset (103,54 ± 1,72 g/l, n = 98 vs. 102,59 ± 1,38 g/l, n = 142, P > 0,05). (B) Recormonin annostus anemian hoitoon oli merkittävästi pienempi kuin Epiaon, 3 853,66 ± 225,13 μ/viikko, n = 98 vs. 7 083,33 ± 264,93 μ/viikko, n = 142. (C-E) Kalsium- (C), fosfori- (D) ja albumiinipitoisuuksissa (E) ei ollut merkittäviä eroja Recormon- ja Epiao-ryhmien välillä. Tiedot laskettiin t-testillä; P > 0.05.
Kalsium-, fosfori- ja albumiinipitoisuudet seerumissa eivät eronneet merkitsevästi Recormon- ja Epiao-ryhmien välillä (vastaavasti 2.27 ± 0,47 vs. 2,29 ± 0,01 mmol/l, P > 0,05; 1,94 ± 0,10 vs. 2,06 ± 0,04 mmol/l, P > 0,05; 39,5 ± 0,44 vs. 40,2 ± 0.35 g/L, P > 0.05; Kuviot 3C-E; Taulukko 1).
ESA-lääkkeiden annosten ja iPTH-pitoisuuksien välinen suhde
Kaikkien hemodialyysipotilaiden osalta iPTH-pitoisuudet olivat Recormon-ryhmässä alhaisemmat kuin Epiao-ryhmässä (336.66 ± 57,76 pg/ml, n = 98 vs. 531,05 ± 39,57 pg/ml, n = 142; P < 0,05; Kuva 4A; Taulukko 1). Samanlainen suuntaus havaittiin hemodialyysipotilailla, joiden hemoglobiiniarvot olivat välillä 110-130 g/l (319,50 ± 74,9 pg/mL Recormon-ryhmässä, n = 28 vs. 499,5 ± 64,38 pg/mL Epiao-ryhmässä, n = 45; P < 0,05; Kuva 4A).
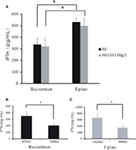
KUVA 4. Verenpainepitoisuus. ESA-lääkkeiden annoksen ja iPTH-tasojen välinen yhteys. (A) iPTH-taso Recormon- ja Epiao-ryhmissä. (B) Recormon-ryhmässä iPTH-tasot potilailla, joita hoidettiin Recormonilla 2 000 vs. 4 000 μ/viikko. (C) Epiao-ryhmässä iPTH-tasot potilailla, joita hoidettiin Epiaolla 3 000 ja >6 000 μ/viikko. Tiedot laskettiin t-testillä; *P < 0,05.
Potilaiden, joiden hemoglobiiniarvot olivat välillä 110-130 g/l, iPTH-taso oli 201,54 ± 42.67 pg/ml (n = 10) potilailla, joita hoidettiin Recormonilla 2000 μ/viikko, mikä oli merkittävästi alhaisempi kuin potilailla, joita hoidettiin Recormonilla 4000 μ/viikko (348,16 ± 117,9 pg/ml, n = 13; P < 0,05, kuva 4B). Vastaavasti keskimääräiset iPTH-tasot olivat Epiao-hoitoa saaneilla potilailla, joita hoidettiin 3 000 μ/viikko, merkitsevästi alhaisemmat kuin Epiao-hoitoa saaneilla potilailla, joita hoidettiin > 6 000 μ/viikko (347,15 ± 75,94 pg/ml, n = 12 vs. 661,01 ± 198,45 pg/ml, n = 27; P < 0,05, kuva 4C).
Keskustelu
Tämä retrospektiivinen tutkimus on ensimmäinen, joka tarjoaa näyttöä siitä, että suuremmat ESA-annokset (Epoetiini alfa ja -beeta) saattavat liittyä korkeampiin iPTH-pitoisuuksiin uremisilla potilailla, joita pidetään säännöllisessä hemodialyysissä. Lisäksi havaitsimme, että potilailla, joiden iPTH-pitoisuus oli 150-300 pg/ml, oli korkeimmat hemoglobiini-, seerumin ferritiini- ja transferriinisaturaatiopitoisuudet, mikä vastasi KDIGO-ohjeisiin (9) perustuvaa iPTH:n suositeltua tasoa.
Anemia on yksi CKD:n yleisimmistä komplikaatioista. Maailman terveysjärjestö on määritellyt anemian hemoglobiinipitoisuudeksi alle 13,0 g/dl miehillä ja vaihdevuosien jälkeisessä iässä olevilla naisilla tai hemoglobiinipitoisuudeksi <12,0 g/dl muilla naisilla. ESA-lääkkeiden käyttö paransi huomattavasti monien aneemisten CKD-potilaiden elämää. Suurten ESA-annosten on kuitenkin osoitettu liittyvän lisääntyneeseen haittavaikutusten riskiin CKD:tä sairastavilla aikuisilla ja lapsilla. Suurilla ESA-annoksilla hoidettujen potilaiden kuolleisuusriski on 1,2-1,5 prosenttia suurempi (23). Tässä tutkimuksessa havaitsimme merkitsevän käänteisen yhteyden iPTH-pitoisuuksien ja hemoglobiinipitoisuuksien välillä hemodialyysipotilailla, joita hoidettiin ESA-lääkkeillä, mikä vastaa aiempien tutkimusten havaintoja (8-10).
Tässä tutkimuksessa Recormon- ja Epiao-ryhmiin kuuluvilla potilailla oli samankaltaiset hemoglobiinipitoisuudet; Recormonissa käytetty annos oli kuitenkin huomattavasti pienempi kuin Epiaossa. Havaitsimme myös, että iPTH-taso oli Recormon-ryhmässä merkittävästi alhaisempi kuin Epiao-ryhmässä. Määrittääksemme tarkemmin ESA-lääkkeiden annoksen ja iPTH-tasojen välisen yhteyden analysoimme Recormonilla tai Epiaolla hoidettujen potilaiden kliiniset tiedot erikseen. iPTH-taso oli huomattavan matalampi Recormonilla 2000 μ/viikko hoidetuilla potilailla kuin Recormonilla 4000 μ/viikko hoidetuilla potilailla. Samanlainen suuntaus havaittiin potilailla, joita hoidettiin Epiaolla annoksella 3 000 tai 6 000 μ/viikko, mikä viittaa siihen, että suuret ESA-annokset voivat olla yhteydessä korkeisiin iPTH-tasoihin. Nämä havainnot osoittavat, että ESA-toksisuutta ei voida selittää pelkästään korkealla hematokriittitasolla. Koska suuret ESA-annokset voivat olla yhteydessä korkeisiin iPTH-pitoisuuksiin dialyysihoitoa saavilla potilailla, loppuvaiheen munuaistautia sairastavia potilaita voidaan hoitaa parhaiten minimoimalla ESA-annos tai pidättämällä se, erityisesti potilailla, joilla on äskettäisiä sydän- ja verisuoni- tai aivoverisuonitapahtumia, hypertensiivisiä hätätilanteita tai akuutteja tromboembolisia tapahtumia. Kun otetaan huomioon lisääntynyt sydän- ja verisuonitapahtumien riski lähes normaaleilla hemoglobiinipitoisuuksilla ja suurilla ESA-lääkeannoksilla CKD-potilailla, Taiwanissa ei itse asiassa suositella suhteettoman suurten ESA-lääkeannosten käyttämistä, jotta saavutettaisiin hemoglobiinitaso 100-110 g/l (24).
Vaikka anemian patogeneesi CKD:ssä on monitekijäistä, erytropoietiinin puute on pääasiallinen syy CKD-potilaiden anemiaan (25). Muita CKD:hen liittyvää anemiaa aiheuttavia tekijöitä ovat raudanpuute, tulehdusanemia, erytropoieesin suppressio, ureemisten toksiinien aiheuttama punasolujen eloonjäämisajan lyheneminen ja verenhukka, kuten ruoansulatuskanavan verenvuoto. Koska raudanpuute on myös yleinen anemian aiheuttaja, raudan suonensisäistä lisäravinteen antamista alettiin edistää Taiwanissa jo vuonna 1996. Taiwanissa CKD-anemian hoidosta saatujen kokemusten perusteella kohtuullinen hemoglobiinitavoite voidaan saavuttaa käyttämällä pienintä mahdollista ESA-annosta ja suonensisäistä rautalisää (24).
Tutkimuksessamme on useita rajoituksia. Ensinnäkin tämä havainnointitutkimus on yhden keskuksen tutkimus. Toiseksi, kun otetaan huomioon mahdolliset sekoittavat tekijät ja valintavirheet indikaation mukaan, näiden tietojen varovainen tulkinta on tarpeen. Havaintomme iPTH:n ja ESA-lääkkeiden välisestä yhteydestä edellyttävätkin lisätutkimuksia pitkittäisten prospektiivisten tutkimusten avulla. Kolmanneksi Epiao-valmisteella hoidettujen potilaiden määrässä on enemmistö (142 Epiao vs. 98 Rocormon), mikä johtuu todennäköisesti Epiaon suhteellisen edullisesta hinnasta Recormoniin verrattuna (taulukko 1). Neljänneksi farmakologiset interventiot, kuten verenpainelääkkeet, ovat saattaneet aiheuttaa ohimeneviä vaihteluita tai jopa häiriöitä iPTH- tai hemoglobiinipitoisuuksissa.
Johtopäätöksenä voidaan todeta, että tämä tutkimus osoittaa, että suuremmat ESA-lääkeannokset saattavat liittyä korkeampiin iPTH-pitoisuuksiin uremisilla potilailla, joita ylläpidetään säännöllisessä hemodialyysissä. Suurempien ESA-annosten osuus sekundaarisen hyperparatyreoosin patogeneesissä on edelleen epäselvä ja saattaa vaatia lisätutkimuksia. Tuloksemme viittaavat siihen, että pienimmän mahdollisen ESA-annoksen käyttämisellä voidaan minimoida mahdolliset riskit ja samalla saavuttaa kohtuullinen hemoglobiinitavoite.
Tekijöiden kontribuutiot
Käsikirjoituksen ovat tarkastaneet ja hyväksyneet kaikki kirjoittajat, eikä sitä ole harkittu julkaistavaksi muualla samankaltaisessa muodossa ja millään kielellä.
Erittely eturistiriidoista
Tekijät ilmoittavat, että tutkimus tehtiin ilman kaupallisia tai taloudellisia suhteita, jotka voitaisiin tulkita mahdolliseksi eturistiriidaksi.
Rahoitus
Tämä tutkimus sai tukea Fujianin maakunnan lääketieteellisen innovaatio-ohjelman rahastosta (nro 2011027).
Lyhenteet
BUN, veren ureatyppi; CKD, krooninen munuaissairaus; ESA, erytropoieesia stimuloiva aine; Hb, hemoglobiini; iPTH, ehjä lisäkilpirauhashormoni; Scr, seerumin kreatiniini.
1. Johtopäätökset. Zhang L, Wang F, Wang L, Wang W, Liu B, Liu J, et al. Prevalence of chronic kidney disease in China: a cross-sectional survey. Lancet (2012) 379:815-22. doi: 10.1016/S0140-6736(12)60033-6
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Martin KJ, Gonzalez EA. Metabolinen luusairaus kroonisessa munuaissairaudessa. J Am Soc Nephrol (2007) 18:875-85. doi:10.1681/ASN.2006070771
PubMed Abstract | CrossRef Full Text | Google Scholar
3. Rodriguez M, Nemeth E, Martin D. The calcium-sensing receptor: a key factor in the pathogenesis of secondary hyperparathyroidism. Am J Physiol Renal Physiol (2005) 288:F253-64. doi:10.1152/ajprenal.00302.2004
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
4. Fysiologiset tutkimukset. Levin A, Thompson CR, Ethier J, Carlisle EJ, Tobe S, Mendelssohn D, et al. Left ventricular mass index increase in early renal disease: impact of decline in hemoglobin. Am J Kidney Dis (1999) 34:125-34. doi:10.1016/S0272-6386(99)70118-6
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
5. Kwack C, Balakrishnan VS. Erytropoietiinihyporesponsiivisuuden hallinta. Semin Dial (2006) 19:146-51. doi:10.1111/j.1525-139X.2006.00141.x
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
6. Gallieni M, Corsi C, Brancaccio D. Hyperparatyreoosi ja anemia munuaisten vajaatoiminnassa. Am J Nephrol (2000) 20:89-96. doi:10.1159/000013563
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
7. Wu SG, Jeng FR, Wei SY, Su CZ, Chung TC, Chang WJ, ym. punasolujen osmoottinen fragiliteetti kroonisesti hemodialysoiduilla potilailla. Nephron (1998) 78:28-32. doi:10.1159/000044878
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Baradaran A, Nasri H. Anemian voimistuminen sekundaarisen hyperparatyreoosin vuoksi hemodialyysipotilailla. Med J Islam Acad Sci (2001) 14(4):161-6.
Google Scholar
9. Med J Islam Acad Sci (2001) 14(4):161-6. Sliem H, Tawfik G, Moustafa F, Zaki H. Liitännäisen sekundaarisen hyperparatyreoosin suhde seerumin fibroblastikasvutekijä-23:een loppuvaiheen munuaistaudissa: tapaus-kontrollitutkimus. Indian J Endocrinol Metab (2011) 15:105-9. doi:10.4103/2230-8210.81939
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
10. Tiedonantajat ja lääkärit. Trovato GM, Carpinteri G, Spina S, Squatrito G, Catalano D, Iannetti E. Hyperparatyreoosi, anemia ja erytropoietiini: vaikutukset dialyysipotilaiden systoliseen toimintaan. Abstracts of 31 st Congress of European Renal Association/European dialysis ND Transplantation Association, September 5-8, 1999 Madrid. Nephrol Dial Transpl (1999) 14:190.
Google Scholar
11. Nephrol Dial Transpl (1999) 14:190. Meytes D, Bogin E, Ma A, Dukes PP, Massry SG. Lisäkilpirauhashormonin vaikutus erytropoieesiin. J Clin Invest (1981) 67:1263-9. doi:10.1172/JCI110154
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Eschbach JW, Abdulhadi MH, Browne JK, Delano BG, Downing MR, Egrie JC ym Recombinant human erythropoietin in anemic patients with end-stage renal disease. Vaiheen III monikeskuksisen kliinisen tutkimuksen tulokset. Ann Intern Med (1989) 111(12):992-1000. doi:10.7326/0003-4819-111-12-992
PubMed Abstract | CrossRef Full Text | Google Scholar
13. TUTKIMUSOHJELMA. Besarab A, Bolton WK, Browne JK, Egrie JC, Nissenson AR, Okamoto DM, et al. The effects of normal as compared with low hematocrit values in patients with cardiac disease who are receiving hemodialysis and epoetin. N Engl J Med (1998) 339:584-90. doi:10.1056/NEJM199808273390903
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
14. Singh AK. Pitäisikö hemoglobiiniarvot säilyttää käyttökelpoisena tulosmittarina? Nephrol News Issues (2010) 24(15-6):18.
PubMed Abstract | Google Scholar
15. Phrommintikul A, Haas SJ, Elsik M, Krum H. Kuolleisuus ja tavoitehemoglobiinipitoisuudet aneemisilla potilailla, joilla on krooninen munuaissairaus ja joita hoidetaan erytropoietiinilla: meta-analyysi. Lancet (2007) 369:381-8. doi:10.1016/S0140-6736(07)60194-9
PubMed Abstract | CrossRef Full Text | Google Scholar
16. TUTKIMUKSET JA TUTKIMUKSET. Regidor D, McClellan WM, Kewalramani R, Sharma A, Bradbury BD. Muutokset erytropoieesia stimuloivan aineen (ESA) annostelussa ja hemoglobiinipitoisuuksissa yhdysvaltalaisilla kroonista munuaissairautta sairastavilla ei-dialyysipotilailla vuosina 2005-2009. Nephrol Dial Transplant (2011) 26:1583-91. doi:10.1093/ndt/gfq573
PubMed Abstract | CrossRef Full Text | Google Scholar
17. Nephrol Dial Transplant (2011) 26:1583-91. dec. Andrews DA, Pyrah ITG, Boren BM, Tannehill-Gregg SH, Lightfoot-Dunn RM. Erytropoieesia stimuloivien aineiden antamisesta johtuva korkea hematokriitti ei täysin ennusta kuolleisuutta tai toksisuutta prekliinisissä lajeissa. Toxicol Pathol (2014) 42:510-23. doi:10.1177/0192623313486317
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
18. Ks. Munuaissairaus: Improving Global Outcomes (KDIGO) CKD-MBD-työryhmä. KDIGO Clinical Practice Guideline for the diagnosis, evaluation, prevention, and treatment of Chronic Kidney Disease-Mineral and Bone Disorder (CKD-MBD). Kidney Int Suppl (2009) 113:S1-130. doi:10.1038/ki.2009.188
CrossRef Full Text | Google Scholar
19. Käypä hoito. Tentori F, Blayney MJ, Albert JM, Gillespie BW, Kerr PG, Bommer J, et al. Kuolleisuusriski dialyysipotilailla, joilla on erilaiset seerumin kalsium-, fosfori- ja PTH-tasot: Dialysis Outcomes and Practice Patterns Study (DOPPS). Am J Kidney Dis (2008) 52(3):519-30. doi:10.1053/j.ajkd.2008.03.020
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
20. DOPPSY. National Kidney Foundation. K/DOQI Clinical Practice Guidelines for chronic kidney disease: Evaluation, classification, and stratification. Am J Kidney Dis (2002) 39(2 Suppl 1):S1-266.
Google Scholar
21. Google Scholar
. Pisoni RL, Bragg-Gresham JL, Young EW, Akizawa T, Asano Y, Locatelli F, et al. Anemian hoito ja tulokset 12 maasta Dialysis Outcomes and Practice Patterns Study (DOPPS) -tutkimuksessa (DOPPS). Am J Kidney Dis (2004) 44(1):94-111. doi:10.1053/j.ajkd.2004.08.005
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Munuaissairaus: KDIGO:n (KDIGO) anemiatyöryhmä. KDIGO clinical practice guideline for anemia in chronic kidney disease. Kidney Int Suppl (2012) 2:279-335.
Google Scholar
23. Kidney Int Suppl (2012) 2:279-335. Suttorp MM, Hoekstra T, Mittelman M, Ott I, Krediet RT, Dekker FW, et al. Treatment with high dose of erythropoiesis-stimulating agents and mortality: analysis with a sequential Cox approach and a marginal structural model. Pharmacoepidemiol Drug Saf (2015) 24(10):1068-75. doi:10.1002/pds.3855
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Hung SC, Kuo KL, Tarng DC, Hsu CC, Wu MS, Huang T-P. Anemian hallinta kroonista munuaissairautta sairastavilla potilailla: Taiwanin käytännön ohjeet. Nephrology (Carlton) (2014) 19:735-9. doi:10.1111/nep.12332
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Randolph JF, Scarlett JM, Stokol T, MacLeod JN. Rekombinantti koiran erytropoietiinin kliininen teho ja turvallisuus koirilla, joilla on kroonisen munuaisten vajaatoiminnan aiheuttama anemia, ja koirilla, joilla on rekombinantti ihmisen erytropoietiinin aiheuttama punasoluaplasia. J Vet Intern Med (2004) 18:81-91. doi:10.1111/j.1939-1676.2004.tb00139.x
CrossRef Full Text | Google Scholar