Kun olet selvittänyt ytimen olemassaolon, voit nyt tarkastella kokeellisia todisteita sen koosta, alkaen Rutherfordin kokeesta.
Yhteenveto oppitunnista
- Keskustelua ja harjoiteltu esimerkki: Ytimen koko (15 minuuttia)
- Keskustelu: Atomin ja ytimen koko (10 minuuttia)
- Opiskelijoiden kysymykset: Forces and closest approach (30 minuuttia)
- Discussion: (5 minuuttia)
- Keskustelu: Ytimen koon yläraja (30 minuuttia)
- Keskustelu: (5 minuuttia)
Keskustelu ja työstetty esimerkki: Ytimen koko
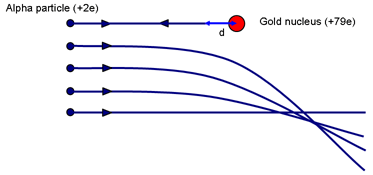
Voit saada käsityksen ytimen mahdollisesta koosta ajattelemalla Rutherfordin koetta. Kysykää: Mikä vaikutusparametri johtaa siihen, että hiukkanen pääsee lähimmäksi ydintä? (Päällekkäinen törmäys, jossa p = 0.)
Energian säilymisperiaatetta käytetään laskettaessa lähimmän lähestymisen etäisyyttä ytimen koon mittana. Seuraavan laskutoimituksen ymmärtäminen riippuu siitä, ovatko oppilaat käsitelleet sähköpotentiaalia ja kenttiä. Vaihtoehtoisesti se toimii hyvänä kertauksena.
Jakso 522-1: Alfahiukkasten sironta – lähimmän lähestymisen etäisyys (Word, 29 KB)
Jakso 522-2: Lähimmän lähestymisen etäisyys (Word, 107 KB)
Kun α saatetaan hetkeksi lepäämään paikalleen (kun se on kiivennyt niin pitkälle kuin mahdollista sähköstaattista kukkulaa pitkin ylöspäin), ytimestä tulevan hylkivän voiman vastapainoksi on tehty työtä. α:n liike-energia on varastoitunut ytimen ympärillä olevaan kenttään. Kun nopeus on nolla, kaikki energia on nyt varastoitunut kenttään.
Jos α pysähtyy hetkellisesti ollessaan etäisyydellä d varauksen Ze omaavasta ytimestä (sen keskipisteestä), kentässä oleva energia on:
Eα = 14πε0 2e Zed
Tämä vastaa α-hiukkasen alkuperäistä liike-energiaa. Rutherford käytti madame Curien hänelle antamaa α-lähdettä. α:n energia oli ~ 7,7 MeV.
Kullalle Z = 79. Ratkaisemalla saadaan d ~ 3 × 10-14 m. Vertaa tätä kulta-atomien halkaisijaan ~ 3 × 10-10 m. Ydin on siis ainakin 10 000 kertaa pienempi kuin atomi. On tärkeää korostaa, että tämä laskelma antaa ylärajan kullan ytimen koolle; emme voi sanoa, että alfahiukkanen koskettaa ydintä; energisempi α saattaisi päästä vielä lähemmäs.
Atomi on suurimmaksi osaksi tyhjä (siksi suurin osa as meni suoraan läpi – mahdolliset elektronit tuskin estäisivät suhteellisen massiivista, suurnopeuksista α:ta).
Keskustelu: Atomin ja ytimen koko
Pyydä oppilaita ehdottamaan pienoismallia ydinatomista. Esimerkiksi: Jos ydin olisi halkaisijaltaan 1 mm, atomi olisi 10 000 kertaa suurempi eli halkaisijaltaan 10 m. Valitse sopiva paikka 1 mm:n ytimelle (pieni kuulalaakeri tai Blu-tac-pallo). Siirry 5 m (viisi suurta askelta) atomin reunaan, jossa elektronit ovat. HUOM: oppikirjan kaavioita atomista, jossa on ydin, ei ole piirretty mittakaavaan.
Vahvista tarkkaa kuvaa pyytämällä oppilasta nousemaan ytimen paikalle, arvioimaan ympärysmittaansa (40 cm?) ja kysymään, missä toisen oppilaan olisi pitänyt seistä ollakseen atomin reunalla. 104 × 40 cm = 4000 m}, joten tämän atomin säde on 2 km! Tarkista paikalliselta kartalta, että löydät nimetyn paikan, jonka oppilaat tunnistavat ja joka on 2 km:n päässä.
Lisävahvistus: kiinteässä aineessa, jossa atomit ovat tiiviisti pakkautuneita, vierekkäisten ytimien välinen etäisyys ~ atomin kokoinen, eli vastaa kahden oppilaan seisomista 4 km:n etäisyydellä toisistaan!
Se on siis melko hämmästyttävää, että jokin osuu ytimeen ylipäätään. Molemmat ovat samankokoisia. Ytimen esittämä poikkileikkauspinta-ala ~säde2, joten ~1 × 10-28 m2}.
Kysy: Miten odottaisit heijastumien määrän riippuvan kohdeytimiä sisältävän metallifolion paksuudesta? (Kuvittele kulta-atomit kerroksittain, poikkeaman mahdollisuus kasvaa paksuuden kasvaessa, mutta absorptio matkalla sisään tai ulos yhä paksummasta kalvosta estää lopulta heijastuneiden ja havaittujen lukumäärän lisääntymisen entisestään.
On suuri apu, jos oppilaat voivat palauttaa mieleen seuraavat suuruusluokat:
Atomiytimen säde ~ 10 -14m
Atomin säde ~ 10 -10m
Opiskelijoiden kysymykset:
Jakso 522-3: Rutherfordin sironta: (Word, 82 KB)
Jakso 522-4: Rutherfordin sironta: (Word, 83 KB)
Keskustelu: Atomiluku ja ytimen varaus
Rutherford käytti tietojaan löytääkseen kullan kohdeytimen varauksen. Jatkokokeet Cu-, Ag- ja Pt-kalvojen varauksen selvittämiseksi antoivat:
| Atomiluku | Sirontakoe | |
| Cu | 29 | 29.3 × e |
| Ag | 47 | 46.3 × e |
| PT | 78 | 77.4 × e |
Ytimen sähkövaraus saadaan siis atomiluku × e:n avulla eli Z e. Yhtä poikkeusta lukuun ottamatta (vety, H-1) Z on aina pienempi kuin atomimassaluku. Mikä siis selittää eron? Atomin on oltava sähköisesti neutraali. Rutherford ehdotti neutronia.
Keskustelu: Ytimen koon yläraja
Muistetaan, että Rutherfordin analyysi antaa ytimen koon ylärajan (d ~ 1 α hiukkasen energia). Mitattava koko riippuu käyttämäsi α-hiukkasen energiasta. Tarvitsemme siis toisen lähestymistavan kullan ytimen koon määrittämiseksi. Keksitkö paremman hiukkasen ytimen koon mittaamiseen? (Neutroni – koska se on varaukseton, se pääsee lähemmäksi.)
Toinen tekniikka on elektronien syvä kimmoton sironta. Viittaa takaisin, jos olet jo käsitellyt hiukkasten aaltoluonnetta (de Broglie-aallot λ = hp), tai tämän aiheen voi halutessaan lisätä tähän. Elektronien diffraktiolaitteistolla on perusyhtäläisyyksiä hiukkassirontaan. Elektronit ammutaan ohueen kalvoon – tässä tapauksessa grafiittiin.
Rutherfordilla oli onni, että α-hiukkasten (hänelle tuntemattomien) de Broglie-aallonpituus oli melko pieni, ja coulombin repulsio pysähtyy, kun päästään liian lähelle – muutoin diffraktiovaikutukset olisivat sekoittaneet tiedot! (Kokeile laskentaa, jos olet jo käsitellyt λ = hp.)
Jakso 506-2: Elektronien diffraktiokuvioiden tulkinta (Word, 30 KB)
Jakso 522-5: Syvä inelastinen sironta (Word, 56 KB)
Episodi 522-6: Elektronit mittaavat ytimien kokoa (Word, 42 KB)
Keskustelu: Tulevan oppitunnin arvoitus
Rutherfordin mallissa on perustavanlaatuinen ongelma. Kysy luokaltasi: Miten atomi, jossa on keskeinen ydin, voi olla vakaa – miksi se ei romahda? Klassisen elektrodynamiikan mukaan elektronien pitäisi lähettää säteilyä kiertäessään ja kiertyä spiraalimaisesti sisäänpäin.
(On hyvä jättää luokalle arvoitus tulevaa oppituntia varten.)