TOIMINTA
Vasemman etummaisen laskevan sepelvaltimon proksimaalisen segmentin ahtauma (pAD) on erityinen iskeemisen sydänsairauden alaryhmä, kun otetaan huomioon näiden leesioiden korkea riskiprofiili, joka niillä on yksinään,1,2 tai usean valtimon taudin yhteydessä.3 Vaarassa olevan sydänlihaksen määrä ja laatu, joka riippuu pAD:n läpäisevyydestä, edellyttää aggressiivisempaa terapeuttista lähestymistapaa. Tämäntyyppisten vaurioiden in vivo -ultraäänitutkimukset ovat osoittaneet, että verisuonet ovat pääasiassa eksentrisiä.4 Tämä selittäisi huonommat tulokset, joita näissä vaurioissa on saatu perkutaanisen transluminaalisen sepelvaltimoiden pallolaajennuksen (PTCA) jälkeen, mikä johtuu elastisen vetäytymisen ilmiöstä. Useissa tutkimuksissa on vertailtu näiden leesioiden hoitostrategioita, joissa interventiohoidon (sepelvaltimoiden revaskularisaatiokirurgia sisäisen rintavaltimon siirteellä tai perkutaaninen revaskularisaatio verrattuna tavanomaiseen lääkehoitoon) jälkeen on yleensä havaittu parempia tuloksia.5-12 Tässä tutkimuksessa arvioidaan stentti-implantoinnin tehokkuutta ja pitkäaikaisturvallisuutta tämäntyyppisissä leesioissa, ja se tehtiin, koska tätä aihetta koskevia tutkimuksia on alueellamme vähän.
MENETELMÄT
Tutkimuspopulaatio
Tutkimusjoukko
Laboratorioomme huhtikuun 1995 ja huhtikuun 1998 välisenä aikana ohjattuja peräkkäisiä potilasta otettiin mukaan prospektiiviseen, satunnaistamattomaan kliiniseen seurantatutkimukseen, johon osallistui 98 potilasta. Tänä aikana tehtiin 1136 PTCA-toimenpidettä, ja tutkimusryhmä edustaa 8,6 % kaikista laboratoriossamme tänä aikana tehdyistä interventiotoimenpiteistä. Seuranta päättyi toukokuussa 2000.
Sisäänotto- ja poissulkukriteerit
Potilaat, joilla oli merkittävä pAD:n ahtauma (yli 70 %:n ahtauma visuaalisesti arvioituna) ennen ensimmäistä septalhaaraa ja suurempaa diagonaalihaaraa ja joilla oli näyttöä iskemian esiintymisestä pAD:sta riippuvaisella alueella, katsottiin kelpuutetuiksi tutkimukseen. Potilaille tehtiin suunnitelmallisesti perkutaaninen pallovaskularisaatio ja stentti-implantointi. Akuutin sydäninfarktin (AMI) yhteydessä lähetetyt potilaat suljettiin pois, samoin kuin vauriot, joiden anatomia ei soveltunut toimenpiteeseen operaattorin arvion mukaan, erityisesti vauriot, joissa oli krooninen tukos ja massiivinen kalkkeutuminen. Kaikki potilaat allekirjoittivat tietoon perustuvan suostumuksen ennen revaskularisaation suorittamista. Tutkimusryhmään kuuluivat kaikki potilaat, joilla oli pAD-leesioita, jotka oli hoidettu laboratoriossamme kyseisenä ajanjaksona.
Toimenpideprotokolla (PTCA+stentin istuttaminen)
Kaikkiin tapauksiin PTCA suoritettiin vaskulaarisen pääsyn kautta reisivaltimon kautta, ja stentti implantoitiin (pallolaajennuksen jälkeen) päästämällä se irti korkeassa paineessa (12-14 ilmakehää). Palmaz-Schatz- ja NIR-stentit (eniten käytetyt mallit) asennettiin manuaalisesti pallolaajennuspalloon. Tutkimuksen viimeisessä vaiheessa käytettiin palloon valmiiksi kiinnitettyjä stenttejä. ”Toimenpiteen angiografinen onnistuminen” määriteltiin siten, että jäännösvaurioita oli alle 30 prosenttia visuaalisesti arvioituna segmentissä, johon stentti oli istutettu. ”Alentunut ejektiofraktio (EF)” määriteltiin siten, että EF oli alle 50 prosenttia visuaalisen arvioinnin perusteella. ”Monisuonitauti” määriteltiin siten, että kahdessa tai useammassa verisuonessa oli merkittäviä sepelvaltimovaurioita (yli 70 %:n ahtaumat silmämääräisesti arvioituna). Kaikki potilaat saivat verihiutaleiden aggregaation estäjähoitoa asetyylisalisyylihapolla määräämättömän ajan ja tiklopidiinihoitoa yhden kuukauden ajan pallolaajennuksen jälkeen. Ennen toimenpidettä annettiin i.v. boluksena 7500-10 000 IU hepariinia potilaan painosta riippuen, jotta saatiin yli 300 s:n osittainen tromboplastiinin aktivoitumisaika.
Seurantaprotokolla
Kaikki potilaat osallistuivat vuosittaiseen kliiniseen seurantaan henkilökohtaisesti tai puhelimitse. Kaikille tehtiin hoitavan kardiologin määräämät testit iskemian toteamiseksi. Tapauksissa, joissa testitulokset olivat epäilyttäviä tai kliinisten oireiden ja testitulosten välillä oli ristiriitaisuuksia, tilasimme uusia testejä sepelvaltimotaudin havaitsemiseksi (uusia rasituskokeita tai radionukliditutkimuksia). Viimeinen käynti oli henkilökohtainen, ja silloin tehtiin kliininen anamneesi, fyysinen tutkimus ja EKG. Potilaille, joilla angina pectoris jatkui vakavuuden kliinisten kriteerien mukaisesti, tehtiin angiografinen uudelleenarviointi suoraan laboratoriossa. Angiografinen restenoosi määriteltiin yli 50 %:n ahtaumaksi stenttiimplantaatiolla hoidetussa pAD-segmentissä.
Tutkimusryhmässä kirjattiin joukko muuttujia myöhempää analyysia ja potilaiden kliinisen kehityksen ennustetekijöiden määrittämistä varten. Nämä muuttujat olivat:
— Kliiniset: ikä, sukupuoli, diagnoosi ennen katetrointia, diabetes mellituksen, valtimoverenpainetaudin, tupakoinnin ja dyslipidemian esiintyminen. Useita riskitekijöitä katsottiin olevan olemassa, kun niihin liittyi vähintään kolme klassista riskitekijää.
— Anatomiset: monisuonisairauden esiintyminen, vasemman kammion toimintahäiriö.
— Toimenpide: stentin pituus ja läpimitta, käytettyjen stenttien lukumäärä, stenttityyppi ja ostiaalisen leesion esiintyminen.
Lopputapahtumat
Sairaalahoidon aikana ja myöhemmässä seurannassa kirjattiin merkittävien haitallisten sydäntapahtumien (MACE, major adverse cardiac events) tai merkittävien komplikaatioiden esiintyvyys, jotka määriteltiin seuraavasti: sydänperäinen kuolema, uuden AMI:n ilmaantuminen ja uuden pAD-revaskularisaation tarve. Muut kuin sydänperäiset kuolemantapaukset ja pAD:sta poikkeavien verisuonten revaskularisaation tarve kirjattiin.
Tilastollinen analyysi
Eri muuttujat koottiin Microsoft Access® -tietokantaan ja analysoitiin SPSS®-tilasto-ohjelman versiolla 9.0. Laadulliset muuttujat on ilmaistu prosentteina ja määrälliset muuttujat keskiarvona ± standardipoikkeama (SD). Kuolemattoman eloonjäämisen, sydänkuolemasta vapaan eloonjäämisen ja tapahtumattoman eloonjäämisen vakuutusmatemaattiset käyrät arvioitiin Kaplan-Meierin menetelmällä. Yksimuuttuja-analyysissä eri kliinisiä, angiografisia ja toimenpidemuuttujia verrattiin sen perusteella, esiintyikö tai puuttuiko merkittäviä haittatapahtumia seurannan lopussa, kvantitatiivisia muuttujia verrattiin Studentin t-testillä ja kvalitatiivisia muuttujia Khiin neliö -testillä. Lisäksi tapahtumattoman eloonjäämisen käyriä verrattiin log-rank-testillä niiden muuttujien osalta, jotka osoittivat taipumusta tapahtumien esittämiseen (PP P
TULOKSET
PERUSTIEDOT
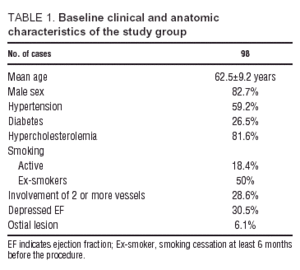
Potilaiden kliiniset ominaisuudet tutkimukseen liittämishetkellä ja sepelvaltimoiden arteriografiassa todetut anatomiset ominaisuudet on esitetty taulukossa 1. Suurin osa potilaista ohjattiin epästabiilin angina pectoriksen vuoksi (87 potilasta epästabiili angina pectoris, 11 potilasta vakaa ponnistus angina pectoris). Kahdellakymmenelläkahdella potilaalla oli kolme tai useampia sydän- ja verisuonitautien riskitekijöitä; heistä 20:llä (91 %) oli verenpainetauti, 19:llä (86 %) diabetes ja 21:llä (95 %) dyslipidemia, kun taas vain 10:llä (55 %) oli aktiivinen tupakointi. Potilaista 71 prosentilla (71 %) oli yksittäinen pAD-leesio, ja 70 prosentilla heistä ei todettu kammion toimintahäiriötä kammiokuvauksessa.
Menetelmä
Menetelmän muuttujat on esitetty taulukossa 2. Seitsemänkymmentäseitsemällä prosentilla (77 %) potilaista pAD:n leesiot olivat lyhyitä, mikä käy ilmi käytettyjen lyhyiden stenttien prosentuaalisesta osuudesta (

Kehitys
Keskimääräinen seuranta-aika oli 38 ± 11 kk, ja se oli lyhyempi kuin 24 kk:n seuranta-aika vain kahdella potilailla, jotka kuolivat potilasta kohden (kahden ja yhdeksän kuukauden kohdalla). Tutkimuksen aikana ei tapahtunut yhtään seurantahäviötä, kuten kuvassa 1 on esitetty graafisesti. Tutkimuksen päättymiseen asti 68 potilaalla (69,4 %) ei ollut angina pectoris -oireita eikä yhtään MACE-tapausta seurannan aikana. Kahdellakymmenelläviidellä potilaalla (25,5 %) oli angina pectoris ja heidät ohjattiin uuteen sepelvaltimotutkimukseen. Seitsemällä potilaalla havaittiin angiografinen restenoosi, mutta uutta perkutaanista tai kirurgista revaskularisaatiomenetelmää ei päätetty tehdä (neljällä potilaalla ei ollut siltoja distaalisiin verisuoniin ja anatomiset vauriot olivat epäsuotuisia uudelle PTCA:lle, ja kolmella muulla potilaalla restenoosin osuus oli alle 70 % ja niiden kliininen hallinta oli riittävää antianginaalisten lääkkeiden avulla). Kahdelletoista potilaalle jouduttiin tekemään uusi kohdeleesion revaskularisaatio: kuudelle tehtiin sepelvaltimoleikkaus ja IMA-bypass 3, 6, 6, 6, 9, 13 ja 14 kuukautta stentin istutuksen jälkeen (yhdelle potilaalle tehtiin leikkaus pAD:n uuden PTCA:n jälkeen varhaisen restenoosin vuoksi 3 kuukauden kuluttua) ja kuudelle potilaalle tehtiin uusi PTCA seurantakuukausien 5 ja 34 välisenä aikana (yhdessä tapauksessa stentti poistettiin sisäisen restenoosin vuoksi). Muut 7 potilasta, joilla oli jatkuva angina pectoris, ohjattiin uuteen revaskularisaatioon PTCA:lla ja stenttiimplantaatioon muissa verisuonissa kuin pAD:ssa, ja heistä 3:lle hoidettiin 2 verisuonta (3 oikean sepelvaltimon revaskularisaatiota, 3 keskimmäisen etummaisen laskevan valtimon revaskularisaatiota ja 4 tylpän marginaalisen valtimon revaskularisaatiota). Kahdella potilaalla oli anteriorinen AMI (toisella hiljainen) 2 ja 4 kuukautta toimenpiteen jälkeen. Koronariografiaa ei tehty myöhemmin, koska testit jäännösiskemian varalta olivat negatiivisia.
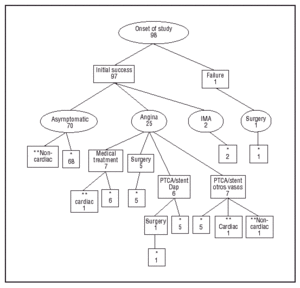
Kuva 1. Kaavio potilaiden kehityksestä (*oireeton tutkimuksen lopussa, **kuolema).
Viisi kuolemantapausta sattui, joista kaksi oli sydänperäisiä 2 ja 38 kuukauden kuluttua tutkimukseen osallistumisesta ja kolme ei-sydänperäisiä (yksi kasvainsairauteen 38 kuukauden kuluttua tutkimukseen osallistumisesta, yksi akuuttiin vatsaonteloon, johon liittyi peräsuoleen kohdistunut verenvuoto 9 kuukauden kuluttua, ja yksi iskeemiseen aivohalvaukseen 24 kuukauden kuluttua).
Kaplan-Meierin testin mukaan todennäköisyys pysyä vapaana MACE:sta oli 83,7 % 60 kuukauden seurannassa (kuva 2), ja kokonaistodennäköisyydet olla sairastumatta sydänperäiseen tai muuhun kuin sydänperäiseen kuolemaan olivat 98 % ja 94,8 % (kuva 3).
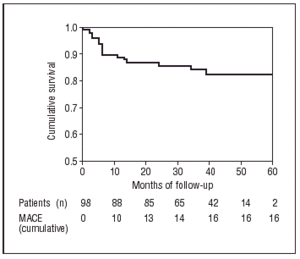
Kuvio 2. Sydänkuolema. Kaplan-Meierin käyrä eloonjäämiselle ilman merkittäviä sydäntapahtumia.
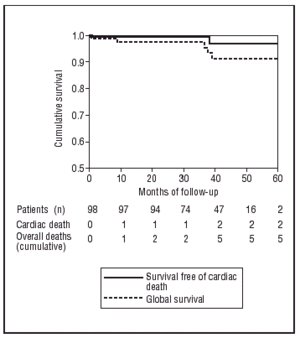
Kuva 3. Kaplan-Meierin käyrät eloonjäämisestä ilman kuolemaa ja ilman sydänperäistä kuolemaa.
Kliiniset, anatomiset ja toimenpidemuuttujat ja niiden yhteys MACE:n mahdolliseen ilmaantumiseen on esitetty taulukossa 3. Univariaattianalyysi osoitti, että kahden stentin käyttö oli yhteydessä suurempaan MACE:n ilmaantuvuuteen (PP=.021) ja AHT-DM-dyslipidemian interaktioon (OR=3,7; 95 % CI, 1,3-10,3; P=.011). Itäiset ahtaumat (OR=3,7; 95 % CI, 0,8-16,6; P=.09) osoittivat suurempaa taipumusta tapahtumien esiintymiseen.
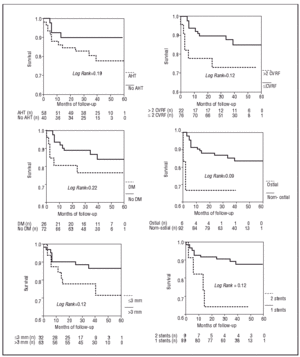
Kuvio 4. MAKE:n yleistyminen. Kaplan-Meierin käyrät eloonjäämisestä ilman merkittäviä sydäntapahtumia eri kliinisten tekijöiden ja toimenpiteen perusteella. CVRF tarkoittaa kardiovaskulaarisia riskitekijöitä.
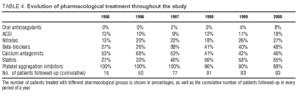
Taulukossa 4 on esitetty potilaiden tutkimuksen aikana saamat farmakologiset hoidot. Verihiutaleiden aggregaation estäjiä (asetyylisalisyylihappoa ja/tai tiklopidiinia) käytettiin usein seurannan aikana kalsiumantagonistien ja beetasalpaajien lisäksi, joita käytti 48 % ja 46 % potilaista tutkimuksen lopussa. Statiinien käyttö lisääntyi huomattavasti, 27 %:sta seurannan alussa 65 %:iin seurannan päättyessä.
KESKUSTELU
Tämän prospektiivisen havainnointitutkimuksen pitkäaikaistulokset (keskimääräinen seuranta-aika 38 kuukautta ja maksimiseuranta-aika enintään 60 kuukautta), joka koski stenttiimplantaatiolla hoidettuja pAD:n proksimaalisen segmentin stenooseja, viittasivat siihen, että toimenpiteen onnistumisprosentti oli korkea (98 %).9 %), alhainen uusien revaskularisaatioiden osuus (12,2 %), suuri todennäköisyys pysyä vapaana MACE:sta (83,7 %) ja alhainen kuolleisuus. On huomattava, että suurella osalla potilaista oli lyhyitä, yhden verisuonen leesioita eikä vasemman kammion toiminta ollut heikentynyt.
Vertailu aiempiin tutkimuksiin
Vaiemmat tutkimukset ovat osoittaneet, että interventiohoito tuottaa enemmän hyötyjä kuin farmakologinen lääkehoito, kun kyseessä on pAD:n vaikea sairaus tai yhden verisuonen sepelvaltimotauti.5,6,6 Kahden tärkeimmän revaskularisaatiotekniikan (PTCA ja IMA-transplantaatti) vertailu paljastaa kuitenkin uusien revaskularisaatioiden suuremman esiintyvyyden PTCA:lla hoidetussa ryhmässä, suuremman antianginaalisten lääkkeiden tarpeen ja huonomman rasituksen sietokyvyn, ja uudelleeninfarktin ja kuolleisuuden määrä on samankaltainen näissä kahdessa ryhmässä.4,7,12-12. Uusien revaskularisaatioiden suurempi esiintyvyys PTCA:n jälkeen johtuu restenoosiilmiöstä, jota esiintyy pääasiassa ensimmäisen vuoden aikana PTCA:n jälkeen.13,14 Restenoosin esiintyvyys eristetyn PTCA:n jälkeen vaihtelee eri sarjoissa 40 prosentista 66 prosenttiin. Restenoosia suosivia tekijöitä ovat muun muassa proksimaaliset vauriot ja laskevan etummaisen sepelvaltimon vaurioituminen.15 Stenttiimplantaation käyttöönotto on selvästi muuttanut näitä tuloksia, sillä se on pienentänyt restenoosin riskin lähes puoleen,9,16-19 ja välittömien komplikaatioiden esiintyvyys on hyvin pieni ja lyhyen ja keskipitkän aikavälin kliininen kehitys on erittäin suotuisa (samankaltainen kuin se, joka on saavutettu IMA-transplantaatilla suoritetun leikkauksen yhteydessä). Aiemmat tutkimukset ovat osoittaneet, että manuaalisesti palloon kiinnitettävien stenttien implantin vikaantumistiheys on 1,5-6,9 % Palmaz-Schatz-stentin osalta ja 1,5-3,1 % NIR-stentin osalta.20,21 Viimeaikaisissa toisen sukupolven stenttejä koskevissa tutkimuksissa, kuten SPORT-NIR-rekisterissä22 , implantin vikaantumisprosentti on ollut vain 0,4 %. Tutkimuksessamme esiintyi vain yksi epäonnistuminen, kun istutettiin Palmaz-Schatz-stentti, joka kiinnitettiin manuaalisesti pallolaajennuspalloon. Tämä 1 %:n epäonnistumisprosentti vastaa aiemmissa tutkimuksissa raportoituja tuloksia.
Restenoosin ja uuden stentin revaskularisaation tarpeen määrä vaihtelee eri tutkimussarjoissa 19 prosentista 31 prosenttiin.10,16,19,23 Tuloksemme vahvistavat, että pAD:n uusia revaskularisaatioita voi tapahtua jopa kahden ja puolen vuoden ajan toimenpiteen jälkeen, vaikka suurin osa uusintatoimenpiteistä tehtiin ensimmäisten kahdentoista kuukauden aikana stentin istutuksen jälkeen (66,6 % tapauksista). PAD:n uusien revaskularisaatioiden esiintyvyys oli 12,2 %, vaikka merkittävän restenoosin todellista esiintyvyyttä ja sen ilmaantumisen nopeutta sarjassamme ei tiedetä, koska emme arvioineet potilaita systemaattisesti angiografian avulla.
Kehityksen ennustetekijät
Analysoiduista tekijöistä ainoastaan kahden stentin käyttö toimenpiteen aikana oli itsenäinen riskitekijä epäsuotuisammalle kliiniselle kehitykselle, mikä on yhteneväinen Bautersin ja muiden ryhmän raportin kanssa24 .
Tekijöitä, jotka perinteisesti viittaavat huonompaan ennusteeseen stenttiimplantaation jälkeen, kuten DM, monisuonitauti, verenpainetauti tai vasemman kammion toimintahäiriö pitkäaikaisseurannassa25 , ei vahvistettu univariaattianalyysissä. DM-potilailla restenoosiilmiön todettiin johtuvan pääasiassa liiallisesta intiman hyperplasiaprosessista verrattuna ei-diabeettisiin potilaisiin26 , joilla tämä prosessi kehittyi vähemmän aggressiivisesti. Ilmiö ilmenee korkeampana restenoosin määränä ja uusien revaskularisaatiotoimenpiteiden tarpeena.27 Tutkimuksemme 23 diabeetikkopotilaasta suurin osa (20 potilasta 23:sta) oli ei-insuliiniriippuvaisia, mikä saattaa selittää sen, miksi DM ei ollut itsenäinen ennuste, sillä viimeaikaiset tutkimukset ovat osoittaneet, että stentin läpäisevyyden kehityksessä on eroja diabetestyypistä riippuen. Ennuste on huonompi insuliiniriippuvaisessa DM:ssä.28,29 Kuitenkin DM:n, AHT:n ja dyslipidemian yhdistelmän todettiin olevan yhteydessä huonompaan kliiniseen kehitykseen monimuuttuja-analyysissä. Tämä osoitti, että vaikka näillä tekijöillä ei ollut yksittäin selkeää yhteyttä ennusteeseen (ainakaan tässä tutkitun kokoisissa näytteissä), tekijöiden yhteisesiintymistä potilaassa on pidettävä vähemmän suotuisan kehityksen ennusteena, kuten ateroskleroottisessa taudissa yleensä.
Lääkkeiden käyttö oli runsasta koko seurannan ajan, mikä johtui pohjimmiltaan perinteisten sydän- ja verisuonitautien riskitekijöiden, kuten hyperkolesterolemian ja AHT:n, suuresta esiintyvyydestä tutkimuspopulaatiossa, ja monisuonisairaudesta, joka ilmeni mukaanottohetkellä (31 %) ja evoluution aikana (seitsemällä potilaalla todettiin sepelvaltimotaudin eteneminen, joka vaati muiden verisuonten revaskularisaatiota).
Kliiniset vaikutukset
Tutkimuksemme tulokset vahvistavat stenttiimplantaation turvallisuuden leesioissa, joihin liittyy pAD, ja hyvän kliinisen pitkäaikaisvasteen, joka joillakin potilailla saavutti 5 vuoden seuranta-ajan. Eloonjäämisestä ja MACE:n puuttumisesta saadut luvut vastaavat aiempia tutkimuksia stentti-implantaatiosta pAD:n yhteydessä30 ja ovat vertailukelpoisia niiden lukujen kanssa, jotka on raportoitu muissa tutkimuksissa, joissa suoritettiin sepelvaltimoiden revaskularisaatio IMA-transplantaatiokirurgian avulla7,31.
Kliinisessä käytännössä8,32 päätös valita IMA-ohitusleikkaus PTCA:n ja stentti-implantoinnin sijasta on tehtävä yksilöllisesti kunkin potilaan kohdalla ottaen huomioon potilaan mielipide sen jälkeen, kun hän on saanut tietoa molemmista hoitovaihtoehdoista, niiden tuloksista ja riskeistä, ja pitäen perkutaanista vaihtoehtoa ensimmäisenä valintana tapauksissa, joissa sepelvaltimoiden anatomia on suotuisa, ja potilailla, joilla tulevien revaskularisaatiohoitojen tarve on ennakoitavissa (esim, nuoret potilaat).
Tutkimuksen rajoitukset
Tutkimuksen tärkein rajoitus oli satunnaistamisen puuttuminen, mikä esti suoran vertailevan analyysin muiden revaskularisaatiostrategioiden kanssa. Koska sepelvaltimoiden arteriografiaa ei tehty systemaattisesti seurannan aikana, emme voi määrittää angiografisen restenoosin todellista määrää tutkimusryhmässä. Käytetty tekniikka oli voimassa vuodesta 1995 lähtien. Uusien materiaalien ja mallien käyttö myöhemmän sukupolven stenteissä sekä uudet antiaggregaatiohoidot, joissa käytetään verihiutaleiden IIb-IIIa-reseptorien antagonisteja, parantavat lyhyen ja pitkän aikavälin tuloksia. Tutkimuksessamme näillä aineilla saadut tulokset eivät kuitenkaan näytä tukevan niiden yleistä käyttöä stenttiimplantaatiossa niiden korkean kustannus-hyötysuhteen vuoksi.
YHTEENVETO
Etummaisen laskevan sepelvaltimon proksimaalisen segmentin ahtauman hoito stenttiimplantaatiolla on turvallista potilailla, joiden sepelvaltimoiden anatomia on suotuisa tähän toimenpiteeseen. Komplikaatioiden osuus on alhainen, ja pitkäaikaisessa seurannassa, joka joissakin tapauksissa tutkimuksessamme on 5 vuotta, siihen liittyy uusien revaskularisaatiotoimenpiteiden vähäinen esiintyvyys ja korkea eloonjäämisprosentti.
TAKAISIN KIITOKSET
Haluaisimme ilmaista vilpittömät kiitoksemme tohtoreille tri. V. Climentille ja J. Sánchezille Alicanten yleisen yliopistollisen sairaalan (Hospital General Universitario of Alicante) kardiologian ja ennaltaehkäisevän lääketieteen osastoilta heidän tuestaan ja ohjauksestaan tämän artikkelin kehittämisessä.