Lei da Decadência Radioativa
Quando um núcleo individual se transforma em outro com a emissão de radiação, diz-se que o núcleo se decompõe. O decaimento radioativo ocorre para todos os núcleos com \(Z > 82\), e também para alguns isótopos instáveis com \(Z < 83\). A taxa de decaimento é proporcional ao número de núcleos N originais (não decaídos) em uma substância. O número de núcleos perdidos por decaimento, { -dN} no intervalo de tempo dt, é escrito
>
onde {lambda} é chamado de constante de decaimento. (O sinal de menos indica que o número de núcleos originais diminui com o tempo.) Em outras palavras, quanto mais núcleos disponíveis para decair, mais decairão (no tempo dt). A equação \ref{eq2} pode ser reescrita como
Integrando ambos os lados da equação, e definindo \eq2} para ser o número de núcleos em \e(t = 0\eq2), obtemos
>
>
>
>
>Traçando os lados esquerdo e direito da Equação {eq4} como um poder de {eq4}, temos a lei da decadência radioactiva.
Lei de decaimento radioactivo
O número total de núcleos radioactivos que restam após o tempo é
>
>
> onde {\i1}o Lambda}é a constante de decaimento para o núcleo particular.
O número total de núcleos cai muito rapidamente no início, e depois mais lentamente (Figura \PageIndex{2}}).
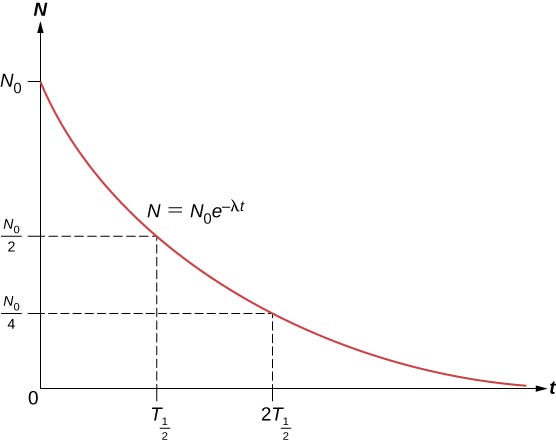
A meia-vida \\((T_{1/2})\) de uma substância radioativa é definida como o tempo para metade dos núcleos originais decairem (ou o tempo em que metade dos núcleos originais permanecem). As meias-vidas de isótopos instáveis são mostradas no gráfico de nuclídeos. O número de núcleos radioativos restantes após um número inteiro (n) de meias-vidas é portanto
Se a constante de decaimento \((\lambda)\) é grande, a meia-vida é pequena, e vice versa. Para determinar a relação entre essas quantidades, note que quando \(t = T_{1/2}}), então \(N = N_0/2\).
Assim, a Equação {eq5} pode ser reescrita como
>
Dividindo ambos os lados por \\(N_0\) e tomando os rendimentos naturais do logaritmo
>
que se reduz a
>
>
>Thus, se conhecemos a meia-vida T1/2 de uma substância radioactiva, podemos encontrar a sua decomposição constante. A vida útil de uma substância radioativa é definida como a quantidade média de tempo que um núcleo existe antes de se decompor. A vida útil de uma substância é apenas a recíproca da constante de decaimento, escrita como
> A atividade A é definida como a magnitude da taxa de decaimento, ou
>
> A infinitesimal mudança dN no intervalo de tempo dt é negativa porque o número de partículas pai (não decaídas) está diminuindo, então a atividade (A) é positiva. Definindo a atividade inicial como \(A_0 = \lambda N_0\), temos
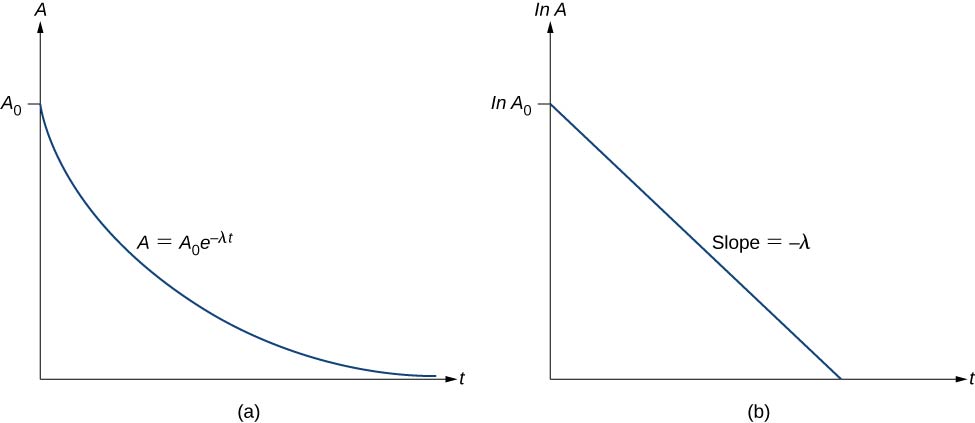
Assim, a atividade A de uma substância radioativa diminui exponencialmente com o tempo (Figura \PageIndex{3}}).
Exemplo \(\PageIndex{1}}}(PageIndex{1}): Constante de decaimento e atividade do estrôncio-90
A meia-vida do estrôncio-90, \(\ce{_{{38}^{90}Sr}}, é 28,8 y. Encontrar (a) sua constante de decaimento e (b) a atividade inicial de 1,00 g do material.
Estratégia
Nós podemos encontrar a constante de decaimento diretamente da Equação \ref{eq8}. Para determinar a atividade, precisamos primeiro encontrar o número de núcleos presentes.
Solução
a. A constante de decaimento é encontrada
\
b. A massa atômica de \(_{38}^{90}Sr\) é 89,91 g. Usando o número Avogadro \(N_A = 6,022 {23}) átomos/mol, encontramos o número inicial de núcleos em 1,00 g do material:
>
>
Deste, descobrimos que a atividade \(A_0\) em \(t = 0\) para 1.00 g de estrôncio-90 é
>
Expressão \\(lambda) em termos da meia-vida da substância, obtemos
>
>
Por isso, a atividade é reduzida pela metade após uma meia-vida. Podemos determinar a constante de decomposição medindo a actividade em função do tempo. Tomando o logaritmo natural dos lados esquerdo e direito da equação {eq11}, obtemos
>
Esta equação segue a forma linear \(y = mx + b\). Se traçarmos a linha A versus t, esperamos uma linha reta com inclinação (-lambda) e y-intercepção (A_0, A_0) (Figura 3b)). A atividade A é expressa em unidades de Becquerels (Bq), onde uma (1, Bq = 1, decadência, por segundo). Esta quantidade também pode ser expressa em decadências por minuto ou decadências por ano. Uma das unidades mais comuns para atividade é a curie (Ci), definida como sendo a atividade de 1 g de Ra. A relação entre o Bq e a Ci é
Exemplo ^(^PageIndex{2}}): O que é a actividade no tecido vivo? 549> 469> Aproximadamente 20 por cento do corpo humano em massa é carbono. Calcule a actividade devida a 1,00 kg de carbono encontrado em um organismo vivo. Expressar a atividade em unidades de Bq e Ci.
Estratégia
A atividade de ^(14}C}) é determinada usando a equação ^(A_0 = ^lambda N_0}), onde λ é a constante de decaimento e ^(N_0}) é o número de núcleos radioativos. O número de núcleos em uma amostra de 1,00 kg é determinado em duas etapas. Primeiro, determinamos o número de núcleos usando o conceito de uma toupeira. Segundo, multiplicamos este valor por 1,3 vezes 10 (a abundância conhecida de 14 C numa amostra de carbono de um organismo vivo) para determinar o número de núcleos de um organismo vivo. A constante de decomposição é determinada a partir da meia-vida conhecida de ^(^{14}C}) (disponível em ).
Solução
Um sinal de carbono tem uma massa de 12,0 g, uma vez que é quase puro ^(^{12}C}). Assim, o número de núcleos de carbono em um quilograma é
> O número de núcleos ^(^{14}C}) em 1 kg de carbono é portanto
>
>
>
>Agora podemos encontrar a atividade ^(A) usando a Equação ^ref{eq11}. A entrada de valores conhecidos nos dá
ou \\(7,89 ^9^^ vezes 10^9^) decai por ano. Para converter isto para a unidade Bq, nós simplesmente convertemos anos em segundos. Assim,
>
ou 250 decaimentos por segundo. Para expressar A em curies, usamos a definição de uma curie,
>
>Assim,
>
>
>
Significado,
>
Apeso aproximado do corpo humano por peso é carbono. Centenas de decomposições acontecem no corpo humano a cada segundo. O carbono 14 e outras substâncias radioativas naturais do corpo compõem a exposição de fundo de uma pessoa à radiação nuclear. Como veremos mais adiante neste capítulo, este nível de atividade está bem abaixo das doses máximas recomendadas.