Lipofilicidade é possivelmente a propriedade físico-química mais importante de um medicamento potencial, desempenha um papel na solubilidade, absorção, penetração da membrana, ligação da proteína plasmática, distribuição, penetração do SNC e divisão em outros tecidos ou órgãos como o fígado e tem um impacto sobre as vias de liberação. É importante no reconhecimento ligand, não só para a proteína alvo mas também para as interacções CYP450, ligação HERG, e indução enzimática mediada PXR.
LogP é um componente da Regra de Lipinski de 5 uma regra de ouro para prever a solubilidade e permeabilidade que se tornou um substituto para a semelhança com o fármaco.
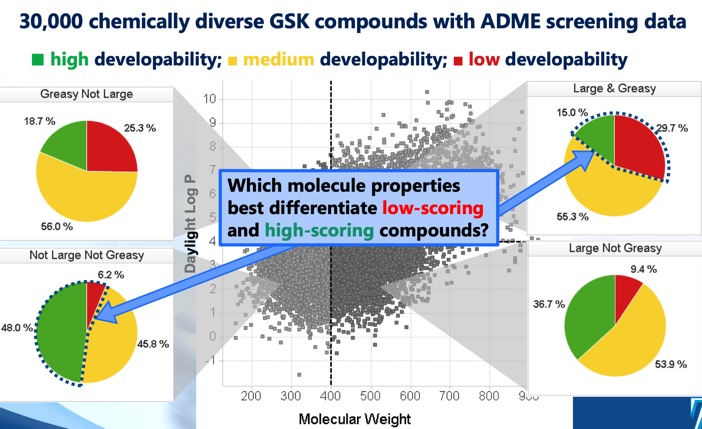
O escore de desenvolvimento DOI identifica quatro regiões distintas do cLog P/peso molecular que definem o espaço químico ótimo e sub-ótimo, e um escore de desenvolvimento derivado de modelos de regressão usando solubilidade, permeabilidade, ligação protéica e dados de triagem de inibição 3A4. Enquanto o setor MWt <400, cLogP <4 sugeria a maior chance de sucesso, notou-se que mesmo o setor MWt >400, cLogP >4 incluía algumas moléculas desenvolvíveis, embora com uma chance muito menor de sucesso.
A medida mais comumente usada de lipofilicidade é LogP, este é o coeficiente de partição de uma molécula entre uma fase aquosa e lipofílica, geralmente octanol e água.
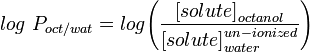
A medida do LogP pode ser realizada de várias maneiras, a mais comum é o método shake-flask, que consiste em dissolver parte do soluto em questão num volume de octanol e água, agitando por um período de tempo, e depois medir a concentração do soluto em cada solvente. Isto pode ser demorado, particularmente se não houver um método espectroscópico rápido para medir a concentração da molécula nas fases. Um método mais rápido de determinação de log P faz uso de cromatografia líquida de alto desempenho. O log P de um soluto pode ser determinado correlacionando seu tempo de retenção com compostos similares com o valor log P conhecido doi.
Cálculo de lipofilicidade
Usualmente não é prático determinar experimentalmente o LogP de cada composto feito (e pode ser de interesse calcular o logP antes da síntese) e assim os resultados calculados são usados, há uma série de ferramentas de software disponíveis tanto no desktop como online (não use para compostos confidenciais).
Muitas destas aplicações funcionam usando um grande conjunto de dados de treinamento de valores conhecidos para determinar contribuições de fragmentos para sub-estruturas e grupos funcionais, porém o logP não é uma simples propriedade aditiva e termos de correção são necessários para permitir efeitos de proximidade, H-bonding, efeitos eletrônicos, etc. como mostrado nos exemplos abaixo.
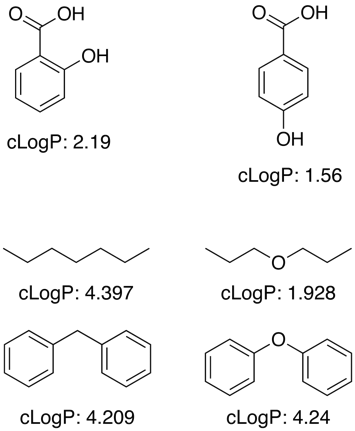
Para grupos funcionais desconhecidos os programas freqüentemente se aproximam usando contribuições de átomos individuais.
As diferentes metodologias para calcular logP podem ser divididas em três abordagens diferentes.
Atómico (por exemplo “AlogP”, ) &Aumento Atômico / Híbrido (“XlogP”, “SlogP”)
Fragmento (“ClogP”, KlogP, ACD/logP)
Métodos baseados em propriedade (“MlogP”, “VlogP”, “MClogP”, “TlogP”)
Atomic logP considera que cada átomo tem uma contribuição para o logP, e que as contribuições para o valor final são puramente aditivas. No entanto é claro que um nitrogênio em um amido é diferente de um nitrogênio em uma amina ou piridina, o Enhanced Atomic leva em conta o tipo de átomo.
Métodos de fragmentos usam um grande conjunto de dados de treinamento de valores conhecidos para determinar contribuições de fragmentos para subestruturas e grupos funcionais, juntamente com termos de correção para levar em conta os efeitos de proximidade. Estes métodos freqüentemente se baseiam em modelos atômicos para novos grupos funcionais.
Os métodos baseados em propriedade tendem a ser computacionalmente exigentes e não realmente adequados para testar grandes conjuntos de dados.
Porque os conjuntos de treinamento e os algoritmos variam entre aplicações é muito importante não combinar resultados calculados usando ferramentas diferentes.
Algumas das ferramentas permitem ao usuário estender o conjunto de treinamento usando valores medidos em casa, isto pode ser crítico ao explorar novos grupos funcionais ou andaimes.
LogD
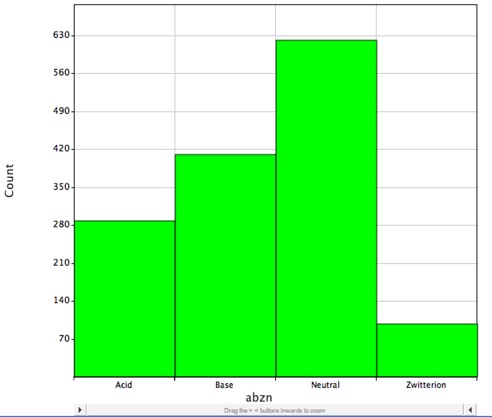
No entanto, a maioria das drogas conhecidas contém grupos ionizáveis, como mostrado no histograma abaixo, isto mostra a distribuição de pequenas moléculas de drogas com DrugBank e é provável que sejam carregadas a pH fisiológico e LogP apenas descreve corretamente o coeficiente de partição de moléculas neutras (não carregadas).
LogD a constante de distribuição é um melhor descritor da lipofilicidade de uma molécula. Isto pode ser determinado de forma semelhante ao LogP mas em vez de utilizar água, a fase aquosa é ajustada a um pH específico utilizando um tampão. O log D é assim dependente do pH, portanto é necessário especificar o pH no qual o log D foi medido. De particular interesse é o log D a pH = 7,4 (o pH fisiológico do soro sanguíneo).
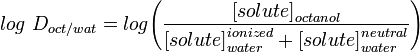
Aplicações como Marvin permitem ao usuário calcular o logD mas também exibir o perfil de distribuição do pH, como mostrado abaixo para Warfarin.
Para compostos com um pKa próximo ao pH fisiológico pode ser crítico considerar qual pode ser a forma ionizada predominante.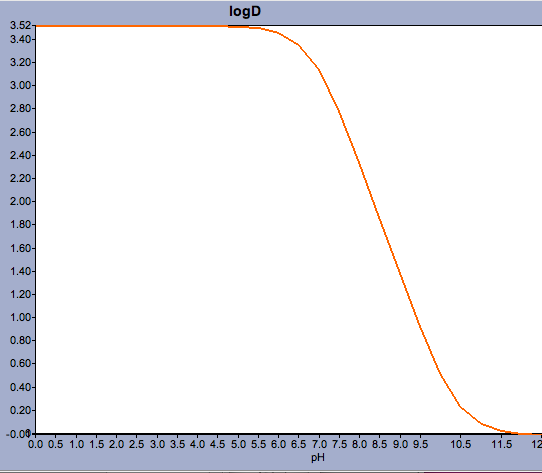
Isto também pode ser valioso quando se pensa na absorção das diferentes regiões do canal alimentar onde o pH varia de 1-3 no estômago a 7-8 no íleo.
As contribuições de vários grupos funcionais para LogD foram exploradas “Contribuições LogD de substitutos comumente usados na química medicinal” DOI, este estudo utilizou a análise de pares moleculares pareados de valores experimentais de LogD de vários milhares de compostos coletados usando o método shake-flask a pH = 7,4. Eles relataram a diferença média do deltaLogD para determinados pares moleculares e os resultados são mostrados abaixo para o caso em que o grupo funcional está em qualquer posição no anel fenil. Também incluí o LogD calculado usando o software Chemaxon.
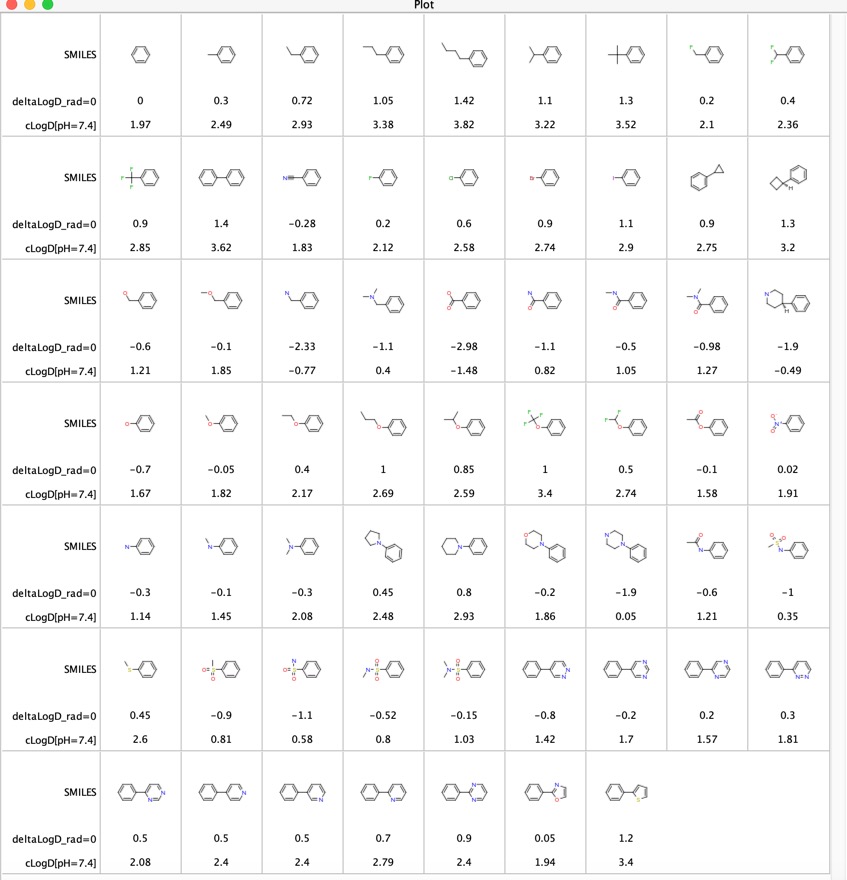
Esta é uma tabela útil para comparar grupos funcionais, em particular as últimas 11 entradas comparam a influência de vários heterócitos no LogD. Estes heterócitos são frequentemente usados como substitutos bioistéricos para um anel fenil.
Pensei que poderia ser interessante comparar as diferenças LogD determinadas usando os pares moleculares combinados (deltaLogD_rad=0) com os valores determinados usando o Chemaxon calculado LogD (deltacLogD). Como você pode ver abaixo há uma correspondência muito boa.
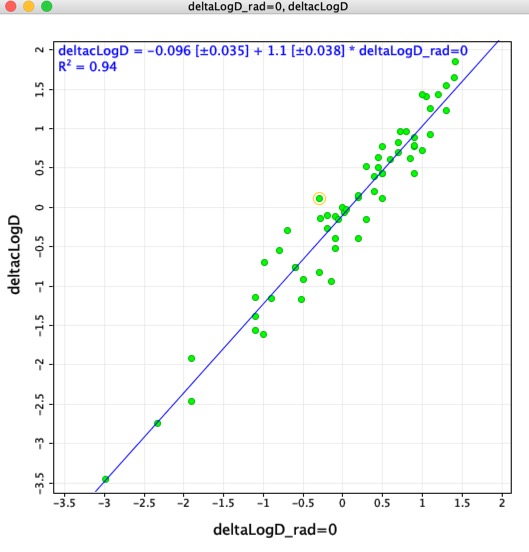
Remember Como os conjuntos de treinamento e os algoritmos variam entre aplicações é muito importante não combinar resultados calculados usando ferramentas diferentes.
É importante ser circunspecto que qualquer melhoria na afinidade de ligação não é inteiramente impulsionada por um aumento no LogD, muitas vezes é útil simplesmente plotar afinidade de ligação versus LogD. As modificações compostas mais interessantes não são necessariamente aquelas que dão o maior aumento na afinidade, mas podem ser aquelas que dão um aumento na afinidade sem um aumento correspondente na lipofilicidade. Olhando para a tabela abaixo há um número muito elevado de compostos de afinidade.
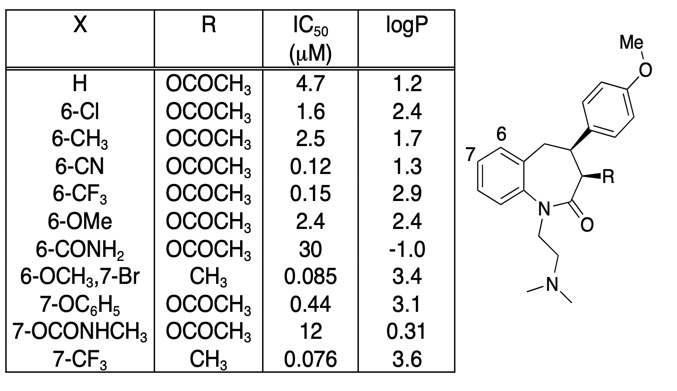
No entanto, se plotarmos IC50 versus LogP como mostrado abaixo há uma correlação muito clara entre LogP e IC50, no entanto um composto é claramente diferente. O substituto 6-CN dá um aumento na afinidade sem um aumento correspondente no LogP.
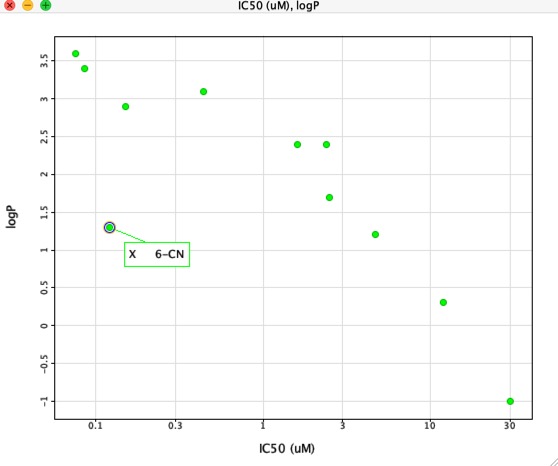
Lipofilicidade também é um componente importante muitas das responsabilidades fora do alvo, incluindo a ligação da proteína plasmática (especialmente albumina), HERG, interações CYP, Transportadores, têm fortes correlações com lipofilicidade, e tem havido uma série de estudos ligando logP elevado à probabilidade de compostos falharem no desenvolvimento como resultado de fracas características ADMET (absorção, distribuição, metabolismo, excreção e toxicidade). Em contraste, é claro que muitas vezes é necessário um certo tamanho e lipofilicidade para atingir níveis razoáveis de afinidade. O equilíbrio destes requisitos é um desafio chave na descoberta de medicamentos e a sugestão é que os químicos visem o sweet spot MWt 250-500 e LogP 2-4. Uma consequência desta abordagem é a necessidade de priorizar o baixo peso molecular, menos compostos lipofílicos da triagem. O foco inicial da química medicinal deve ser a seleção de pontos de partida de boa qualidade e, em seguida, controlar eficazmente as mudanças nas propriedades físico-químicas durante o processo de otimização.
Leitura do valor
De olho no ponto doce: o papel da natureza e da nutrição na química medicinal DOI
Eficiência lipofílica: a métrica de eficiência mais importante na química medicinal DOI
Última atualização 12 de janeiro de 2019