Cancer é o resultado da quebra dos controles que regulam as células. As causas da decomposição incluem sempre alterações em genes importantes. Estas alterações são frequentemente o resultado de mutações, alterações na sequência de ADN dos cromossomas. Mutações podem ser mudanças muito pequenas, afetando apenas alguns nucleotídeos ou podem ser muito grandes, levando a grandes mudanças na estrutura dos cromossomos.
Tantas pequenas e grandes mutações podem afetar o comportamento das células. Combinações de mutações em genes importantes podem levar ao desenvolvimento do câncer. O material abordado nesta página descreve a relação entre mutação e câncer, os diferentes tipos de mutações e o que as causa. Mais informação sobre os tópicos desta página também pode ser encontrada na maioria dos livros de introdução à Biologia, recomendamos Campbell Biology, 11ª edição.1
Topics nesta página:
- Mutação e cancro
- Mutações e cancro
- Tipos de mutação
- Mutações de pontos
- Translocações
- Amplificação de genes
- Inversões, Eliminações, e Duplicações
- Aneuploidia
- Mudanças Epigenéticas
- Causas de Mutação
- Resumo da Mutação
- Saber o Fluxo: Mutação
Mutação e câncer
Os comportamentos anormais demonstrados pelas células cancerígenas são o resultado de uma série de mutações nos principais genes reguladores. As células tornam-se progressivamente mais anormais à medida que mais genes se tornam danificados. Muitas vezes, os genes que estão no controle da reparação do DNA tornam-se danificados, tornando as células ainda mais suscetíveis a níveis sempre crescentes de caos genético.
Below é uma animação que demonstra a relação entre cromossomos, genes e DNA.
Pensa-se que a maioria dos cancros surgem de uma única célula precursora mutante. Como essa célula se divide, as células ‘filhas’ resultantes podem adquirir diferentes mutações e diferentes comportamentos ao longo de um período de tempo. Aquelas células que ganham uma vantagem na divisão ou resistência à morte celular tenderão a tomar conta da população. Desta forma, as células tumorais são capazes de ganhar uma ampla gama de capacidades que normalmente não são vistas na versão saudável do tipo de célula representada. As mudanças de comportamento observadas nas células cancerígenas são o foco da seção de Biologia do Câncer do site.
Mutações nos principais genes reguladores (supressores tumorais e proto-oncógenos) alteram o comportamento das células e podem potencialmente levar ao crescimento não regulado observado no câncer.
Para quase todos os tipos de câncer estudados até o momento, parece que a transição de uma célula normal e saudável para uma célula cancerígena é uma progressão gradual que requer muitas mudanças genéticas que se somam para criar a célula cancerígena. Estas mutações ocorrem tanto em oncogenes como em supressores tumorais. Esta é uma das razões pelas quais o câncer é muito mais prevalente em indivíduos mais velhos. Para gerar uma célula cancerígena, uma série de mutações deve ocorrer na mesma célula. Uma vez que a probabilidade de qualquer gene sofrer mutações é muito baixa, é muito improvável que várias mutações diferentes ocorram na mesma célula. Por esta razão, as células de um corpo de 70 anos de idade tiveram mais tempo para acumular as mudanças necessárias para formar células cancerígenas, mas as de uma criança têm muito menos probabilidade de ter adquirido as mudanças genéticas necessárias. É claro que algumas crianças têm cancro, mas é muito mais comum em indivíduos mais velhos. O gráfico abaixo mostra as taxas de câncer de cólon nos Estados Unidos em função da idade. O gráfico foi obtido do Instituto Nacional do Câncer. 2
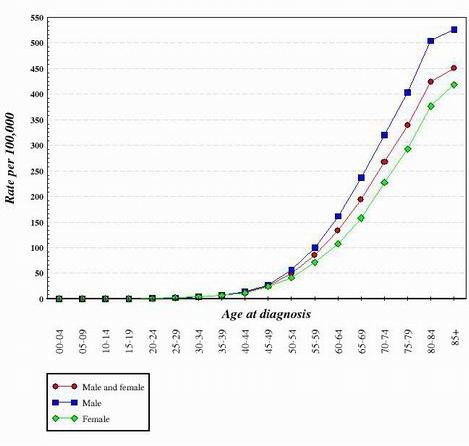
Ao observar a forma das curvas como as mostradas acima, concluiu-se que são necessárias várias alterações genéticas para criar células que se tornam cancerosas.
No laboratório, os pesquisadores têm tentado criar células tumorais, alterando ou introduzindo proteínas regulatórias chave. Vários estudos têm tentado definir o número mínimo de alterações genéticas necessárias para criar uma célula cancerosa, com resultados intrigantes.3
Na natureza, as mutações podem acumular-se nas células ao longo do tempo e se o grupo ‘certo’ de genes for mutado, pode resultar cancro. Um estudo realizado em 2012 mostrou que as células-tronco da medula óssea em um indivíduo saudável acumulam muitas mutações à medida que a pessoa envelhece. Apenas mais algumas alterações nos genes-chave podem causar câncer. Os resultados implicam que células ‘normais’ e células cancerígenas podem não ser tão diferentes em muitos casos.4
Mutações hereditárias no cancro
Para complicar as coisas, é claro que as mudanças necessárias para criar uma célula cancerígena podem ser realizadas de muitas maneiras diferentes. Embora todos os cancros tenham que superar o mesmo espectro de funções reguladoras para crescer e progredir, os genes envolvidos podem ser diferentes. Além disso, a ordem em que os genes se desregulamentam ou se perdem também pode variar. Como exemplo, os tumores do câncer de cólon de dois indivíduos diferentes podem envolver conjuntos muito diferentes de supressores tumorais e oncogenes, mesmo que o resultado (câncer) seja o mesmo.
A grande heterogeneidade observada no câncer, mesmo os do mesmo órgão, significa que o diagnóstico e o tratamento são complicados. Os avanços atuais na classificação molecular dos tumores devem permitir o desenho racional dos protocolos de tratamento com base nos genes reais envolvidos em um determinado caso. Novos testes diagnósticos podem envolver o rastreamento de centenas ou milhares de genes para criar um perfil personalizado do tumor em um indivíduo. Esta informação deve permitir a personalização dos tratamentos de câncer orientados para o indivíduo. Para mais informações sobre isto, consulte a secção Genómica/Proteómica.
As alterações genéticas que levam a um crescimento celular não regulado podem ser adquiridas de duas formas diferentes. É possível que a mutação possa ocorrer gradualmente ao longo de vários anos, levando ao desenvolvimento de um caso ‘esporádico’ de cancro. Alternativamente, é possível herdar genes disfuncionais que levam ao desenvolvimento de uma forma familiar de um determinado tipo de câncer. Alguns exemplos de cancros com componentes hereditários conhecidos incluem:
- Cancro da mama – A herança de versões mutantes dos genes BRCA1 e BRCA2 são factores de risco conhecidos. Embora muitos, se não a maioria, dos indivíduos com câncer de mama não tenham alterações detectáveis nesses genes, ter uma forma mutante aumenta a probabilidade de desenvolver câncer de mama.
- Câncer de cólon – Sabe-se que os defeitos nos genes reparadores do DNA, como o MSH2, predispõem os indivíduos ao câncer colorretal hereditário não-polipose (HNPCC).
- Retinoblastoma – Sabe-se que os defeitos no gene supressor do tumor Rb causam este câncer ocular e vários outros tipos de cânceres. Mais sobre esta doença específica pode ser encontrada na seção sobre Rb
Esta é uma lista incompleta dos tipos de câncer hereditário conhecidos, e é certo que mais formas hereditárias de câncer serão identificadas como a genética de vários tipos de câncer são esclarecidas.
Mais informações sobre este tópico podem ser encontradas nos Capítulos 2 e 4 de A Biologia do Câncer de Robert A. Weinberg.
Tipos de Mutação
O processo pelo qual as proteínas são feitas, tradução, é baseado na ‘leitura’ do mRNA que foi produzido através do processo de transcrição. Qualquer alteração no DNA que codifica um gene levará a uma alteração do mRNA produzido. Por sua vez, o mRNA alterado pode levar à produção de uma proteína que não funciona mais adequadamente. Mesmo a alteração de um único nucleotídeo ao longo do DNA de um gene pode levar a uma proteína completamente não funcional.
Existem várias formas diferentes de alterar o DNA. A seção seguinte descreve os diferentes tipos de alteração genética com mais detalhes.
Mutações pontuais
Alterações genéticas podem ser colocadas em duas categorias gerais. A primeira categoria é composta de alterações que alteram apenas um ou poucos nucleotídeos ao longo de uma cadeia de DNA. Estes tipos de alterações são denominadas mutações pontuais.
Quando os ribossomos lêem uma molécula de RNA mensageiro, cada três nucleotídeos é interpretado como um aminoácido. Estes três códigos de letra são chamados de códons. Para fazer uma analogia com uma frase em inglês: ‘The fat cat eat the rat’ conteria 6 códons. As mudanças causadas pela mutação podem levar a coisas como “O morcego gordo comeu o rato” ou “O fa” ou “O oca gordo comeu o rato… O impacto na proteína depende de onde a mudança ocorre e do tipo de mudança.
Os códões de três letras lidos pelos ribossomos podem ser alterados por mutação de uma de três maneiras:
Mutações sem sentido
O novo códão faz com que a proteína termine prematuramente, produzindo uma proteína que é encurtada e muitas vezes não funciona correctamente ou não funciona de todo.
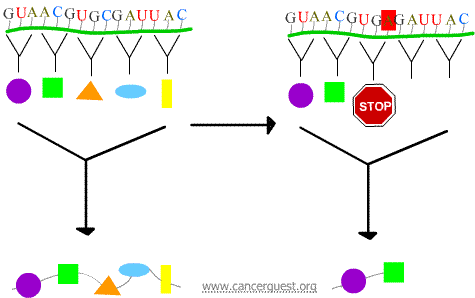
Mutações absurdas
O novo códão faz com que um aminoácido incorreto seja inserido na proteína. Os efeitos na função da proteína dependem do que é inserido no lugar do aminoácido normal.

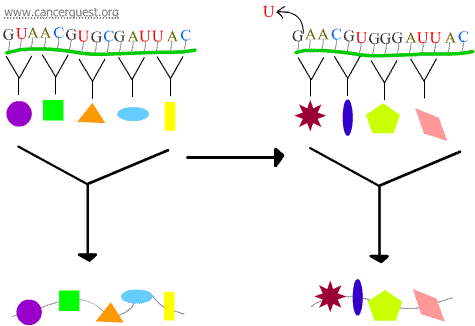
Mutações do feixe
A perda ou ganho de 1 ou 2 nucleotídeos faz com que o códão afectado e todos os códões que se seguem sejam mal lidos. Isto leva a um produto proteico muito diferente e frequentemente não funcional.
>
>
Erros de transcrição
Alguns danos no ADN resultam num nucleótido modificado ou num pequeno grupo de nucleótidos que não pode ser “lido” pela RNA polimerase. Quando o complexo de RNA polimerase chega a estes pontos, eles por vezes contornam os danos adicionando nucleotídeos num esforço para continuar, mesmo que isso signifique colocar a coisa errada. Este processo é conhecido como mutagênese transcripcional e pode desempenhar um papel significativo no desenvolvimento do câncer.5
Translocações
Uma outra categoria de mutações envolve alterações de maiores quantidades de DNA, muitas vezes ao nível do cromossomo. Estas são chamadas translocações e envolvem a quebra e o movimento de fragmentos cromossômicos. Muitas vezes, quebras em dois cromossomos diferentes permitem a formação de dois cromossomos ‘novos’, com novas combinações de genes.
Embora possa parecer que isso não causaria muitos problemas, uma vez que todos os genes ainda estão presentes, o processo pode levar ao crescimento desregulado de células de várias maneiras-
1. Os genes podem não ser transcritos e traduzidos apropriadamente em sua nova localização.
2. O movimento de um gene pode levar a um aumento ou diminuição do seu nível de transcrição.
3. A quebra e reentrada também pode ocorrer dentro de um gene (como mostrado em verde acima), levando à sua inativação.
Para alguns cânceres, translocações particulares são muito comuns e podem até ser usadas no diagnóstico da doença. As translocações são comuns em leucemias e linfomas e têm sido menos comumente identificadas em cancros de tecidos sólidos. Um exemplo seria uma troca entre os cromossomos 9 e 22 observada em mais de 90% dos pacientes com leucemia mielóide crônica (LMC). A troca leva à formação de uma forma abreviada do cromossomo 22 chamado cromossomo Filadélfia (após a localização da sua descoberta). Esta translocação leva à formação de um oncogene do abl proto-oncogene.67
Outros cancros que estão frequentemente (ou sempre) associados a translocações particulares incluem o linfoma de Burkitt, linfomas de células B e vários tipos de leucemia.
Amplificação Genética
Neste processo muito incomum, o processo normal de replicação do DNA é seriamente defeituoso. O resultado é que ao invés de se fazer uma única cópia de uma região de um cromossomo, muitas cópias são produzidas. Isto leva à produção de muitas cópias dos genes que estão localizados naquela região do cromossoma. Algumas vezes, tantas cópias da região amplificada são produzidas que elas podem realmente formar seus próprios pequenos pseudo-cromossomos chamados cromossomos de dois minutos.
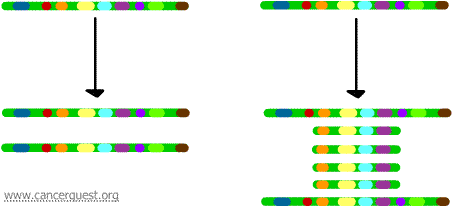
Os genes em cada uma das cópias podem ser transcritos e traduzidos, levando a uma superprodução do mRNA e proteína correspondente aos genes amplificados como mostrado abaixo. As linhas quadrangulares representam o mRNA sendo produzido através da transcrição de cada cópia do gene.
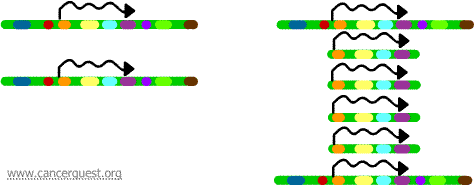
Embora este processo não seja visto em células normais, ele ocorre com bastante frequência em células cancerígenas. Se um oncogene é incluído na região amplificada, então a superexpressão resultante desse gene pode levar ao crescimento desregulado das células. Exemplos disto incluem a amplificação do oncogene myc em uma ampla gama de tumores e a amplificação do ErbB-2 ou HER-2/neu oncogene em cânceres de mama e ovários. No caso do HER-2/ oncogene pneumático, os tratamentos clínicos foram desenhados para atingir células exageradamente expressoras do produto protéico.
A amplificação do gene também contribui para um dos maiores problemas no tratamento do câncer: a resistência aos medicamentos. Os tumores resistentes aos medicamentos podem continuar a crescer e a espalhar-se, mesmo na presença de medicamentos de quimioterapia. Um gene comumente envolvido é chamado MDR para resistência a múltiplos fármacos. O produto protéico deste gene actua como uma bomba localizada na membrana das células. É capaz de ejetar seletivamente moléculas da célula, incluindo drogas quimioterápicas. Esta remoção torna os medicamentos ineficazes.
Isto é discutido mais detalhadamente na secção sobre resistência aos medicamentos. A amplificação de diferentes genes pode tornar ineficazes outros medicamentos de quimioterapia.
Inversões, Duplicações e Eliminações
Inversões
Nestas alterações, segmentos de ADN são libertados a partir de um cromossoma e depois reintroduzidos na orientação oposta. Como nos exemplos anteriores, este rearranjo pode levar a uma expressão genética anormal, quer activando um oncogene ou desactivando um gene supressor do tumor.
Duplicações/Deleções
Por meio de erros de replicação, um gene ou grupo de genes pode ser copiado mais de uma vez dentro de um cromossoma. Isto é diferente da amplificação de genes, pois os genes não são replicados fora do cromossoma e só são copiados uma vez a mais, não centenas ou milhares de vezes. Os genes também podem ser perdidos devido a falha no processo de replicação ou outros danos genéticos.
 >
>
Aneuploidia
Aneuploidia é a mudança genética que envolve a perda ou ganho de cromossomas inteiros. Devido a problemas no processo de divisão celular, os cromossomas replicados podem não se separar com precisão nas células filhas. Isto pode resultar em células que têm muitos cromossomas ou poucos cromossomas. Um exemplo de uma condição aneuploide bastante comum não relacionada ao câncer é a síndrome de Down, na qual há uma cópia extra do cromossomo 21 em todas as células do indivíduo afetado.
Na animação abaixo, são feitas cópias de dois cromossomos, mas quando a célula divide os cromossomos não são distribuídos uniformemente para as duas células que se formam (células filhas). O resultado é que uma das células tem demasiados cromossomas e uma não tem o suficiente.
Células cancerígenas são muito frequentemente aneuploid. Os humanos têm normalmente 46 cromossomas nas suas células, mas as células cancerígenas têm muitas vezes muito mais, por vezes mais do que 100. A presença dos cromossomas extras torna as células instáveis e perturba severamente os controles de divisão celular. Existe actualmente um debate em curso sobre se todos os cancros são ou não aneuploides. Independentemente de ser esse o caso, é claro que a aneuploidia é uma característica comum das células cancerígenas.
Alterações Epigenéticas
Além das alterações reais na sequência de DNA, a expressão gênica pode ser alterada por alterações no DNA e na cromatina que não alteram a sequência. Como essas alterações não alteram a seqüência do DNA nos genes, elas são chamadas de alterações epigenéticas. Dois tipos de alterações epigenéticas são descritos abaixo.
Metilação
Nesta alteração, alguns nucleotídeos no DNA são modificados pela adição de um grupo metilo (-CH3) à base. A metilação do DNA está associada com a inativação dessa região específica do DNA. Foram observados padrões anormais de metilação do ADN em células cancerosas. Tal como as alterações descritas, a metilação altera a expressão dos genes afectados.
Acetilação
Nesta alteração epigenética, as proteínas histónicas em torno das quais o ADN é ferido tornam-se modificadas pela adição de grupos acetil (-CH3CHO). Esta alteração leva a um afrouxamento da interacção DNA:histone e está associada a um aumento da expressão genética. A modificação dos processos de adição e remoção de grupos acetil ao ADN é uma área activa de investigação do tratamento do cancro.
Mais sobre alterações epigenéticas e tratamentos do cancro.
Causas de Mutação
Como vimos, as células cancerígenas são criadas a partir de células precursoras normais através de uma acumulação de danos genéticos. Os mecanismos pelos quais as alterações são induzidas são variados. Em um sentido amplo, os agentes de mudança genética (mutação) enquadram-se principalmente nas categorias descritas abaixo e são discutidos em profundidade na seção seguinte.
Mutações espontâneas
Mutações espontâneas: As bases (A, T, G, C) no DNA são alteradas ou perdidas devido a erros de replicação não reparados ou eventos moleculares aleatórios. Por exemplo, a perda de um grupo amino de citosina, uma base normal encontrada no DNA, leva à produção de uracil, uma base normalmente não encontrada no DNA. Se esta alteração não for detectada e revertida, pode ocorrer uma mutação. Ocasionalmente, uma base inteira pode ser perdida como resultado da clivagem da ligação entre a espinha dorsal do ADN e a base. Isto leva a uma lacuna na hélice dupla do ADN, que, se não for reparada, pode levar a uma mutação na próxima vez que o ADN for copiado (ou seja, durante a replicação).
Mutações induzidas
Mutações induzidas: As mutações podem ser induzidas pela exposição de organismos (ou células) a uma variedade de tratamentos. Algumas das mais comuns são:
Radiação- Uma das primeiras mutações conhecidas, a radiação é um potente indutor de mutações. Diferentes tipos de radiação causam diferentes tipos de alterações genéticas. A radiação ultravioleta (UV) causa mutações pontuais. Os raios X podem causar quebras na dupla hélice do DNA e levar a translocações, inversões e outros tipos de danos cromossômicos. A exposição aos raios UV na luz solar tem sido ligada ao câncer de pele. Observe que as propriedades nocivas da radiação ao DNA foram utilizadas em vários tratamentos diferentes de câncer baseados em radiação.
Mostrado abaixo é um tipo de mutação que é causada pela radiação ultravioleta. Neste exemplo, o bombardeamento da dupla hélice do DNA pelos raios UV faz com que duas bases se unam. Isto altera a estrutura do DNA e pode levar a mudanças permanentes se não for reparado.
Outro tipo de radiação é a energia emitida por elementos radioativos naturais (como radônio e urânio) ou fontes artificiais como aquelas encontradas (e criadas) em reatores nucleares. A radiação deste tipo vem em diferentes tipos e pode causar diferentes tipos de danos às células e tecidos. A radiação pode danificar diretamente o DNA ou pode causar a formação de produtos químicos (isto é, espécies reativas de oxigênio ou ROS) que podem danificar o DNA ou outros componentes celulares.
A exposição à radiação de materiais radioativos foi bem documentada. Análises dos sobreviventes das bombas atômicas lançadas sobre o Japão durante a Segunda Guerra Mundial mostraram grandes aumentos nas leucemias logo após a exposição e depois aumentos em outros tipos de câncer nas décadas seguintes.8
Quantidades perigosas de materiais radioativos também foram liberadas acidentalmente de usinas nucleares. A exposição à radiação devido à liberação acidental de materiais radioativos do reator nuclear de Chernobyl tem sido associada a aumentos no câncer de tiróide e outros cânceres malignos.9
Máquinas de imagem médica (como máquinas de raio X e tomógrafos) também expõem os pacientes à radiação. As quantidades usadas para qualquer teste não são consideradas como causadoras de quantidades significativas de câncer, mas o impacto a longo prazo de muitos testes durante um período de anos não é claro.10 Da mesma forma, a exposição dos passageiros de avião a exames de corpo inteiro em aeroportos não é considerada como representando um risco de câncer.11 Os passageiros que voam em aviões também são expostos à radiação do espaço, mas a um nível baixo e não se pensa que representem um risco de câncer, mesmo para os membros da tripulação.1112
Mutagênios químicos – Sabe-se que muitos produtos químicos diferentes causam mutações. Essas substâncias químicas exercem seu efeito ligando-se ao DNA ou aos blocos de construção do DNA e interferindo com os processos de replicação ou transcrição. Alguns exemplos de mutagénicos potentes são o benzo-a-pireno, um químico encontrado na fumaça do cigarro, e a aflatoxina, um mutagénico mais frequentemente encontrado em produtos agrícolas mal armazenados.
Inflamação Crônica – A inflamação crônica pode levar a danos no DNA devido à produção de produtos químicos mutagénicos pelas células do sistema imunológico. Um exemplo seria a inflamação prolongada causada pela infecção com o vírus da hepatite. Saiba mais sobre vírus e câncer.
Oxygen Radicals- Durante a captura de energia dos alimentos, que ocorre em nossas mitocôndrias, podem ser gerados produtos químicos que são muito reativos e capazes de danificar as membranas celulares e o próprio DNA. Estes intermediários de oxigénio reactivos (ROI) também podem ser gerados pela exposição das células à radiação, como mostrado abaixo.
A actividade mutagénica do ROI está associada ao desenvolvimento do cancro, bem como às actividades de vários tratamentos anticancerígenos, incluindo a radiação e a quimioterapia. 131415
Abnormal Cell Division
Mitose, é possível que o processo de divisão celular não consiga dividir os cromossomas replicados com precisão em duas células filhas. Um erro deste tipo levará à produção de células aneuplóides. As células ou estarão ausentes, ou terão ganho um número significativo de genes. Este processo raro pode criar células que são mais propensas à divisão celular não regulada. Como dito anteriormente, uma grande porcentagem de cânceres isolados de humanos são aneuplóides.
Se uma célula tem uma mutação em um gene cujo produto protéico é responsável pela ‘verificação’ do processo de divisão, as coisas podem ficar rapidamente fora de controle e as células filhas de cada divisão podem se tornar cada vez mais anormais.
Vírus como Mutagens
Vírus são considerados responsáveis por uma porcentagem significativa de casos de câncer. Os vírus podem causar cancro de várias formas e a forma como cada tipo de vírus funciona é provavelmente ligeiramente diferente. Alguns vírus (incluindo muitos retrovírus) podem causar mutações pela inserção dos seus genes no genoma da célula infectada. O DNA inserido pode destruir ou alterar a atividade dos genes afetados.161718
Vírus também podem causar mutações de forma indireta. Como um exemplo: Uma infecção com o vírus da hepatite pode durar muitos anos. Durante esse tempo o sistema de defesa do organismo tenta se livrar do vírus, produzindo produtos químicos tóxicos. Essas substâncias químicas podem causar danos às células “espectadoras” saudáveis, enviando-as pelo caminho que leva ao cancro. Existem inúmeras outras formas de vírus causarem câncer.1920
Por causa da importância dos vírus no desenvolvimento de muitos cancros, criamos uma seção dedicada a vírus e câncer.
Transposões como Mutagens
Transposões são sequências curtas de DNA que têm a capacidade de se mover de um local no DNA para outro local. Transposons codificam uma enzima, transposase, que atua para unir o transposon em novos locais em um genoma (ver esquema, abaixo à esquerda, de um transposon) Transposons foram descobertos por Barbara McClintock e ela ganhou um prêmio Nobel por seu trabalho.2122 O genoma humano contém muitas cópias inativadas de transposons que perderam sua capacidade de se mover ou ‘pular’ para novos locais. Cerca de 50% do genoma humano é composto de transposons ‘mortos’.23
O movimento de transposons ativos pode levar a mutações, alterando a atividade dos genes. Um exemplo visível do movimento dos transposons (chamado transposição), é a coloração dos grãos no milho indiano (ver abaixo à direita). Pensa-se que os transposons que são activos em humanos estão envolvidos em doenças humanas, incluindo o cancro.242526


Resumo da mutação
Mudança genética (mutação) Introdução
- Os comportamentos anormais demonstrados pelas células cancerígenas são o resultado de uma série de mutações em genes reguladores chave (isto é, genes reparadores de DNA).
- Pensa-se que a maior parte dos cancros são provenientes de uma única célula precursora que adquire mutações suficientes para se tornar uma célula cancerígena.
Mutações de ADN
- Mudanças genéticas podem ser pequenas, afectando apenas um ou alguns nucleótidos (mutações pontuais) ou podem ser bastante grandes, alterar a estrutura de um cromossoma ou cromossomas.
- Mutações pontuais
- Tradução é a produção de uma proteína por enzimas que ‘lêem’ três nucleotídeos ‘palavras’ (códons) ao longo de um RNA mensageiro (mRNA).
- A alteração de um único nucleotídeo ao longo do DNA de um gene pode levar a uma proteína completamente não-funcional. As mutações são agrupadas de acordo com as mudanças que elas criam no produto protéico resultante do gene afetado.
- Mutações sem sentido – O novo códão (mutante) faz com que a síntese protéica pare prematuramente.
- Mutações com sentido – O códão alterado resulta na inserção de um aminoácido incorreto na proteína.
- Mutações Frameshift – A perda ou ganho de 1 ou 2 nucleotídeos em um mRNA faz com que os códons sejam mal lidos. Frequentemente resulta em proteínas encurtadas e não funcionais.
- Mudanças de nível cromossómico
- Translocações – Quebra e (às vezes) troca de fragmentos cromossómicos.
- Amplificação de genes – A replicação anormal cria múltiplas cópias de uma região de um cromossoma. Em última instância, isto leva à superprodução das proteínas correspondentes.
- Inversões – Segmentos de DNA são liberados de um cromossomo e então reinseridos na orientação oposta.
- Duplicações/Deleções – Um gene ou grupo de genes pode se perder completamente ou ser copiado mais de uma vez dentro de um cromossomo.
- Aneuploidia – Uma alteração genética que envolve a perda ou ganho de cromossomas inteiros.
- Mutações espontâneas podem ocorrer devido a DNA não reparado ou eventos moleculares aleatórios.
- Aneuploidia é muito comum em células cancerígenas.
Mudanças Epigenéticas
- Expressão do gene pode ser alterada por alterações no DNA e cromatina que não alteram a sequência genética. Exemplos incluem metilação do DNA e acetilação das histonas.
- Metilação – Alguns nucleotídeos no DNA são modificados pela adição de um grupo metilo que está associado com a inativação daquela região do DNA
- Acetilação – A adição de grupos acetil afrouxa o DNA e aumenta a expressão gênica.
Mutações induzidas
- Mutações podem ser induzidas expondo organismos (ou células) a uma variedade de tratamentos:
- Radiação – Os raios UV causam mutações pontuais e os raios X causam múltiplas formas de danos.
- Mutagens químicas – Podem ligar-se ao DNA ou aos blocos de construção do DNA e interferir com os processos de replicação ou transcrição.
- Inflamação Crônica – Danos ao DNA devido à produção de produtos químicos mutagênicos pelas células do sistema imunológico
- Radicais de oxigênio – Resultados da produção de energia de uma célula e podem danificar o DNA.
Outras alterações genéticas
- Divisão celular dominante resultando em divisão incorrecta dos cromossomas pode levar à aneuploidia.
- Os vírus podem causar danos genéticos de várias formas diferentes e estão associados a uma vasta gama de cancros.
Mutação e câncer
- Parece que a transição de uma célula normal e saudável para uma célula cancerígena é uma progressão gradual.
- O desenvolvimento do câncer requer alterações genéticas em vários oncogenes e supressores tumorais diferentes.
- Todos os cânceres têm que superar o mesmo espectro de funções reguladoras para crescer e progredir, mas os genes envolvidos podem ser diferentes.
- A heterogeneidade do câncer complica o diagnóstico e o tratamento.
- É possível herdar genes disfuncionais levando ao desenvolvimento de uma forma familiar de um tipo particular de câncer.
Conhecer o Fluxo: Mutação
Saber o Fluxo é um jogo interativo para você testar seu conhecimento. Para jogar:
- Arraste as escolhas apropriadas da coluna da direita e coloque-as em ordem nas caixas da esquerda. Note que você só vai usar cinco das seis escolhas para completar o jogo.
- Quando terminar, clique em ‘Check’ para ver quantas você acertou.
- Para respostas incorretas, clique em ‘Description’ para rever as informações sobre os processos.
- Para tentar novamente, escolha ‘Reset’ e comece de novo.
-
1
-
2
-
3
-
4
-
5
-
Saiba maisUma célula está no processo de síntese de DNA
-
Saiba maisMuitas cópias de uma região de um cromossoma são feitas
-
Saiba maisTranscrição de genes amplificados
-
Saiba maisTranslação de genes amplificados
-
Saiba maisOverprodução de uma chave A proteína leva ao crescimento de tumor resistente a drogas
-
Aprenda maisDuplicação Ocorre
Tocar novamente
- 1. Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). Campbell Biology (11ª ed.). Pearson.
- 2. Vigilância, Epidemioloy, e Resultados Finais (SEER) representados pelo Instituto Nacional do Câncer
- 3. Hahn WC, Counter CM, Lundberg AS, Beijerbergen RL, Brooks MW, Weinberg RA. “Criação de células tumorais humanas com elementos genéticos definidos”. Natureza 400: 464-468
- 4. Welch JS, Ley TJ, Link DC, Westervelt P, Walter MJ, Graubert TA, DiPersio JF, Ding L, Mardis ER, Wilson RK et al. A origem e evolução das mutações na leucemia mielóide aguda. Cell, 20 de julho de 2012
- 5. Brégeon D, Doetsch PW. Transcriptional mutagenesis: causes and involvement in tumour development. Nat Rev Cancer. 2011 Mar;11(3):218-27.
- 6. Nowell PC, Hungerford DA. “Estudos cromossómicos sobre leucócitos humanos normais e leucémicos”. J Natl Cancer Inst (1960). 25: 85-100.
- 7. Rowley JD. “Uma nova anormalidade cromossômica consistente em leucemia mielóide crônica identificada por fluorescência de quinacrina e coloração de Giemsa”. Natureza (1973). 243: 290-293.
- 8. Ozasa K, Shimizu Y, Sakata R, Sugiyama H, Grant EJ, Soda M, Kasagi F, Suyama A. RISCO DE CÂNCER E DOENÇAS NÃO CÂNCERESAS NA BOMBA ATÔMICA. Dosimetria de Prot. Radiat Prot. 2011 Abr 18.
- 9. Cardis E, Hatch M. O Acidente de Chernobyl – uma perspectiva epidemiológica. Clin Oncol (R Coll Radiol). 2011;23(4):251-260. doi:10.1016/j.clon.2011.01.510 Mar 9.
- 10. Fazel R, Krumholz HM, Wang Y, Ross JS, Chen J, Ting HH, Shah ND, Nasir K, Einstein AJ, Nallamothu BK. Exposição à radiação ionizante de baixa dose de procedimentos de imagem médica. N Engl J Med. 2009 Ago 27;361(9):849-57.
- 11. a. b. Mehta P, Smith-Bindman R. Screening Full-Body Screening do Aeroporto: Qual é o risco? Arch Intern Med. 2011 Mar 28.
- 12. Bagshaw M. Radiação cósmica na aviação comercial. Travel Med Infect Dis. 2008 maio;6(3):125-7. Epub 2007 Nov 26.
- 13. Kang DH. “Oxidative Stress, DNA damage and breast cancer”. AACN Clinues Issues. (2002). 13:540-549
- 14. Athar M. “Stress oxidativo e carcinogênese experimental”. Indiano J. Exp. Biol. (2002). 40:656-667
- 15. Marnett LJ. “Radicais oxidantes, peroxidação lipídica e danos no DNA.” (2002)181-182:219-222
- 16. Nair V. Oncogénese induzida por retrovírus e segurança dos vectores retrovirais. Curr Opinião Mol Ther. 2008 Out;10(5):431-8.
- 17. Brady G, Macarthur GJ, Farrell PJ. Vírus Epstein-Barr e linfoma de Burkitt. Postgrad Med J. 2008 Jul;84(993):372-7.
- 18. Ruprecht K, Mayer J, Sauter M, Roemer K, Mueller-Lantzsch N. Endogenous retroviruses and cancer. Cell Mol Life Sci. 2008 Nov;65(21):3366-82.
- 19. Lupberger J, Hildt E. Hepatite B oncogénese induzida pelo vírus da hepatite B. Mundo J Gastroenterol. 2007 Jan 7;13(1):74-81.
- 20. Castello G, Scala S, Palmieri G, Curley SA, Izzo F. Carcinoma hepatocelular relacionado ao HCV: Da inflamação crónica ao cancro. Clin Immunol. 2010 Mar;134(3):237-50. Epub 2009 Nov 11.
- 21. McClintock B. A origem e o comportamento dos loci mutáveis no milho. Proc Natl Acad Sciad U S A. 1950 Jun;36(6):344-55.
- 22. McClintock, Bárbara Prêmio Nobel de Palestra
- 23. Burns KH, Boeke JD. Tectónica de transposição humana. Célula. 2012 maio 11;149(4):740-52.
- 24. Kozeretska IA, Demydov SV, Ostapchenko LI. Elementos genéticos móveis e cancro. Das mutações à terapia genética. Exp Oncol. 2011 Dez;33(4):198-205.
- 25. Solyom S, Kazazian HH Jr. Elementos móveis no genoma humano: implicações para a doença. Genoma Med. 2012 Fev 24;4(2):12.
- 26. Iskow RC, McCabe MT, Mills RE, Torene S, Pittard WS, Neuwald AF, Van Meir EG, Vertino PM, Devine SE. Mutagênese natural de genomas humanos por retrotransposições endógenas. Células. 2010 Jun 25;141(7):1253-61.