Legea dezintegrării radioactive
Când un nucleu individual se transformă în altul cu emisie de radiații, se spune că nucleul se dezintegrează. Dezintegrarea radioactivă are loc pentru toate nucleele cu \(Z > 82\), dar și pentru unii izotopi instabili cu \(Z < 83\). Rata de dezintegrare este proporțională cu numărul N de nuclee originale (nedecuplate) dintr-o substanță. Numărul de nuclee pierdute prin dezintegrare, \(-dN\) în intervalul de timp dt, se scrie
\
unde \(\lambda\) se numește constanta de dezintegrare. (Semnul minus indică faptul că numărul de nuclee originale scade în timp.) Cu alte cuvinte, cu cât mai multe nuclee disponibile pentru dezintegrare, cu atât mai multe sunt cele care se dezintegrează (în intervalul de timp dt). Ecuația \ref{eq2} poate fi rescrisă sub forma
\
Integrând ambele părți ale ecuației și definind \(N_0\) ca fiind numărul de nuclee la \(t = 0\), obținem
\
Aceasta ne dă
Cuprinzând partea stângă și partea dreaptă a ecuației \ref{eq4} ca o putere a lui \(e\), avem legea dezintegrării radioactive.
Legea dezintegrării radioactive
Numărul total \(N\) de nuclee radioactive rămase după un timp \(t\) este
\
unde \(\lambda\) este constanta de dezintegrare pentru nucleul respectiv.
Numărul total de nuclee scade foarte rapid la început, iar apoi mai lent (Figura \(\PageIndex{2}\)).
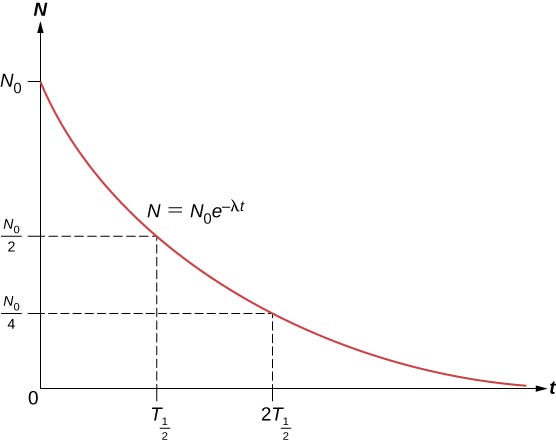
Viața de înjumătățire \((T_{1/2})\) a unei substanțe radioactive este definită ca fiind timpul în care jumătate din nucleele originale se dezintegrează (sau timpul la care rămâne jumătate din nucleele originale). Timpul de înjumătățire al izotopilor instabili este prezentat în tabelul de nuclizi. Prin urmare, numărul de nuclee radioactive rămase după un număr întreg (n) de înjumătățiri este
\
Dacă constanta de dezintegrare \((\lambda)\) este mare, timpul de înjumătățire este mic, și viceversa. Pentru a determina relația dintre aceste mărimi, rețineți că atunci când \(t = T_{1/2}\), atunci \(N = N_0/2\).
Așa, ecuația \ref{eq5} poate fi rescrisă ca
\
Divizând ambele părți cu \(N_0\) și luând logaritmul natural se obține
\
care se reduce la
\
Așa, dacă cunoaștem timpul de înjumătățire T1/2 al unei substanțe radioactive, putem afla constanta de dezintegrare a acesteia. Durata de viață \(\overline{T}\) a unei substanțe radioactive este definită ca fiind durata medie de timp în care un nucleu există înainte de a se dezintegra. Durata de viață a unei substanțe este doar reciproca constantei de dezintegrare, scrisă sub forma
\
Activitatea A este definită ca mărime a vitezei de dezintegrare, sau
\
Variația infinitezimală dN în intervalul de timp dt este negativă deoarece numărul de particule mamă (nedecompuse) este în scădere, astfel încât activitatea (A) este pozitivă. Definind activitatea inițială ca fiind \(A_0 = \lambda N_0\), avem
\
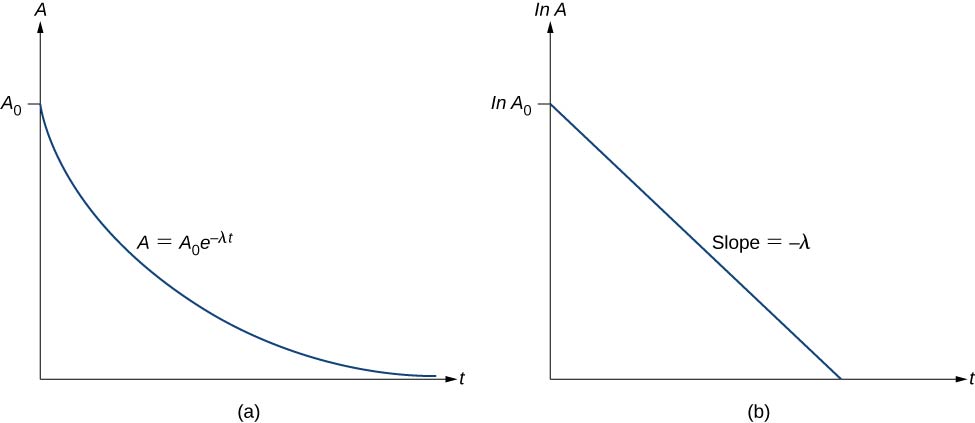
Din acest motiv, activitatea A a unei substanțe radioactive scade exponențial cu timpul (Figura \(\PageIndex{3}\)).
Exemplu \(\PageIndex{1}\): Constanta de dezintegrare și activitatea stronțiului-90
Viața de înjumătățire a stronțiului-90, \(\ce{_{38}^{90}Sr}\), este de 28,8 y. Găsiți (a) constanta sa de dezintegrare și (b) activitatea inițială a 1,00 g de material.
Strategie
Potem găsi constanta de dezintegrare direct din ecuația \ref{eq8}. Pentru a determina activitatea, trebuie mai întâi să aflăm numărul de nuclee prezente.
Soluție
a. Se constată că constanta de dezintegrare este
\
b. Masa atomică a \(_{38}^{90}Sr\) este de 89,91 g. Utilizând numărul lui Avogadro \(N_A = 6,022 \ ori 10^{23}\) atomi/mol, aflăm numărul inițial de nuclee din 1,00 g de material:
\
Din aceasta, aflăm că activitatea \(A_0\) la \(t = 0\) pentru 1.00 g de stronțiu-90 este
\
Exprimând \(\lambda\) în termeni de timp de înjumătățire a substanței, obținem
\
Deci, activitatea se înjumătățește după un timp de înjumătățire. Putem determina constanta de dezintegrare \(\lambda\) prin măsurarea activității în funcție de timp. Luând logaritmul natural al laturilor stângă și dreaptă ale Ecuației \ref{eq11}, obținem
\
Această ecuație urmează forma liniară \(y = mx + b\). Dacă reprezentăm grafic \ln A în funcție de t, ne așteptăm la o linie dreaptă cu panta \(-\lambda\) și intersecția y \(\ln \, A_0\) (Figura \(\PageIndex{3b}\)). Activitatea A este exprimată în unități de becquereli (Bq), unde un \(1 \, Bq = 1 \, dezintegrare \, pe \, secundă\). Această cantitate poate fi, de asemenea, exprimată în descompuneri pe minut sau în descompuneri pe an. Una dintre cele mai comune unități de măsură pentru activitate este curie (Ci), definită ca fiind activitatea a 1 g de \(^{226}Ra\). Relația dintre Bq și Ci este
\
Exemplu \(\PageIndex{2}\): Care este activitatea\(^{14}C\) în țesuturile vii?
Aproximativ \(20\%\) din corpul uman, ca masă, este carbon. Calculați activitatea datorată \(^{14}C\) în 1,00 kg de carbon care se găsește într-un organism viu. Exprimați activitatea în unități de Bq și Ci.
Strategie
Activitatea \(^{14}C\) se determină cu ajutorul ecuației \(A_0 = \lambda N_0\), unde λ este constanta de dezintegrare și \(N_0\) este numărul de nuclee radioactive. Numărul de nuclei de \(^{14}C\) dintr-un eșantion de 1,00 kg se determină în două etape. În primul rând, se determină numărul de nuclee \(^{12}C\) folosind conceptul de mol. În al doilea rând, înmulțim această valoare cu \(1,3 \ ori 10^{{-12}\) (abundența cunoscută de \(^{14}C\) într-o mostră de carbon dintr-un organism viu) pentru a determina numărul de nuclei de \(^{14}C\) dintr-un organism viu. Constanta de dezintegrare se determină din timpul de înjumătățire cunoscut al \(^{14}C\) (disponibil la ).
Soluție
Un mol de carbon are o masă de 12,0 g, deoarece este \(^{12}C\) aproape pur. Astfel, numărul de nuclee de carbon într-un kilogram este
\
Numărul de nuclee de \(^{14}C\) din 1 kg de carbon este deci
\
Acum putem afla activitatea \(A\) folosind Ecuația \ref{eq11}. Introducând valorile cunoscute ne dă
\
sau \(7,89 \ ori 10^9\) descompuneri pe an. Pentru a converti această valoare în unitatea Bq, pur și simplu convertim anii în secunde. Astfel,
\
sau 250 de dezintegrări pe secundă. Pentru a exprima A în curies, folosim definiția unui curie,
\
Așa,
Semnificație
Aproximativ \(20\%\) din corpul uman, în greutate, este carbon. Sute de dezintegrări de \(^{14}C\) au loc în corpul uman în fiecare secundă. Carbonul-14 și alte substanțe radioactive prezente în mod natural în organism alcătuiesc expunerea de fond a unei persoane la radiații nucleare. După cum vom vedea mai târziu în acest capitol, acest nivel de activitate este cu mult sub dozele maxime recomandate.
.