Cancerul este rezultatul cedării controalelor care reglează celulele. Cauzele acestei defecțiuni includ întotdeauna modificări ale unor gene importante. Aceste modificări sunt adesea rezultatul unor mutații, modificări în secvența ADN a cromozomilor. Mutațiile pot fi modificări foarte mici, afectând doar câteva nucleotide sau pot fi foarte mari, ducând la schimbări majore în structura cromozomilor.
Atât mutațiile mici cât și cele mari pot afecta comportamentul celulelor. Combinațiile de mutații în gene importante pot duce la apariția cancerului. Materialul abordat în această pagină descrie relația dintre mutație și cancer, diferitele tipuri de mutații și cauzele acestora. Informații suplimentare despre subiectele de pe această pagină pot fi găsite și în majoritatea manualelor introductive de biologie, vă recomandăm Campbell Biology, ediția a 11-a.1
Subiecte de pe această pagină:
- Mutații și cancer
- Mutații ereditare și cancer
- Tipuri de mutații
- Mutații punctiforme
- Translocații
- Amplificarea genelor
- Inversiuni, Deleții și duplicații
- Modificări epigenetice
Aneuploidie
Mutația și cancerul
Comportamentele anormale demonstrate de celulele canceroase sunt rezultatul unei serii de mutații în genele reglatoare cheie. Celulele devin progresiv mai anormale pe măsură ce mai multe gene sunt afectate. Adesea, genele care controlează repararea ADN-ului devin ele însele deteriorate, ceea ce face ca celulele să fie și mai susceptibile la niveluri tot mai mari de haos genetic.
Acesta este o animație care demonstrează relația dintre cromozomi, gene și ADN.
Se crede că majoritatea cancerelor apar de la o singură celulă precursoare mutantă. Pe măsură ce acea celulă se divide, celulele „fiice” rezultate pot dobândi diferite mutații și comportamente diferite de-a lungul unei perioade de timp. Acele celule care obțin un avantaj în ceea ce privește diviziunea sau rezistența la moartea celulară vor avea tendința de a prelua controlul asupra populației. În acest fel, celulele tumorale sunt capabile să dobândească o gamă largă de capacități care nu sunt observate în mod normal în versiunea sănătoasă a tipului de celule reprezentat. Modificările de comportament observate în celulele canceroase sunt punctul central al secțiunii Biologia cancerului din site.
Mutațiile în genele de reglementare cheie (supresori tumorali și proto-oncogene) modifică comportamentul celulelor și pot duce, potențial, la creșterea nereglementată observată în cancer.
Pentru aproape toate tipurile de cancer studiate până în prezent, se pare că trecerea de la o celulă normală, sănătoasă, la o celulă canceroasă este o progresie în trepte care necesită multe modificări genetice care se adaugă pentru a crea celula canceroasă. Aceste mutații apar atât la nivelul oncogenelor, cât și al supresorilor tumorali. Acesta este unul dintre motivele pentru care cancerul este mult mai răspândit la persoanele în vârstă. Pentru a genera o celulă canceroasă, trebuie să apară o serie de mutații în aceeași celulă. Având în vedere că probabilitatea ca orice genă să sufere o mutație este foarte mică, este de la sine înțeles că șansa ca mai multe mutații diferite să apară în aceeași celulă este cu adevărat foarte puțin probabilă. Din acest motiv, celulele dintr-un organism în vârstă de 70 de ani au avut la dispoziție mai mult timp pentru a acumula modificările necesare pentru a forma celule canceroase, dar cele ale unui copil au mult mai puține șanse să fi dobândit modificările genetice necesare. Desigur, unii copii fac cancer, dar acesta este mult mai frecvent la persoanele mai în vârstă. Graficul de mai jos prezintă ratele de cancer de colon în Statele Unite în funcție de vârstă. Graficul a fost obținut de la Institutul Național de Cancer. 2
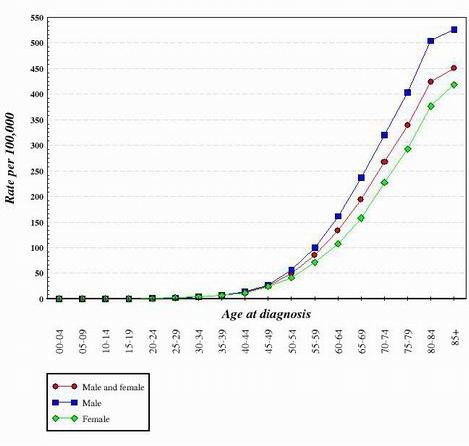
Urmărind forma unor curbe precum cele prezentate mai sus, s-a ajuns la concluzia că sunt necesare mai multe modificări genetice pentru a crea celule care devin canceroase.
În laborator, cercetătorii au încercat să creeze celule tumorale prin modificarea sau introducerea unor proteine reglatoare cheie. Mai multe studii au încercat să definească numărul minim de modificări genetice necesare pentru a crea o celulă canceroasă, cu rezultate intrigante.3
În natură, mutațiile se pot acumula în celule în timp și, dacă grupul „potrivit” de gene suferă mutații, poate rezulta cancerul. Un studiu din 2012 a arătat că celulele stem din măduva osoasă la o persoană sănătoasă acumulează multe mutații pe măsură ce persoana respectivă îmbătrânește. Doar câteva modificări în plus ale unor gene cheie pot provoca cancer. Rezultatele implică faptul că celulele „normale” și celulele canceroase ar putea să nu fie atât de diferite în multe cazuri.4
Mutații ereditare în cancer
Pentru a complica lucrurile, este clar că modificările necesare pentru a crea o celulă canceroasă pot fi realizate în multe moduri diferite. Deși toate cancerele trebuie să depășească același spectru de funcții de reglementare pentru a se dezvolta și a progresa, genele implicate pot fi diferite. În plus, ordinea în care genele se dereglează sau se pierd poate, de asemenea, să varieze. Ca exemplu, tumorile de cancer de colon de la doi indivizi diferiți pot implica seturi foarte diferite de supresori tumorali și oncogene, chiar dacă rezultatul (cancer) este același.
Eterogenitatea mare observată în cazul cancerului, chiar și al celor din același organ, înseamnă că diagnosticul și tratamentul sunt complicate. Progresele actuale în clasificarea moleculară a tumorilor ar trebui să permită conceperea rațională a protocoalelor de tratament pe baza genelor reale implicate în fiecare caz în parte. Noile teste de diagnosticare pot implica depistarea a sute sau mii de gene pentru a crea un profil personalizat al tumorii la un individ. Aceste informații ar trebui să permită adaptarea tratamentelor împotriva cancerului în funcție de individ. Pentru mai multe informații în acest sens, consultați secțiunea Genomică/Proteomică.
Modificările genetice care duc la creșterea nereglementată a celulelor pot fi dobândite în două moduri diferite. Este posibil ca mutația să apară treptat, de-a lungul unui număr de ani, ducând la dezvoltarea unui caz „sporadic” de cancer. Alternativ, este posibil să se moștenească gene disfuncționale care duc la dezvoltarea unei forme familiale a unui anumit tip de cancer. Câteva exemple de cancere cu componente ereditare cunoscute includ:
- Cancerul de sân- Moștenirea unor versiuni mutante ale genelor BRCA1 și BRCA2 sunt factori de risc cunoscuți. Deși multe, dacă nu majoritatea persoanelor cu cancer de sân nu prezintă modificări detectabile în aceste gene, faptul de a avea o formă mutantă crește probabilitatea de a dezvolta cancer de sân.
- Cancerul de colon- Se știe că defectele în genele de reparare a ADN-ului, cum ar fi MSH2, predispun indivizii la cancer colorectal ereditar fără polipoză (HNPCC).
- Retinoblastomul- Se știe că defectele în gena supresoare a tumorii Rb cauzează acest cancer al ochiului și alte câteva tipuri de cancere. Mai multe despre această boală particulară pot fi găsite în secțiunea privind Rb
Aceasta este o listă incompletă a tipurilor de cancer moștenite cunoscute și este sigur că vor fi identificate mai multe forme de cancer moștenite, pe măsură ce se va clarifica genetica diferitelor tipuri de cancer.
Mai multe informații pe această temă pot fi găsite în capitolele 2 și 4 din The Biology of Cancer de Robert A. Weinberg.
Tipuri de mutații
Procesul prin care sunt fabricate proteinele, traducerea, se bazează pe „citirea” ARNm care a fost produs prin procesul de transcriere. Orice modificare a ADN-ului care codifică o genă va duce la o alterare a ARNm produs. La rândul său, ARNm alterat poate duce la producerea unei proteine care nu mai funcționează corespunzător. Chiar și modificarea unei singure nucleotide de-a lungul ADN-ului unei gene poate duce la o proteină complet nefuncțională.
Există mai multe moduri diferite în care ADN-ul poate fi alterat. Următoarea secțiune descrie mai detaliat diferitele tipuri de modificări genetice.
Mutații punctiforme
Alterările genetice pot fi încadrate în două categorii generale. Prima categorie este formată din modificări care modifică doar una sau câteva nucleotide de-a lungul unui lanț de ADN. Aceste tipuri de modificări sunt denumite mutații punctiforme.
Când ribozomii citesc o moleculă de ARN mesager, fiecare trei nucleotide este interpretată ca un aminoacid. Aceste coduri de trei litere se numesc codoni. Pentru a face o analogie cu o propoziție în limba engleză: „Pisica grasă a mâncat șobolanul” ar conține 6 codoni. Modificările cauzate de mutație pot duce la lucruri precum „Liliacul gras a mâncat șobolanul.” sau „Fa” sau „Grasa oca tat-o la…”. Impactul asupra proteinei depinde de locul în care are loc modificarea și de tipul de modificare.
Codonii de trei litere citiți de ribozomi pot fi modificați prin mutație într-unul din cele trei moduri:
Mutații fără sens
Noul codon face ca proteina să se termine prematur, producând o proteină care este scurtată și care adesea nu funcționează corect sau nu funcționează deloc.
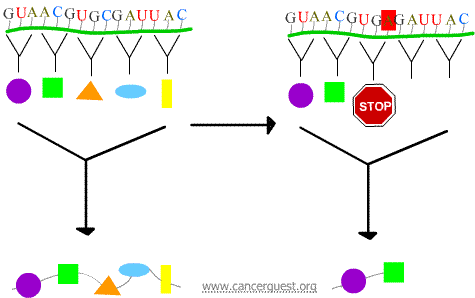
Mutații misense
Noul codon determină inserarea unui aminoacid incorect în proteină. Efectele asupra funcției proteinei depind de ceea ce este inserat în locul aminoacidului normal.

Mutații de deplasare a cadrelor
Pierderea sau câștigarea a 1 sau 2 nucleotide determină citirea greșită a codonului afectat și a tuturor codonilor care îl urmează. Acest lucru duce la un produs proteic foarte diferit și adesea nefuncțional.
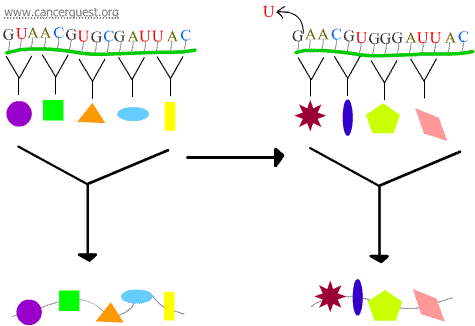
Erorile de transcriere
Câteva leziuni ale ADN-ului au ca rezultat un nucleotid modificat sau un grup mic de nucleotide care nu poate fi „citit” de ARN polimeraza. Atunci când complexul ARN-polimerazei ajunge în aceste puncte, va ocoli uneori deteriorarea prin adăugarea de nucleotide într-un efort de a continua, chiar dacă asta înseamnă să pună ceva greșit. Acest proces este cunoscut sub numele de mutageneză transcripțională și poate juca un rol semnificativ în dezvoltarea cancerului.5
Translocații
O altă categorie de mutații implică alterări ale unor cantități mai mari de ADN, adesea la nivelul cromozomului. Acestea se numesc translocații și implică ruperea și deplasarea unor fragmente de cromozomi. Adesea, rupturile în doi cromozomi diferiți permit formarea a doi cromozomi „noi”, cu noi combinații de gene.
În timp ce ar putea părea că acest lucru nu ar cauza prea multe probleme, deoarece toate genele sunt încă prezente, procesul poate duce la o creștere celulară dereglementată într-un număr de moduri-
1. Este posibil ca genele să nu fie transcrise și traduse în mod corespunzător în noua lor locație.
2. Mișcarea unei gene poate duce la o creștere sau la o scădere a nivelului de transcriere a acesteia.
3. Ruperea și reunirea pot avea loc, de asemenea, în cadrul unei gene (așa cum se arată în verde mai sus), ceea ce duce la inactivarea acesteia.
Pentru unele tipuri de cancer, anumite translocații sunt foarte frecvente și pot fi chiar folosite în diagnosticarea bolii. Translocațiile sunt frecvente în leucemii și limfoame și au fost mai rar identificate în cancerele țesuturilor solide. Un exemplu ar fi un schimb între cromozomii 9 și 22 observat la peste 90% dintre pacienții cu leucemie mielogenă cronică (LMC). Schimbul duce la formarea unei forme scurtate a cromozomului 22, numită cromozomul Philadelphia (după locul în care a fost descoperit). Această translocație duce la formarea unei oncogene din proto-oncogenul abl.67
Alte tipuri de cancer care sunt adesea (sau întotdeauna) asociate cu anumite translocații includ limfomul Burkitt, limfoamele cu celule B și mai multe tipuri de leucemie.
Amplificarea genelor
În acest proces foarte neobișnuit, procesul normal de replicare a ADN-ului este serios afectat. Rezultatul este că, în loc să se realizeze o singură copie a unei regiuni a unui cromozom, se produc mai multe copii. Acest lucru duce la producerea mai multor copii ale genelor care sunt localizate pe acea regiune a cromozomului. Uneori, sunt produse atât de multe copii ale regiunii amplificate încât acestea pot forma de fapt propriii lor pseudo-cromozomi mici, numiți cromozomi de două minute.
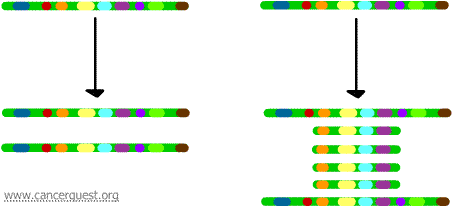
Genele de pe fiecare dintre copii pot fi transcrise și traduse, ceea ce duce la o supraproducție de ARNm și proteine corespunzătoare genelor amplificate, așa cum se arată mai jos. Liniile mâzgălite reprezintă ARNm care este produs prin transcrierea fiecărei copii a genei.
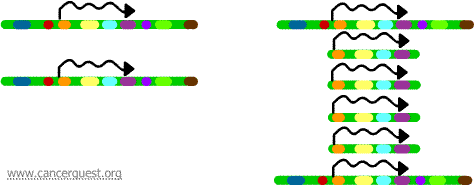
În timp ce acest proces nu este observat în celulele normale, el apare destul de des în celulele canceroase. Dacă o oncogenă este inclusă în regiunea amplificată, atunci supraexpresia rezultată a acelei gene poate duce la o creștere celulară dereglementată. Exemple în acest sens sunt amplificarea oncogenei myc într-o gamă largă de tumori și amplificarea oncogenei ErbB-2 sau HER-2/neu în cancerele mamare și ovariene. În cazul oncogenei HER-2/neu, tratamentele clinice au fost concepute pentru a viza celulele care supraexprimă produsul proteic.
Amplificarea genelor contribuie, de asemenea, la una dintre cele mai mari probleme în tratamentul cancerului: rezistența la medicamente. Tumorile rezistente la medicamente pot continua să crească și să se răspândească chiar și în prezența medicamentelor de chimioterapie. O genă frecvent implicată se numește MDR, pentru rezistență multiplă la medicamente. Produsul proteic al acestei gene acționează ca o pompă situată în membrana celulelor. Aceasta este capabilă să ejecteze selectiv moleculele din celulă, inclusiv medicamentele de chimioterapie. Această eliminare face ca medicamentele să devină ineficiente.
Acest lucru este discutat mai detaliat în secțiunea privind rezistența la medicamente. Amplificarea diferitelor gene poate face ca alte medicamente de chimioterapie să devină ineficiente.
Inversiuni, duplicații și deleții
Inversiuni
În aceste modificări, segmente de ADN sunt eliberate de pe un cromozom și apoi reintroduse în orientare opusă. Ca și în exemplele anterioare, această rearanjare poate duce la exprimarea anormală a unei gene, fie prin activarea unei oncogene, fie prin dezactivarea unei gene supresoare de tumori.
Duplicații/eliminări
Prin erori de replicare, o genă sau un grup de gene poate fi copiată de mai multe ori în cadrul unui cromozom. Acest lucru este diferit de amplificarea genelor prin faptul că genele nu sunt replicate în afara cromozomului și sunt copiate doar o singură dată în plus, nu de sute sau mii de ori. Genele pot fi, de asemenea, pierdute din cauza eșecului procesului de replicare sau a altor leziuni genetice.

Aneuploidie
Aneuploidie este modificarea genetică ce implică pierderea sau câștigarea de cromozomi întregi. Din cauza unor probleme în procesul de diviziune celulară, este posibil ca cromozomii replicați să nu se separe cu exactitate în celulele fiice. Acest lucru poate duce la celule care au prea mulți cromozomi sau prea puțini cromozomi. Un exemplu de afecțiune aneuploidă destul de frecventă care nu are legătură cu cancerul este sindromul Down, în care există o copie în plus a cromozomului 21 în toate celulele individului afectat.
În animația de mai jos, sunt realizate copii a doi cromozomi, dar când celula se divide, cromozomii nu sunt distribuiți în mod egal în cele două celule care se formează (celule fiice). Rezultatul este că una dintre celule are prea mulți cromozomi și una nu are suficienți.
Celele canceroase sunt foarte des aneuploide. Oamenii au în mod normal 46 de cromozomi în celulele lor, dar celulele canceroase au adesea mult mai mulți, uneori mai mult de100. Prezența cromozomilor în plus face ca celulele să fie instabile și perturbă grav controalele asupra diviziunii celulare. În prezent, există o dezbatere în curs de desfășurare cu privire la faptul dacă toate cancerele sunt sau nu aneuploide. Indiferent dacă acesta este cazul, este clar că aneuploidia este o caracteristică comună a celulelor canceroase.
Modificări epigenetice
În plus față de modificările reale ale secvenței ADN, expresia genelor poate fi modificată prin modificări ale ADN-ului și cromatinei care nu schimbă secvența. Deoarece aceste modificări nu modifică secvența ADN din gene, ele sunt denumite modificări epigenetice. Două tipuri de modificări epigenetice sunt descrise mai jos.
Metilarea
În această modificare, unele nucleotide din ADN sunt modificate prin adăugarea unei grupări metil (-CH3) la bază. Metilarea ADN-ului este asociată cu inactivarea acelei anumite regiuni de ADN. Modele anormale de metilare a ADN-ului au fost observate în celulele canceroase. Ca și modificările descrise, metilarea modifică expresia genelor afectate.
Acetilarea
În această modificare epigenetică, proteinele histonice în jurul cărora este înfășurat ADN-ul se modifică prin adăugarea de grupări acetil (-CH3CHO). Această alterare duce la o slăbire a interacțiunii ADN:histonă și este asociată cu o creștere a expresiei genice. Modificarea proceselor de adăugare și îndepărtare a grupărilor acetil la ADN este un domeniu activ de cercetare a tratamentului cancerului.
Mai multe despre modificările epigenetice și tratamentele împotriva cancerului.
Cauze ale mutației
După cum am văzut, celulele canceroase sunt create din celule precursoare normale prin intermediul unei acumulări de leziuni genetice. Mecanismele prin care sunt induse modificările sunt variate. În sens larg, agenții modificării genetice (mutației) se încadrează în principal în categoriile descrise mai jos și sunt discutate în profunzime în secțiunea următoare.
Mutații spontane
Mutații spontane: Bazele (A, T, G, C) din ADN sunt alterate sau pierdute din cauza unor erori de replicare nereparate sau a unor evenimente moleculare aleatorii. De exemplu, pierderea unei grupări amino din citosină, o bază normală care se găsește în ADN, duce la producerea de uracil, o bază care nu se găsește în mod normal în ADN. Dacă această modificare nu este detectată și inversată, se poate produce o mutație. Ocazional, o bază întreagă poate fi pierdută ca urmare a ruperii legăturii dintre coloana vertebrală a ADN-ului și bază. Acest lucru duce la un decalaj în dublul helix de ADN, care, dacă nu este reparat, poate duce la o mutație la următoarea copiere a ADN-ului (adică în timpul replicării).
Mutații induse
Mutații induse: Mutațiile pot fi induse prin expunerea organismelor (sau a celulelor) la o varietate de tratamente. Unele dintre cele mai frecvente sunt:
Radiații- Unul dintre primii mutageni cunoscuți, radiațiile sunt un puternic inductor de mutații. Diferite tipuri de radiații cauzează diferite tipuri de modificări genetice. Radiațiile ultraviolete (UV) provoacă mutații punctiforme. Razele X pot provoca rupturi în dublul helix de ADN și pot duce la translocații, inversiuni și alte tipuri de deteriorări ale cromozomilor. Expunerea la razele UV din lumina solară a fost legată de cancerul de piele. Rețineți că proprietățile nocive ale radiațiilor asupra ADN-ului au fost utilizate în mai multe tratamente diferite împotriva cancerului pe bază de radiații.
Descoperiți mai jos un tip de mutație care este cauzată de radiațiile ultraviolete. În acest exemplu, bombardarea dublei elice a ADN-ului de către razele UV face ca două baze să se unească. Acest lucru modifică structura ADN-ului și poate duce la modificări permanente dacă nu sunt reparate.
Un alt tip de radiație este energia emisă de elementele radioactive care apar în mod natural (cum ar fi radonul și uraniul) sau de surse create de om, cum ar fi cele găsite (și create) în reactoarele nucleare. Radiațiile de acest tip sunt de diferite tipuri și pot provoca diferite tipuri de daune celulelor și țesuturilor. Radiațiile pot deteriora direct ADN-ul sau pot provoca formarea de substanțe chimice (adică specii reactive de oxigen sau ROS) care pot deteriora apoi ADN-ul sau alte componente celulare.
Expunerea la radiații provenite din materiale radioactive a fost bine documentată. Analizele efectuate asupra supraviețuitorilor bombelor atomice lansate asupra Japoniei în timpul celui de-al Doilea Război Mondial au arătat creșteri mari ale leucemiilor la scurt timp după expunere și apoi creșteri ale altor tipuri de cancer în deceniile următoare.8
Cantități periculoase de materiale radioactive au fost, de asemenea, eliberate accidental de la centralele nucleare. Expunerea la radiații ca urmare a eliberării accidentale de materiale radioactive de la reactorul nuclear de la Cernobîl a fost asociată cu creșteri ale cancerului tiroidian și ale altor tipuri de cancer malign.9
Mașinile de imagistică medicală (cum ar fi aparatele cu raze X și scanerele CT) expun, de asemenea, pacienții la radiații. Cantitățile utilizate pentru un singur test nu sunt considerate a provoca cantități semnificative de cancer, dar impactul pe termen lung al mai multor teste pe o perioadă de ani nu este clar.10 De asemenea, nu se consideră că expunerea pasagerilor de avion la scanări corporale complete în aeroporturi prezintă un risc de cancer.11 Pasagerii care zboară cu avioanele sunt, de asemenea, expuși la radiații din spațiu, dar la un nivel scăzut și nu se crede că prezintă un risc de cancer, chiar și pentru membrii echipajului de zbor.1112
Mutageni chimici- Se știe că multe substanțe chimice diferite provoacă mutații. Aceste substanțe chimice își exercită efectul prin legarea la ADN sau la elementele constitutive ale ADN-ului și interferarea cu procesele de replicare sau de transcriere. Câteva exemple de mutageni puternici sunt benzo-a-pirenul, o substanță chimică care se găsește în fumul de țigară, și aflatoxina, un mutagen care se găsește cel mai adesea în produsele agricole depozitate necorespunzător.
Inflamația cronică- Inflamația cronică poate duce la deteriorarea ADN-ului din cauza producerii de substanțe chimice mutagene de către celulele sistemului imunitar. Un exemplu ar fi inflamația pe termen lung cauzată de infecția cu virusul hepatitei. Aflați mai multe despre viruși și cancer.
Radicalii de oxigen- În timpul captării energiei din alimente, care are loc în mitocondriile noastre, pot fi generate substanțe chimice care sunt foarte reactive și sunt capabile să deterioreze membranele celulare și ADN-ul însuși. Acești intermediari reactivi ai oxigenului (ROI) pot fi generați și prin expunerea celulelor la radiații, așa cum se arată mai jos.
Activitatea mutagenă a ROI este asociată cu dezvoltarea cancerului, precum și cu activitățile mai multor tratamente anticancerigene, inclusiv radiațiile și chimioterapia. 131415
Diviziune celulară anormală
În timpul mitozei, este posibil ca procesul de diviziune celulară să nu reușească să împartă cu exactitate cromozomii replicați în două celule fiice. O eroare de acest tip va duce la producerea de celule aneuploide. Celulele fie vor lipsi, fie vor fi câștigat un număr semnificativ de gene. Acest proces rar poate crea celule care sunt mai predispuse la diviziune celulară nereglementată. După cum s-a afirmat anterior, un mare procent din cancerele izolate de la oameni sunt aneuploide.
Dacă o celulă are o mutație într-o genă al cărei produs proteic este responsabil pentru „verificarea” procesului de diviziune, lucrurile pot scăpa rapid de sub control și celulele fiice ale fiecărei diviziuni pot deveni din ce în ce mai anormale.
Virusurile ca agenți mutageni
Se crede că virusurile sunt responsabile pentru un procent semnificativ de cazuri de cancer. Virusurile pot provoca cancer într-o varietate de moduri, iar modul în care acționează fiecare tip de virus este probabil să fie ușor diferit. Unele virusuri (inclusiv multe retrovirusuri) pot provoca mutații prin inserarea genelor lor în genomul celulei infectate. ADN-ul inserat poate distruge sau modifica activitatea genelor afectate.161718
Virusurile pot provoca, de asemenea, mutații în mod indirect. Ca un exemplu: O infecție cu virusul hepatitei poate dura mulți ani. În acest timp, sistemul de apărare al organismului încearcă să scape de virus prin producerea de substanțe chimice toxice. Aceste substanțe chimice pot provoca daune celulelor „trecătoare”, altfel sănătoase, trimițându-le pe drumul care duce la cancer. Există numeroase alte moduri în care virușii pot provoca cancer.1920
Din cauza importanței virușilor în dezvoltarea multor tipuri de cancer, am creat o secțiune dedicată virușilor și cancerului.
Transpozoni ca agenți mutageni
Transpozonii sunt secvențe scurte de ADN care au capacitatea de a se deplasa dintr-o locație în ADN în altă locație. Transpozonii codifică o enzimă, transpaza, care acționează pentru a îmbina transpozonul în noi locații într-un genom (a se vedea schema de mai jos, în stânga, a unui transpozon) Transpozonii au fost descoperiți de Barbara McClintock și a primit premiul Nobel pentru munca sa.2122 Genomul uman conține multe copii inactivate ale transpozonilor care și-au pierdut capacitatea de a se deplasa sau de a „sări” în noi locații. Aproximativ 50% din genomul uman este compus din transpozoni „morți”.23
Mișcarea transpozonilor activi poate duce la mutații, modificând activitatea genelor. Un exemplu vizibil de mișcare a transpozonilor (numită transpoziție), este colorarea boabelor la porumbul indian (vezi mai jos în dreapta). Se crede că transpozonii care sunt activi la om sunt implicați în bolile umane, inclusiv în cancer.242526


Rezumat al mutațiilor
Schimbare genetică (mutație) Introducere
- Comportamentele anormale demonstrate de celulele canceroase sunt rezultatul unei serii de mutații în genele de reglare cheie (de exemplu, genele de reparare a ADN-ului).
- Cele mai multe cancere se crede că apar dintr-o singură celulă precursoare care dobândește suficiente mutații pentru a deveni o celulă canceroasă.
Mutații ale ADN-ului
- Modificările genetice pot fi mici, afectând doar una sau câteva nucleotide (mutații punctiforme) sau pot fi destul de mari, modificând structura unui cromozom sau a unor cromozomi.
- Mutații punctiforme
- Translația este producerea unei proteine de către enzimele care „citesc” trei „cuvinte” de nucleotide (codoni) de-a lungul unui ARN mesager (ARNm).
- Chiar și schimbarea unei singure nucleotide de-a lungul ADN-ului unei gene poate duce la o proteină complet nefuncțională. Mutațiile sunt grupate în funcție de modificările pe care le creează în produsul proteic rezultat din gena afectată.
- Mutații nonsens – Noul codon (mutant) determină oprirea prematură a sintezei proteice.
- Mutații missens – Codonul modificat duce la inserția unui aminoacid incorect în proteină.
- Mutații frameshift – Pierderea sau câștigarea a 1 sau 2 nucleotide într-un ARNm determină citirea greșită a codonilor. Rezultă frecvent proteine scurtate și nefuncționale.
- Modificări la nivel de cromozom
- Translocații – Ruperea și (uneori) schimbul de fragmente de cromozomi.
- Amplificarea genelor – Replicarea anormală creează mai multe copii ale unei regiuni a unui cromozom. În cele din urmă, acest lucru duce la o supraproducție a proteinelor corespunzătoare.
- Inversiuni – Segmente de ADN sunt eliberate dintr-un cromozom și apoi reintroduse în orientarea opusă.
- Duplicări/Deleții – O genă sau un grup de gene pot fi pierdute cu totul sau copiate de mai multe ori în cadrul unui cromozom.
- Aneuploidie – O modificare genetică care implică pierderea sau câștigarea unor cromozomi întregi.
- Mutațiile spontane pot apărea din cauza ADN-ului nereparat sau a unor evenimente moleculare aleatorii.
- Aneuploidia este foarte frecventă în celulele canceroase.
Modificări epigenetice
- Expresia genică poate fi modificată prin modificări ale ADN-ului și ale cromatinei care nu schimbă secvența genetică. Exemplele includ metilarea ADN-ului și acetilarea histonelor.
- Metilarea – Unele nucleotide din ADN sunt modificate prin adăugarea unei grupări metil care este asociată cu inactivarea acelei regiuni de ADN
- Acetilarea – Adăugarea de grupări acetil slăbește ADN-ul și crește expresia genică.
Mutații induse
- Mutațiile pot fi induse prin expunerea organismelor (sau a celulelor) la o varietate de tratamente:
- Radiații – Razele UV provoacă mutații punctiforme, iar razele X provoacă multiple forme de deteriorare.
- Mutageni chimici – Se pot lega de ADN sau de elementele constitutive ale ADN-ului și pot interfera cu procesele de replicare sau de transcriere.
- Inflamație cronică – Leziuni ale ADN-ului datorate producției de substanțe chimice mutagene de către celulele sistemului imunitar
- Radicalii de oxigen – Rezultă din producția de energie a unei celule și pot deteriora ADN-ul.
Alte modificări genetice
- Diviziunea celulară aberantă care are ca rezultat diviziunea incorectă a cromozomilor poate duce la aneuploidie.
- Virusurile pot provoca leziuni genetice în mai multe moduri diferite și sunt asociate cu o gamă largă de cancere.
Mutații și cancer
- Se pare că tranziția de la o celulă normală, sănătoasă, la o celulă canceroasă este o progresie în trepte.
- Dezvoltarea cancerului necesită modificări genetice în mai multe oncogene diferite și supresori tumorali.
- Toate cancerele trebuie să depășească același spectru de funcții de reglementare pentru a se dezvolta și a progresa, dar genele implicate pot fi diferite.
- Eterogenitatea cancerului complică diagnosticul și tratamentul.
- Este posibil să moștenim gene disfuncționale care să conducă la dezvoltarea unei forme familiale a unui anumit tip de cancer.
Cunoaște fluxul: Mutația
Cunoaște fluxul este un joc interactiv prin care vă puteți testa cunoștințele. Pentru a juca:
- Trageți alegerile corespunzătoare din coloana din dreapta și plasați-le în ordine în căsuțele din stânga. Rețineți că veți folosi doar cinci din cele șase alegeri pentru a finaliza jocul.
- Când ați terminat, faceți clic pe „Verificare” pentru a vedea câte ați nimerit.
- Pentru răspunsurile incorecte, faceți clic pe „Descriere” pentru a revizui informațiile despre procese.
- Pentru a încerca din nou, alegeți „Resetare” și începeți din nou.
-
1
-
2
-
3
-
4
-
5
-
Aflați mai multeO celulă se află în procesul de sinteză a ADN-ului
-
Aflați mai multeSe realizează mai multe copii ale unei regiuni a unui cromozom
- .
Aflați mai multTranscrierea genelor amplificate
-
Aflați mai multTranscrierea genelor amplificate
-
Aflați mai multSupraproducția unei chei proteină duce la creșterea unei tumori rezistente la medicamente
-
Aflați mai multeSe produce duplicarea
Joacă din nou
- 1. Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). Campbell Biology (11th ed.). Pearson.
- 2. Surveillance, Epidemioloy, and End Results (SEER) reprezentat de National Cancer Institute
- 3. Hahn WC, Counter CM, Lundberg AS, Beijerbergen RL, Brooks MW, Weinberg RA. „Crearea de celule tumorale umane cu elemente genetice definite”. Nature 400: 464-468
- 4. Welch JS, Ley TJ, Ley TJ, Link DC, Westervelt P, Walter MJ, Graubert TA, DiPersio JF, Ding L, Mardis ER, Wilson RK et al. The origin and evolution of mutations in acute myeloid leukemia. Cell, 20 iulie 2012
- 5. 5. Brégeon D, Doetsch PW. Mutageneza transcripțională: cauze și implicare în dezvoltarea tumorilor. Nat Rev Cancer. 2011 Mar;11(3):218-27.
- 6. Nowell PC, Hungerford DA. „Chromosome studies on normal and leukemic human leukocytes”. J Natl Cancer Inst (1960). 25: 85-100.
- 7. Rowley JD. „O nouă anomalie cromozomială consistentă în leucemia mielogenă cronică identificată prin fluorescență cu chinacrină și colorație Giemsa”. Nature (1973). 243: 290-293.
- 8. Ozasa K, Shimizu Y, Sakata R, Sugiyama H, Grant EJ, Soda M, Kasagi F, Suyama A. RISCUL DE CANCER ȘI DE BOLI NON-CANCERICE LA SUPRAVIEȚUITORII LA BOMBĂ ATOMICĂ. Radiat Prot Dosimetry. 2011 Apr 18.
- 9. Cardis E, Hatch M. The Chernobyl accident–an epidemiological perspective. Clin Oncol (R Coll Radiol). 2011;23(4):251-260. doi:10.1016/j.clon.2011.01.510 9. Mar.
- 10. Fazel R, Krumholz HM, Wang Y, Ross JS, Chen J, Ting HH, Shah ND, Nasir K, Einstein AJ, Nallamothu BK. Expunerea la doze mici de radiații ionizante din procedurile de imagistică medicală. N Engl J Med. 2009 Aug 27;361(9):849-57.
- 11. a. b. Mehta P, Smith-Bindman R. Airport Full-Body Screening: Care este riscul? Arch Intern Med. 2011 Mar 28.
- 12. Bagshaw M. Radiațiile cosmice în aviația comercială. Travel Med Infect Dis. 2008 May;6(3):125-7. Epub 2007 Nov 26.
- 13. Kang DH. „Stresul oxidativ, deteriorarea ADN-ului și cancerul de sân”. AACN Clin Issues. (2002). 13:540-549
- 14. Athar M. „Oxidative stress and experimental carcinogenesis” (Stresul oxidativ și carcinogeneza experimentală). Indian J. Exp. Biol. (2002). 40:656-667
- 15. Marnett LJ. „Oxi-radicalii, peroxidarea lipidelor și deteriorarea ADN-ului”. (2002)181-182:219-222
- 16. Nair V. Oncogeneza indusă de retrovirusuri și siguranța vectorilor retrovirali. Curr Opin Mol Ther. 2008 Oct;10(5):431-8.
- 17. Brady G, Macarthur GJ, Farrell PJ. Virusul Epstein-Barr și limfomul Burkitt. Postgrad Med J. 2008 Jul;84(993):372-7.
- 18. Ruprecht K, Mayer J, Sauter M, Roemer K, Mueller-Lantzsch N. Endogenous retroviruses and cancer. Cell Mol Life Sci. 2008 Nov;65(21):3366-82.
- 19. Lupberger J, Hildt E. Hepatitis B virus-induced oncogenesis. World J Gastroenterol. 2007 Jan 7;13(1):74-81.
- 20. Castello G, Scala S, Palmieri G, Curley SA, Izzo F. HCV-related hepatocellular carcinoma: De la inflamația cronică la cancer. Clin Immunol. 2010 Mar;134(3):237-50. Epub 2009 Nov 11.
- 21. McClintock B. Originea și comportamentul locilor mutabile în porumb. Proc Natl Acad Sci U S A. 1950 Jun;36(6):344-55.
- 22. McClintock, Barbara Prelegere de acordare a Premiului Nobel
- 23. Burns KH, Boeke JD. Tectonica transpozonilor umani. Cell. 2012 May 11;149(4):740-52.
- 24. Kozeretska IA, Demydov SV, Ostapchenko LI. Elemente genetice mobile și cancer. De la mutații la terapia genică. Exp Oncol. 2011 Dec;33(4):198-205.
- 25. Solyom S, Kazazian HH Jr. Elemente mobile în genomul uman: implicații pentru boli. Genome Med. 2012 Feb 24;4(2):12.
- 26. Iskow RC, McCabe MT, Mills RE, Torene S, Pittard WS, Neuwald AF, Van Meir EG, Vertino PM, Devine SE. Mutageneza naturală a genomurilor umane de către retrotranspozoni endogeni. Cell. 2010 Jun 25;141(7):1253-61.