US Pharm. 2018;43(12):HS-2-HS-6.
ABSTRACT: Las hemorragias gastrointestinales (SGI) son una fuente importante de hospitalizaciones en los Estados Unidos. Las hemorragias gastrointestinales se clasifican en dos tipos: hemorragias digestivas altas y hemorragias digestivas bajas. Cada tipo puede presentarse de forma distinta y requiere un tratamiento diferente. Las hemorragias digestivas altas dependen de la terapia endoscópica y pueden beneficiarse de varios tratamientos farmacológicos en situaciones específicas, como los inhibidores de la bomba de protones y los macrólidos. El manejo de la GIB inferior se centra en la colonoscopia y en el tratamiento mecánico de las hemorragias, con poca intervención farmacológica. Los farmacéuticos pueden prestar un servicio eficaz a estos pacientes en múltiples puntos de atención al paciente.
La hemorragia gastrointestinal (GIB) es un problema médico relativamente frecuente, que causa una parte importante de la morbilidad, las hospitalizaciones e incluso la mortalidad anual en los Estados Unidos. La tasa bruta estimada de hospitalizaciones secundarias a cualquier tipo de GIB en los EE.UU. se calcula en unos 375 por cada 100.000 al año.1-3 En el caso de los eventos agudos de GIB, algunos estudios identifican una tasa de mortalidad a los 30 días de hasta el 14%, mientras que otros informan de un rango entre el 6% y el 10% al año, con tasas que aumentan en pacientes con edad avanzada y un mayor número de comorbilidades subyacentes asociadas.4-7 Se calcula que cada año se gastan más de 2.500 millones de dólares en el tratamiento hospitalario del GIB.8
Dada la naturaleza del GIB, es importante diferenciar el estado de la enfermedad, ya que la localización de la hemorragia puede dictar tanto la presentación como el tratamiento (TABLAS 1-3). Históricamente, la distinción entre GIB superior (UGIB) y GIB inferior (LGIB) se basaba en la localización de la hemorragia en relación con el ligamento de Treitz.9,10 Con esta definición, la hemorragia proximal al ligamento de Treitz se clasifica como UGIB, mientras que la hemorragia distal al ligamento de Treitz se clasifica como LGIB. Aunque existen otras definiciones en la literatura, esta definición es la que se ha establecido en la mayor parte de la práctica.11,12



En el momento de la presentación, la evaluación de cualquier sospecha de GIB es inicialmente similar, independientemente del origen de la hemorragia. La evaluación inmediata debe centrarse en la estabilidad hemodinámica del paciente. Esta prioridad ha sido bien establecida en otros modelos hemorrágicos y sigue siendo válida en los casos de GIB.16-18 Debe realizarse una evaluación física de la presión arterial, la frecuencia cardíaca y el estado ortostático, y se debe proporcionar reanimación según corresponda. Esta reanimación debe comenzar con fluidos intravenosos, pero también puede requerir transfusiones de concentrados de glóbulos rojos.
La evaluación adicional de los pacientes que presentan una GIB debe incluir una historia clínica centrada en la identificación de la naturaleza, la duración y el posible origen de la hemorragia, así como pruebas de laboratorio (CBC, BMP, estudios de coagulación).17,18 Al evaluar a estos pacientes desde el punto de vista del farmacéutico, es importante tener en cuenta cualquier uso actual o reciente de medicamentos que pueda aumentar el riesgo de hemorragia, incluidos agentes como antiinflamatorios no esteroideos, antiagregantes plaquetarios y/o anticoagulantes. La identificación temprana de estos factores puede ayudar a acelerar tanto el diagnóstico como la respuesta terapéutica adecuada.
La evaluación y estratificación del riesgo es clínicamente útil para ayudar a distinguir a los pacientes con alto y bajo riesgo de resultados adversos.17,18 Al estratificar a los pacientes en grupos de riesgo evaluados, se puede tomar una decisión inicial informada. En concreto, la estratificación puede proporcionar información sobre factores como el momento de la endoscopia o la colonoscopia, el nivel de atención necesario y el momento del alta. Existen varias herramientas establecidas para ayudar en la evaluación del riesgo individual.
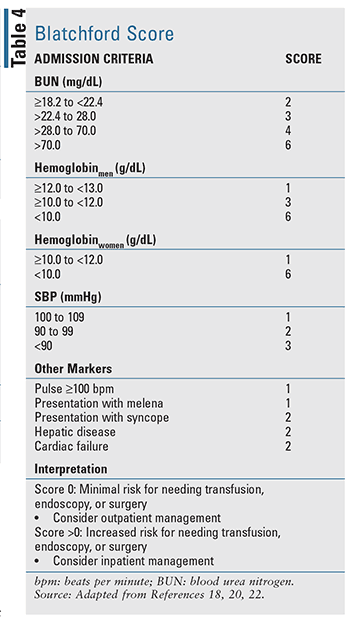
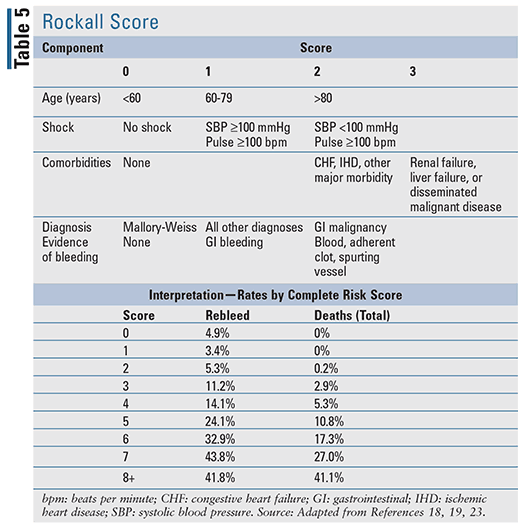
Para los pacientes con UGIB aguda, existen varias herramientas de predicción clínica que se han desarrollado, incluyendo dos herramientas bien evaluadas y citadas en las guías basadas en la evidencia: la puntuación de Blatchford (TABLA 4) y la puntuación de Rockall (TABLA 5).17-20 La puntuación de Rockall utiliza datos clínicos inmediatamente en el momento de la presentación.19 Los factores que evalúan la gravedad de la hemorragia, como la presión arterial sistólica y la frecuencia cardíaca, se evalúan junto con las características del paciente, como la edad y las enfermedades comórbidas, lo que da lugar a una herramienta para evaluar los resultados pronósticos y potencialmente la mortalidad. Del mismo modo, la puntuación de Blatchford utiliza datos clínicos y de laboratorio para ayudar a predecir el riesgo de intervención y la mortalidad.20 En el caso del LGIB agudo, las reglas pronósticas disponibles para evaluar el riesgo son limitadas y están menos validadas en comparación con el UGIB.22
Farmacología de la hemorragia digestiva alta
Los inhibidores de la bomba de protones (IBP) son la clase de fármacos más asociada al tratamiento del UGIB. En un paciente con UGIB, el ácido gástrico puede inhibir la agregación plaquetaria y debilitar la coagulación potencial, lo que conduce a una alteración de la interrupción de la hemorragia. Para inhibir este proceso, la inhibición de la secreción de ácido gástrico destinada a elevar el pH del estómago a 6 o más puede ayudar a estabilizar los coágulos y mejorar los resultados clínicos.24
Los IPP son únicos en el sentido de que tienen una aplicación potencial tanto antes como después de la endoscopia. En el contexto de la preendoscopia, las directrices no forman consenso sobre su uso, pero pueden disminuir la proporción de pacientes con alto riesgo de estigmatización de la hemorragia en el momento del procedimiento.25 A pesar del beneficio potencial en esta población, la evidencia sugiere que el uso de los IBP no afecta a las nuevas hemorragias, a la cirugía necesaria o a la mortalidad, lo que lleva a cierta controversia clínica respecto a su aplicación. Sin embargo, los pacientes en los que no se puede realizar una endoscopia o ésta se retrasa han demostrado una posible disminución del riesgo de resangrado mediante la utilización de IBP. Las pruebas sugieren que los IBP disminuyen la incidencia de los estigmas de alto riesgo de hemorragia en el momento de la endoscopia, pero no afectan a las nuevas hemorragias, a la necesidad de cirugía ni a la mortalidad.17,26 Tras el tratamiento endoscópico, los IBP pueden utilizarse tanto de forma aguda como crónica.17
Infusión continua frente a IBP intermitente
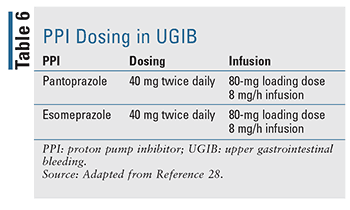
La dosis y la administración adecuadas de los IBP se han evaluado detenidamente en los últimos años (TABLA 6). Una dosis IV en bolo seguida de infusión fue durante mucho tiempo el curso normal de la terapia y sigue siendo el tratamiento de elección en las directrices actualmente disponibles, pero los datos sugieren que la dosis en bolo IV dos veces al día no es inferior en los resultados de resangrado, mortalidad y duración de la estancia hospitalaria.17,27 La literatura reciente ha demostrado que el uso intermitente de IBP no fue inferior y ofrece un claro beneficio en la dosis del fármaco, el coste y la utilización de recursos. Los autores sugieren que se actualicen las directrices para recomendar el tratamiento intermitente con IBP en la GIB tratada por vía endoscópica.27 En la práctica, muchas instituciones favorecen ahora la dosificación intermitente con el fin de disminuir el uso de recursos y el coste global.
IBP intravenoso frente a antagonistas H2 intravenosos
Considerando que los antagonistas H2 (H2A) se utilizan con una intención similar en otros estados de enfermedad, su uso en la UGIB se ha investigado junto con los IBP. Un metaanálisis de 2015 que evaluó las dos clases en el contexto de la UGIB descubrió que, si bien la diferencia en la mortalidad no era significativa, los resultados como la tasa de hemorragias recurrentes y la tasa de recepción de cirugía mostraban un claro beneficio en los IBP. Este déficit se debe probablemente a la inferioridad de los H2A a la hora de mantener el pH gástrico por encima de 6,0, el pH aproximado en el que pueden funcionar los procesos de coagulación.29
Macrólidos
En un esfuerzo por mejorar la visualización durante la endoscopia y disminuir así la necesidad de repetir la endoscopia, se suele utilizar la eritromicina IV, un macrólido antimicrobiano que también actúa como agente procinético. Una dosis única de 250 mg o 3 mg/kg es generalmente bien tolerada.17,30 Un meta-análisis de 2016 concluyó que el uso de eritromicina antes de la endoscopia disminuyó significativamente la necesidad de una segunda endoscopia y la duración de la estancia hospitalaria, y por lo tanto lleva una recomendación para ser utilizado en las directrices de la Sociedad Europea de Endoscopia Gastrointestinal.30,31
Es justo preguntarse si el posible beneficio es un efecto de clase o específico de la eritromicina. Se ha evaluado la azitromicina, un macrólido generalmente más utilizado, y parece ser una alternativa no inferior a la eritromicina. La azitromicina puede conllevar algunas ventajas logísticas, como no requerir reconstitución y, en general, una mayor disponibilidad debido a su uso en el tratamiento empírico de la neumonía.32
Tratamiento de H pylori
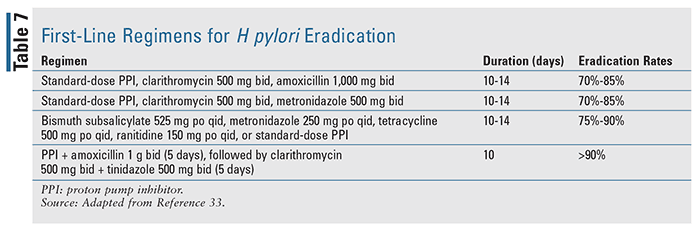
Los pacientes diagnosticados de hemorragia asociada a la infección por Helicobacter pylori deben ser tratados mediante una terapia de erradicación basada en las directrices, con el objetivo de lograr la resolución completa de la infección.17 La bibliografía disponible indica que la erradicación de H pylori es significativamente más eficaz que el tratamiento antisecretor solo en pacientes con UGIB. Los regímenes de primera línea para la erradicación de H pylori se detallan en la TABLA 7, basados en las directrices del Colegio Americano de Gastroenterología sobre el manejo de la infección por H pylori.33 Una vez resuelta la infección, este grupo de pacientes no suele necesitar recibir tratamiento antisecretor de mantenimiento, a menos que requieran antiinflamatorios no esteroideos o terapia antitrombótica, con los que es necesario un tratamiento antisecretor a largo plazo, ya que su uso puede aumentar significativamente el riesgo de resangrado.17,18
Resumen del tratamiento
Después de la evaluación inicial y la estratificación del riesgo y una vez que el paciente está hemodinámicamente estable, la colonoscopia precedida de la limpieza del colon es el procedimiento de diagnóstico inicial para la mayoría de los pacientes que presentan un LGIB.21 El manejo del LGIB incluye principalmente intervenciones no farmacológicas; sin embargo, todavía hay oportunidades para que los farmacéuticos participen en el cuidado de los pacientes.
Aplicación de IBP en el LGIB
A diferencia del UGIB, la literatura disponible que evalúa el uso de IBP en el LGIB no muestra beneficios. Los ensayos que evalúan el UGIB y el LGIB han demostrado que, si bien los IBP no demuestran una mejora de los resultados en el LGIB, en realidad pueden aumentar el riesgo de LGIB.34 Los mecanismos teóricos de este aumento del riesgo se centran a menudo en posibles cambios en la microbiota, y por lo tanto pueden potenciar el posible riesgo de los AINE. Estos resultados han resultado controvertidos; sin embargo, ofrecen pruebas de que los pacientes con LGIB no se benefician del tratamiento con IBP. Este riesgo potencial debe evaluarse cuidadosamente en los pacientes, en particular en aquellos con riesgo de UGIB, ya que puede ser necesario evaluar cuidadosamente el riesgo frente al beneficio.34
El papel del farmacéutico
Los farmacéuticos de muchas especialidades están en una posición única para ayudar en el tratamiento y manejo de los pacientes con GIB. Los farmacéuticos ambulatorios están en una posición privilegiada para vigilar de forma proactiva los posibles factores de riesgo en los pacientes, incluyendo las altas dosis de AINE y anticoagulantes, y reducir la posibilidad de GIB en primera línea. Además, pueden proporcionar un importante asesoramiento y optimización de la dosis para los pacientes tanto antes como después de un diagnóstico de GIB. Del mismo modo, los farmacéuticos clínicos de hospitalización también pueden desempeñar un papel importante en el tratamiento de la GIB. Pueden estar en posición de ayudar en múltiples áreas durante la evaluación inicial y el manejo. La conciliación inicial de la medicación puede revelar detalles relevantes para el diagnóstico y el tratamiento de los pacientes, como la identificación del uso de AINE o anticoagulantes por parte de los pacientes externos. Los farmacéuticos también pueden proporcionar recomendaciones al equipo sanitario sobre qué medicamentos pueden aportar beneficios a cada caso de GIB.
1. El-Tawil A. Tendencias sobre la hemorragia gastrointestinal y la mortalidad: ¿dónde estamos parados? World J Gastroenterol. 2012;18(11):1154-1158.
2. Zhao Y, Encinosa W. Hospitalizaciones por hemorragia gastrointestinal en 1998 y 2006. Statistical Brief #65. Healthcare Cost and Utilization Project (HCUP) statistical briefs. December 2008.
3. Whelan CT, Chen C, Kaboli P, et al. Upper versus lower gastrointestinal bleeding: a direct comparison of clinical presentation, outcomes, and resource utilization. J Hosp Med. 2010;5(3):141-147.
4. Wilcox CM, Cryer BL, Henk HJ, et al. Mortalidad asociada a eventos de hemorragia gastrointestinal: comparación de los resultados clínicos a corto plazo de los pacientes hospitalizados por hemorragia gastrointestinal superior e infarto agudo de miocardio en un entorno de atención administrada de EE.UU. Clin Exp Gastroenterol. 2009;2:21-30.
5. García Rodríguez LA, Ruigómez A, Hasselgren G, et al. Comparación de la mortalidad por hemorragia por úlcera péptica entre pacientes con o sin antecedentes de úlcera péptica. Epidemiología. 1998;9(4):452-456.
6. Wilcox CM, Clark WS. Causas y resultados de la hemorragia gastrointestinal superior e inferior: la experiencia del Hospital Grady. South Med J. 1999;92:44-50.
7. Yavorski RT, Wong RK, Maydonovitch C, et al. Analysis of 3,294 cases of upper gastrointestinal bleeding in military medical facilities. Am J Gastroenterol. 1995;90:568-573.
8. Johanson JF. Frenando los costes de las hemorragias gastrointestinales. Am J Gastroenterol. 1998;93:1384-1385.
9. Red Escocesa de Directrices Intercolegiales (SIGN). Manejo de la hemorragia gastrointestinal aguda superior e inferior. September 2008. www.sign.ac.uk/assets/sign105.pdf.
10. Kim, SK, Cho CD, Wojtowycz AR. The ligament of Treitz (the suspensory ligament of the duodenum): anatomic and radiographic correlation. Abdom Imaging. 2008;33:395-397.
11. Matthew B, et al. Diagnosis of gastrointestinal bleeding: a practical guide for clinicians. World J Gastrointest Pathophysiol. 2014;5(4):467-478.
12. Raju GS, et al. Declaración de posición médica del Instituto de la Asociación Americana de Gastroenterología (AGA) sobre la hemorragia gastrointestinal oscura. Gastroenterology. 2007;133(5):1694-1696.
13. Tielleman T, Bujanda D, Cryer B, et al. Epidemiología y factores de riesgo de la hemorragia digestiva alta. Gastrointest Endosc Clin N Am. 2015;25(3):415-428.
14. Rodríguez-Hernández H, Rodríguez-Morán M, González JL, et al. Factores de riesgo asociados a la hemorragia digestiva alta y a la mortalidad. Rev Med Inst Mex Seguro Soc. 2009;47(2):179-184.
15. Strate L. Hemorragia digestiva baja: epidemiología y diagnóstico. Gastroenterol Clin North Am. 2005;34(4):643-664.
16. Cocchi MN, Kimlin E, Walsh M, et al. Identificación y reanimación del paciente traumatizado en shock. Emerg Med Clin N Am. 2007;25:623-642.
17. Laine L, Jensen DM. Manejo de pacientes con hemorragia ulcerosa. Am J Gastroenterol. 2012;107:345-360.
18. Siau K, Chapman W, Sharma N, et alManagement of acute upper gastrointestinal bleeding: an update for the general physician. J R Coll Physicians Edinb. 2017;47:218-230.
19. Rockall T, Logan R, Devlin H, et al.Evaluación del riesgo tras una hemorragia gastrointestinal superior aguda. Gut. 1996;38:316-321.
20. Blatchford O, Murray W, Blatchford M. A risk score to predict need for treatment for uppergastrointestinal haemorrhage. Lancet. 2000;356:1318-1321.
21. Recio-Ramírez, JM, Sánchez-Sánchez Mdel P, Peña-Ojeda JA, et al. Capacidad predictiva de la puntuación de Glasgow-Blatchford para la estratificación del riesgo de hemorragia digestiva alta en un servicio de urgencias. Revista Española de Enfermedades Digestivas. 2015;107(5):262-267.
22. Strate L, Grainek IM. Guía clínica del ACG: Manejo de pacientes con hemorragia digestiva baja aguda. Am J Gastroenterol. Publicación anticipada en línea 1 de marzo de 2016. 2016;111:459-474.
23. Bessa X, O’Callaghan E, Balleste B, et al. Aplicabilidad de la puntuación Rockall en pacientes sometidos a terapia endoscópica por hemorragia gastrointestinal superior. Dig Liver Dis. 2006;38:12-17.
24. Chaimoff C, Creter D, Djaldetti M. The effect of pH on platelet and coagulation factor activities. Am J Surg. 1978;136(2):257-259.
25. Sreedharan A, Martin J, Leontiadis GI, et al. Tratamiento con inhibidores de la bomba de protones iniciado antes del diagnóstico endoscópico en la hemorragia digestiva alta. Cochrane Database Syst Rev. 2010(7):CD005415.
26. Leontiadis GI , Sharma VK , Howden CW. Tratamiento con inhibidores de la bomba de protones para la hemorragia por úlcera péptica: Colaboración Cochrane meta-análisis de ensayos controlados aleatorios. Mayo Clin Proc. 2007;82:286-296.
27. Sachar H, Vaidya K, Laine L, et al. Tratamiento con inhibidores de la bomba de protones intermitente frente a continuo para las úlceras sangrantes de alto riesgo: una revisión sistemática y metaanálisis. JAMA Intern Med. 2014;174(11):1755-1762.
28. Cheng H, Sheu B. Inhibidores de la bomba de protones intravenosos para la hemorragia por úlcera péptica: beneficios y límites clínicos. World J Gastrointest Endosc. 2011;3(3):49-56.
29. Zhang YS, Li Q, He BS, et al. Tratamiento con inhibidores de la bomba de protones frente a tratamiento con antagonistas de los receptores H2 para la hemorragia gastrointestinal superior después de la endoscopia: un metaanálisis. World J Gastroenterol. 2015;21(20):6341-6351.
30. Rahman R, Nguyen D, Sohail U, et al. Administración de eritromicina preendoscópica en la hemorragia gastrointestinal superior: un meta-análisis actualizado y una revisión sistemática. Ann Gastroenterol. 2016,29:312-317.
31. Gralnek IM, Dumonceau JM, Kuipers EJ, et al. Diagnóstico y manejo de la hemorragia gastrointestinal superior no variceal: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy. 2015;47:1-46.
32. Issa D, Solomon S, Di Pace B, et al. Comparación de las infusiones de azitromicina con las de eritromicina en la mejora de la visualización de la endoscopia para la hemorragia gastrointestinal superior. Congreso Mundial en ACG2017. Sesión 2A.
33. Chey WD, Wong BC. Comité de Parámetros de Práctica del Colegio Americano de Gastroenterología. Guía del Colegio Americano de Gastroenterología sobre el manejo de la infección por Helicobacter pylori. Am J Gastroenterol. 2007; 102:1808-1825.
34. Luée A, Lanas A. Protons pump inhibitor treatment and lower gastrointestinal bleeding: balancing risks and benefits. World J Gastroenterol. 2016;22(48):10477-10481.