Oxidos de amina y la eliminación de Cope
Los óxidos de amina se preparan oxidando 3º-aminas o piridinas con peróxido de hidrógeno o perácidos (e.p. ej. ZOOH, donde Z=H o acil).
\NLos óxidos de amina son bases relativamente débiles, pKa aprox. 4,5, en comparación con la amina madre. La función covalente coordinada N-O es polar, siendo el oxígeno un potente aceptor de enlaces de hidrógeno. Si uno de los sustituyentes alquílicos consiste en una cadena larga, como C12H25, el óxido de amina resultante es un surfactante anfótero y se utiliza en champús y otros agentes de limpieza suaves.
Una reacción de eliminación, complementaria a la eliminación de Hofmann, se produce cuando los óxidos de 3º-amina se calientan a temperaturas de 150 a 200 ºC. Esta reacción se conoce como eliminación de Cope. Se suele llevar a cabo mediante la adición gota a gota de una solución de óxido de amina a un tubo calentado lleno de pequeñas perlas de vidrio. Una corriente de gas nitrógeno que fluye a través de la columna transporta los productos volátiles de alqueno a un receptor refrigerado. El producto que contiene nitrógeno es una amina hidroxilada. A diferencia de la eliminación de Hofmann, esta reacción tiene lugar mediante una reorganización cíclica concertada, como se muestra en el siguiente diagrama. Para tal mecanismo, los grupos beta-hidrógeno y óxido de amina tienen necesariamente una relación sincrónica.
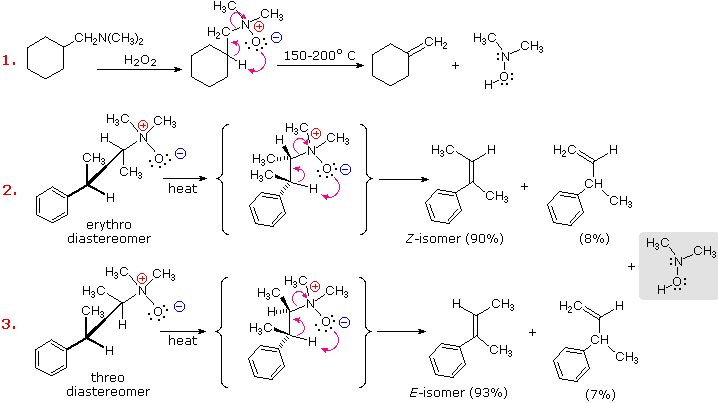
La eliminación de óxidos de amina diastereoméricos, como los mostrados en los ejemplos #2 & 3 anteriores, proporcionan una prueba de la relación sincrónica de los grupos beta-hidrógeno y óxido de amina. Estos ejemplos también demuestran una fuerte regioselectividad que favorece el doble enlace más estable.
Sineliminaciones pirolíticas
Los óxidos de amina no son las únicas funciones que experimentan una sineliminación unimolecular al calentarse. Para ver ejemplos de otros casos, haga clic aquí