US Pharm. 2018;43(12):HS-2-HS-6.
ABSTRACT: Gastrointestinala blödningar (GIB) är en betydande källa till sjukhusinläggningar i USA. GIBs kategoriseras i två typer: övre gastrointestinala blödningar och nedre gastrointestinala blödningar. Varje typ kan uppvisa olika kännetecken och kräva olika behandling. Övre GIB är beroende av endoskopisk behandling och kan gynnas av olika farmakologiska behandlingar i specifika scenarier, t.ex. protonpumpshämmare och makrolider. Behandlingen av nedre GIB är inriktad på koloskopi och mekanisk behandling av blödningar, med liten farmakologisk intervention. Apotekare kan ge effektiv service till dessa patienter på flera ställen i patientvården.
Gastrointestinala blödningar (GIB) är ett relativt vanligt medicinskt problem som orsakar en betydande del av morbiditet, sjukhusvistelser och även dödlighet årligen i USA. Den obearbetade uppskattade sjukhusvistelsen sekundärt till någon typ av GIB i USA uppskattas till cirka 375 per 100 000 per år.1-3 För akuta GIB-händelser identifierar vissa studier en 30-dagarsdödlighet som är så hög som 14 %, medan andra rapporterar ett intervall på mellan 6 % och 10 % per år, med en ökning hos patienter med stigande ålder och ett högre antal associerade underliggande komorbiditeter.4-7 Det uppskattas att mer än 2,5 miljarder dollar spenderas årligen för vård av GIB i slutenvården.8
Med tanke på GIB:s karaktär är det viktigt att differentiera sjukdomstillståndet, eftersom blödningens placering kan diktera både presentation och behandling (TABELLER 1-3). Historiskt sett har distinktionen mellan övre GIB (UGIB)och nedre GIB (LGIB) baserats på blödningens placering i förhållande till Treitz ligament.9,10 Med denna definition kategoriseras blödning proximalt till Treitz ligament som en UGIB, medan blödning distalt till Treitz ligament kategoriseras som en LGIB. Även om det finns andra definitioner i viss litteratur är denna definition allmänt etablerad i de flesta praxis.11,12



Vid presentationen är utredningen av alla misstänkta GIB inledningsvis likartad, oavsett ursprunget till blödningen. Omedelbar utvärdering bör fokusera på patientens hemodynamiska stabilitet. Denna prioritering har fastställts väl i andra hemorragiska modeller och gäller även i fall av GIB.16-18 Fysisk bedömning av blodtryck, hjärtfrekvens och ortostatiskt status ska utföras och återupplivning ska ges vid behov. Denna återupplivning bör börja med intravenösa vätskor men kan också kräva transfusioner av packade röda blodkroppar.
Den ytterligare bedömningen av patienter som presenteras med GIB bör innefatta en fokuserad anamnes som syftar till att identifiera blödningens art, varaktighet och potentiella källa samt laboratorietester (CBC, BMP, koagulationsstudier).17,18 När man utvärderar dessa patienter ur ett apoteksperspektiv är det viktigt att notera eventuell aktuell eller nyligen genomförd läkemedelsanvändning som kan öka risken för blödning, inklusive medel som icke-steroida antiinflammatoriska läkemedel, trombocythämmande medel och/eller antikoagulantia. Tidig identifiering av dessa faktorer kan bidra till att påskynda både diagnos och lämpligt behandlingssvar.
Riskbedömning och riskstratifiering är kliniskt användbart för att hjälpa till att särskilja patienter med hög och låg risk för ogynnsamma utfall.17,18 Genom att stratifiera patienterna i utvärderade riskgrupper kan ett initialt informerat beslutsfattande göras. Särskilt kan stratifiering ge insikt i faktorer som tidpunkt för endoskopi eller koloskopi, nödvändig vårdnivå och tidpunkt för utskrivning. Olika etablerade verktyg finns tillgängliga för att underlätta bedömningen av individuell risk.
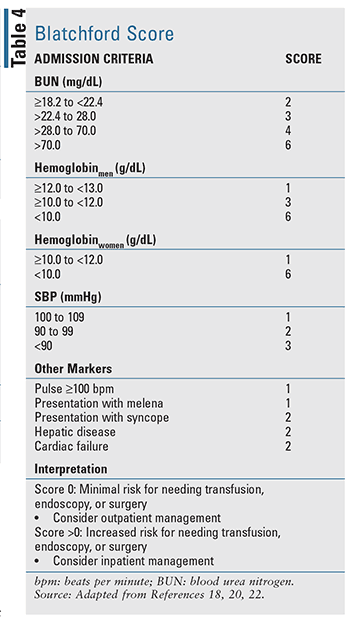
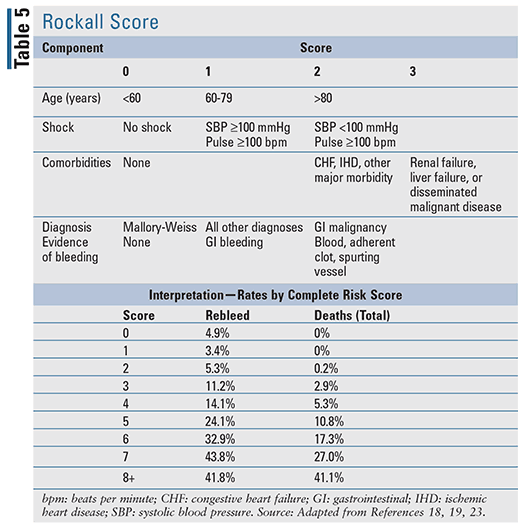
För patienter med akut UGIB finns det flera kliniska prediktionsverktyg som har utvecklats, inklusive två väl utvärderade verktyg som citeras i evidensbaserade riktlinjer: Blatchford-poängen (TABELL 4) och Rockall-poängen (TABELL 5).17-20 Rockall-poängen använder sig av kliniska data omedelbart vid presentationen.19 Faktorer som bedömer blödningens svårighetsgrad, t.ex. systoliskt blodtryck och hjärtfrekvens, bedöms tillsammans med patientens egenskaper, t.ex. ålder och komorbiditet, vilket resulterar i ett verktyg för att bedöma prognostiska resultat och potentiellt dödlighet. På liknande sätt använder Blatchford-poängen både kliniska och laboratoriedata för att hjälpa till att förutsäga risken för ingrepp och mortalitet.20 För akut LGIB är de tillgängliga prognostiska reglerna för att bedöma risken begränsade och mindre validerade jämfört med UGIB.22
Farmakoterapi vid övre gastrointestinala blödningar
Protonpumpsinhibitorer (PPI) är den läkemedelskategori som är mest associerad med behandling av UGIB. Hos en UGIB-patient kan magsyra hämma trombocytaggregationen och försvaga den potentiella koagulationen, vilket leder till en försämring av blödningsstoppet. För att hämma denna process kan en hämning av magsyrasekretionen avsedd att höja pH-värdet i magsäcken till 6 eller högre bidra till att stabilisera blodproppar och förbättra de kliniska resultaten.24
PPI:er är unika i det avseendet att de har en potentiell tillämpning både före och efter endoskopi. När det gäller preendoskopi råder det inte konsensus i riktlinjerna om deras användning, men de kan minska andelen patienter med hög risk för stigmata för blödning vid tidpunkten för ingreppet.25 Trots potentiella fördelar i denna population tyder bevisen på att användning av PPI inte påverkar återblödning, nödvändig kirurgi eller mortalitet, vilket leder till en viss klinisk kontrovers när det gäller deras tillämpning. Patienter för vilka endoskopi inte kan utföras eller kommer att fördröjas har dock visat på en potentiell minskning av risken för återblödning genom användning av PPI. Det finns belägg för att PPI minskar förekomsten av högriskstigmata för blödning vid tidpunkten för endoskopi men påverkar inte återblödning, nödvändig kirurgi eller mortalitet.17,26 Efter endoskopisk behandling kan PPI användas både akut och kroniskt.17
Kontinuerlig infusion kontra intermittent PPI
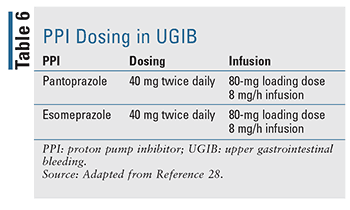
Passande dosering och administrering av PPI har utvärderats noggrant under de senaste åren (TABELL 6). En bolus IV-dos följt av infusion var länge det normala behandlingsförloppet och förblir den vanligaste behandlingen i nu tillgängliga riktlinjer, men data tyder på att två gånger daglig IV-bolusdosering inte är bättre när det gäller utfallet av återblödning, mortalitet och sjukhusvistelsens längd.17,27 I den senaste litteraturen har det visat sig att intermittent PPI-användning inte var sämre och ger en klar fördel när det gäller läkemedelsdos, kostnad och resursutnyttjande. Författarna föreslår att att riktlinjerna uppdateras för att rekommendera intermittent PPI-behandling vid endoskopiskt behandlad GIB.27 I praktiken föredrar många institutioner nu intermittent dosering för att minska resursanvändningen och den totala kostnaden.
Intravenösa PPI kontra intravenösa H2-antagonister
Med tanke på att H2-antagonister (H2A) används med liknande syfte vid andra sjukdomstillstånd har deras användning vid UGIB undersökts vid sidan av PPI. En metaanalys från 2015 som utvärderade de två klasserna i samband med UGIB fann att medan skillnaden i mortalitet befanns vara icke-signifikant, visade utfall som återkommande blödningsfrekvens och frekvensen av mottagande av kirurgi tydliga fördelar för PPI:er. Detta underskott beror sannolikt på H2As underlägsenhet när det gäller att upprätthålla magens pH över 6,0, det ungefärliga pH där koagulationsprocesser kan fungera.29
Makrolider
I ett försök att förbättra visualiseringen under endoskopi och därmed minska behovet av upprepad endoskopi används vanligen intravenöst erytromycin, en antimikrobiell makrolid som också fungerar som ett prokinetiskt medel. En engångsdos på 250 mg eller 3 mg/kg tolereras i allmänhet väl.17,30 I en metaanalys från 2016 drogs slutsatsen att användning av erytromycin före endoskopi signifikant minskade behovet av andrahandsendoskopi och längden på sjukhusvistelsen, och därför har det en rekommendation om att användas i riktlinjerna från European Society of Gastrointestinal Endoscopy.30,31
Det är rimligt att fråga sig om den eventuella fördelen är en klass-effekt eller specifik för erytromycin. Azitromycin, en generellt sett mer vanligt förekommande makrolid, har utvärderats och tycks vara ett icke underlägset alternativ till erytromycin. Azitromycin kan ha vissa logistiska fördelar, t.ex. att det inte kräver rekonstitution och att det generellt sett är mer tillgängligt på grund av att det används vid empirisk behandling av lunginflammation. 32
H pylori-behandling
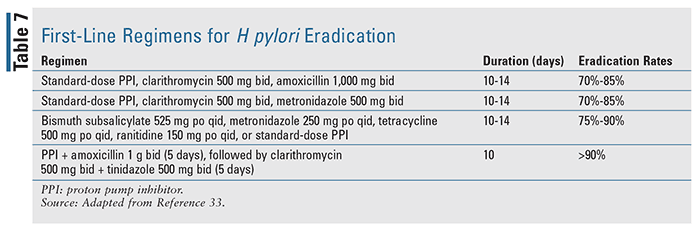
Patienter som diagnostiseras med blödning i samband med Helicobacter pylori-infektion bör behandlas med hjälp av en riktlinjebaserad eradikationsterapi med målet att infektionen ska vara helt upplösad.17 Tillgänglig litteratur tyder på att eradikation av H pylori är betydligt effektivare än enbart antisekretorisk behandling hos patienter med UGIB. Första linjens regimer för eradikering av H pylori beskrivs i detalj i TABELL 7 baserat på American College of Gastroenterology’s riktlinjer för hantering av H pylori-infektion.33 När infektionen är löst behöver denna patientgrupp vanligtvis inte få underhållsbehandling med antisekretoriska medel såvida de inte behöver icke-steroida antiinflammatoriska läkemedel eller antitrombotisk terapi, med vilka långvarig antisekretorisk behandling är nödvändig, eftersom användningen av dessa medel kan öka risken för återblödning avsevärt.17,18
Behandlingsöversikt
Efter den initiala bedömningen och riskstratifieringen och när patienten är hemodynamiskt stabil är koloskopi som föregås av kolonrengöring det första diagnostiska förfarandet för de flesta patienter som presenterar en LGIB.21 Hanteringen av LGIB innefattar mestadels icke-farmakologiska interventioner, men det finns fortfarande möjligheter för apotekare att delta i patientvården.
PPI-användning vid LGIB
Till skillnad från UGIB visar tillgänglig litteratur som utvärderar PPI-användning vid LGIB ingen fördel. Försök som utvärderar UGIB och LGIB har visat att medan PPI inte visar på förbättrade resultat vid LGIB, kan de faktiskt öka risken för LGIB.34 De teoretiserade mekanismerna för denna ökade risk fokuserar ofta på möjliga förändringar i mikrobiota, och kan därmed potentiera eventuell risk från NSAID. Dessa resultat har visat sig vara kontroversiella; de ger dock bevis för att patienter med LGIB inte gynnas av PPI-behandling. Denna potentiella risk bör noggrant bedömas hos patienter, särskilt de som löper risk för UGIB, eftersom en noggrann bedömning av risk kontra nytta kan behöva göras.34
Apotekarnas roll
Apotekare från många specialiteter befinner sig i en unik position för att hjälpa till vid behandling och hantering av GIB-patienter. Farmaceuter i öppenvården har en utmärkt position för att proaktivt bevaka potentiella riskfaktorer hos patienterna, inklusive högdos NSAID och antikoagulantia, och minska risken för GIB i första ledet. Dessutom kan de tillhandahålla viktig rådgivning och dosoptimering för patienter både före och efter en GIB-diagnos. På samma sätt kan kliniska farmaceuter inom slutenvården också ha en stor roll i behandlingen av GIB. De kan vara i stånd att hjälpa till på flera områden under den inledande utvärderingen och behandlingen. Den inledande läkemedelsavstämningen kan avslöja detaljer som är relevanta för diagnos och behandling av patienterna, t.ex. identifiering av användning av NSAID eller antikoagulantia i öppenvården. Apotekare kan också ge rekommendationer till vårdteamet om vilka läkemedel som kan vara till nytta för varje GIB-fall.
1. El-Tawil A. Trender för gastrointestinal blödning och dödlighet: var står vi? World J Gastroenterol. 2012;18(11):1154-1158.
2. Zhao Y, Encinosa W. Hospitaliseringar för gastrointestinala blödningar 1998 och 2006. Statistical Brief #65. Statistiska rapporter från Healthcare Cost and Utilization Project (HCUP). December 2008.
3. Whelan CT, Chen C, Kaboli P, et al. Upper versus lower gastrointestinal bleeding: a direct comparison of clinical presentation, outcomes, and resource utilization. J Hosp Med. 2010;5(3):141-147.
4. Wilcox CM, Cryer BL, Henk HJ, et al. Mortalitet i samband med gastrointestinala blödningshändelser: jämförelse av kortsiktiga kliniska resultat för patienter som lagts in på sjukhus för övre gastrointestinala blödningar och akut hjärtinfarkt i ett amerikanskt förvaltningsområde. Clin Exp Gastroenterol. 2009;2:21-30.
5. Garcia Rodriguez LA, Ruigómez A, Hasselgren G, et al. Comparison of mortality from peptic ulcer bleed between patients with or without peptic ulcer antecedents. Epidemiology. 1998;9(4):452-456.
6. Wilcox CM, Clark WS. Causes and outcome of upper and lower gastrointestinal bleeding: the Grady Hospital experience. South Med J. 1999;92:44-50.
7. Yavorski RT, Wong RK, Maydonovitch C, et al. Analys av 3 294 fall av övre gastrointestinal blödning i militära sjukvårdsinrättningar. Am J Gastroenterol. 1995;90:568-573.
8. Johanson JF. Att begränsa kostnaderna för gastrointestinala blödningar. Am J Gastroenterol. 1998;93:1384-1385.
9. Scottish Intercollegiate Guidelines Network (SIGN). Hantering av akut övre och nedre gastrointestinal blödning. September 2008. www.sign.ac.uk/assets/sign105.pdf.
10. Kim, SK, Cho CD, Wojtowycz AR. Treitz ligament (duodenums suspensiva ligament): anatomisk och radiografisk korrelation. Abdom Imaging. 2008;33:395-397.
11. Matthew B, et al. Diagnostisering av gastrointestinala blödningar: en praktisk guide för kliniker. World J Gastrointest Pathophysiol. 2014;5(4):467-478.
12. Raju GS, et al. American Gastroenterological Association (AGA) Institute medical position statement on obscure gastrointestinal bleeding. Gastroenterology. 2007;133(5):1694-1696.
13. Tielleman T, Bujanda D, Cryer B, et al. Epidemiologi och riskfaktorer för övre gastrointestinal blödning. Gastrointest Endosc Clin N Am. 2015;25(3):415-428.
14. Rodriguez-Hernandez H, Rodríguez-Morán M, González JL, et al. Riskfaktorer förknippade med övre gastrointestinal blödning och med dödlighet. Rev Med Inst Mex Seguro Soc. 2009;47(2):179-184.
15. Strate L. Lower GI blödning: epidemiologi och diagnos. Gastroenterol Clin North Am. 2005;34(4):643-664.
16. Cocchi MN, Kimlin E, Walsh M, et al. Identifiering och återupplivning av traumapatienter i chock. Emerg Med Clin N Am. 2007;25:623-642.
17. Laine L, Jensen DM. Hantering av patienter med sårblödning. Am J Gastroenterol. 2012;107:345-360.
18. Siau K, Chapman W, Sharma N, et alHantering av akut övre gastrointestinal blödning: en uppdatering för allmänläkaren. J R Coll Physicians Edinb. 2017;47:218-230.
19. Rockall T, Logan R, Devlin H, et al. Riskbedömning efter akut övre gastrointestinal blödning. Gut. 1996;38:316-321.
20. Blatchford O, Murray W, Blatchford M. A risk score to predict need for treatment for uppergastrointestinal haemorrhage. Lancet. 2000;356:1318-1321.
21. Recio-Ramirez, JM, Sánchez-Sánchez Mdel P, Peña-Ojeda JA, et al. Den prediktiva förmågan hos Glasgow-Blatchford-poängen för riskstratifiering av övre gastrointestinal blödning på en akutmottagning. Revista Española de Enfermedades Digestivas. 2015;107(5):262-267.
22. Strate L, Grainek IM. ACG Clinical Guideline: Behandling av patienter med akut nedre gastrointestinal blödning. Am J Gastroenterol. Förhands publicering online 1 mars 2016. 2016;111:459-474.
23. Bessa X, O’Callaghan E, Balleste B, et al. Applicability of the Rockall score in patients undergoing endoscopic therapy for upper gastrointestinal bleeding. Dig Liver Dis. 2006;38:12-17.
24. Chaimoff C, Creter D, Djaldetti M. Effekten av pH på trombocyternas och koagulationsfaktorernas aktivitet. Am J Surg. 1978;136(2):257-259.
25. Sreedharan A, Martin J, Leontiadis GI, et al. Behandling med protonpumpshämmare påbörjad före endoskopisk diagnos vid övre gastrointestinal blödning. Cochrane Database Syst Rev. 2010(7):CD005415.
26. Leontiadis GI , Sharma VK , Howden CW. Behandling med protonpumpshämmare vid blödning från magsår: Cochrane Collaboration metaanalys av randomiserade kontrollerade prövningar. Mayo Clin Proc. 2007;82:286-296.
27. Sachar H, Vaidya K, Laine L, et al. Intermittent vs kontinuerlig behandling med protonpumpshämmare för högriskblödande magsår: en systematisk översikt och metaanalys. JAMA Intern Med. 2014;174(11):1755-1762.
28. Cheng H, Sheu B. Intravenösa protonpumpshämmare för blödning av magsår: kliniska fördelar och begränsningar. World J Gastrointest Endosc. 2011;3(3):49-56.
29. Zhang YS, Li Q, He BS, et al. Behandling med protonpumpshämmare jämfört med H2-receptorantagonister vid övre gastrointestinal blödning efter endoskopi: en metaanalys. World J Gastroenterol. 2015;21(20):6341-6351.
30. Rahman R, Nguyen D, Sohail U, et al. Pre-endoskopisk erytromycinadministration vid övre gastrointestinal blödning: en uppdaterad metaanalys och systematisk översikt. Ann Gastroenterol. 2016,29:312-317.
31. Gralnek IM, Dumonceau JM, Kuipers EJ, et al. Diagnostik och hantering av icke-variceal övre gastrointestinal blödning: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoskopi. 2015;47:1-46.
32. Issa D, Solomon S, Di Pace B, et al. A Comparison of Azithromycin to Erythromycin Infusions in Improving Visualization of Endoscopy for Upper Gastrointestinal Bleeding. Världskongress vid ACG2017. Session 2A.
33. Chey WD, Wong BC. Kommittén för praxisparametrar vid American College of Gastroenterology. American College of Gastroenterology guideline on the management of Helicobacter pylori infection. Am J Gastroenterol. 2007; 102:1808-1825.
34. Luée A, Lanas A. Behandling med protonpumpshämmare och nedre gastrointestinala blödningar: avvägning av risker och fördelar. World J Gastroenterol. 2016;22(48):10477-10481.