A lipofilitás talán a legfontosabb fizikai-kémiai tulajdonsága egy potenciális gyógyszernek, szerepet játszik az oldhatóságban, a felszívódásban, a membránpenetrációban, a plazmafehérjékhez való kötődésben, a megoszlásban, a CNS penetrációban és a más szövetekbe vagy szervekbe, például a májba való átjutásban, és hatással van a clearance útjaira. Fontos a ligandumfelismerésben, nemcsak a célfehérjéhez, hanem a CYP450 kölcsönhatásokhoz, a HERG-kötődéshez és a PXR által közvetített enzimindukcióhoz is.
A logP a Lipinski-féle 5-ös szabály egyik összetevője, amely az oldhatóság és a permeabilitás előrejelzésére szolgáló ökölszabály, és amely a gyógyszer-szerűség helyettesítőjévé vált.
A Developability score DOI négy különböző cLog P/molekulatömeg régiót azonosít, amelyek meghatározzák az optimális és szuboptimális kémiai teret, valamint az oldhatósági, permeabilitási, fehérje kötődési és 3A4 gátlási szűrési adatok felhasználásával készült regressziós modellekből származó fejleszthetőségi pontszámot. Míg a MWt <400, cLogP <4 szektor sugallta a legnagyobb esélyt a sikerre, megjegyezték, hogy még a MWt >400, cLogP >4 szektor is tartalmazott néhány fejleszthető molekulát, bár sokkal kisebb eséllyel.
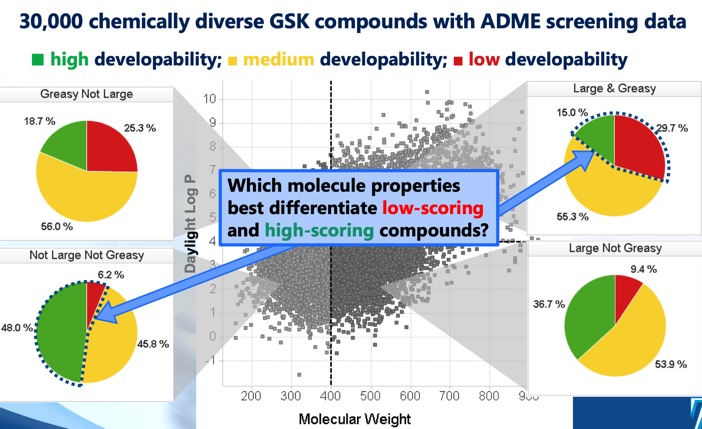
A lipofilitás leggyakrabban használt mértéke a LogP, ez a molekula megoszlási együtthatója a vizes és lipofil fázisok, általában oktanol és víz között.
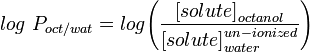
A LogP mérése többféle módon történhet, a legelterjedtebb a rázólombik módszer, amely abból áll, hogy a kérdéses oldott anyag egy részét feloldjuk egy térfogatnyi oktanolban és vízben, egy ideig rázzuk, majd mérjük az oldott anyag koncentrációját az egyes oldószerekben. Ez időigényes lehet, különösen akkor, ha nincs gyors spektroszkópiai módszer a molekula koncentrációjának mérésére a fázisokban. A log P meghatározásának gyorsabb módszere a nagy teljesítményű folyadékkromatográfiát használja. Az oldott anyag log P-je meghatározható a retenciós idejének az ismert log P-értékkel rendelkező hasonló vegyületekkel való korrelálásával doi.
Lipofilitás számítása
Általában nem praktikus minden előállított vegyület logP-jét kísérletileg meghatározni (és érdekes lehet a logP kiszámítása a szintézis előtt), ezért számított eredményeket használnak, számos szoftvereszköz áll rendelkezésre mind asztali, mind online (ne használja bizalmas vegyületekhez).
Ezek közül az alkalmazások közül sok úgy működik, hogy egy nagy, ismert értékeket tartalmazó gyakorló adathalmaz segítségével határozza meg az alstruktúrák és funkcionális csoportok fragmentum-hozzájárulásait, azonban a logP nem egy egyszerű additív tulajdonság, és korrekciós kifejezésekre van szükség a közelségi hatások, H-kötések, elektronikai hatások stb. figyelembevételéhez, amint az az alábbi példákban látható.
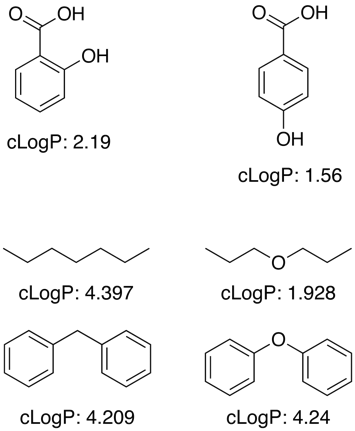
Ismeretlen funkcionális csoportok esetében a programok gyakran az egyes atomok hozzájárulásaival közelítenek.
A logP kiszámításának különböző módszerei három különböző megközelítésre oszthatók.
Atomi (pl. “AlogP”, ) &Elősített atomi / hibrid (“XlogP”, “SlogP”)
Fragmentum (“ClogP”, KlogP, ACD/logP)
Tulajdonság alapú módszerek (“MlogP”, “VlogP”, “MClogP”, “TlogP”)
Az atomi logP figyelembe veszi, hogy minden atom hozzájárul a logP-hez, és hogy a végső értékhez való hozzájárulás tisztán additív. Világos azonban, hogy egy nitrogén egy amidban más, mint egy nitrogén egy aminban vagy piridinben, a Enhanced Atomic figyelembe veszi az atomtípust.
A töredékmódszerek ismert értékekből álló nagy gyakorló adathalmazt használnak az alstruktúrák és funkciós csoportok töredék-hozzájárulásainak meghatározásához, valamint korrekciós kifejezéseket a közelségi hatások figyelembevételére. Ezek a módszerek az új funkcionális csoportok esetében gyakran atomos modellekre támaszkodnak.
A tulajdonságalapú módszerek általában számításigényesek, és nem igazán alkalmasak nagy adathalmazok tesztelésére.
Mivel a képzési halmazok és az algoritmusok alkalmazásonként eltérőek, nagyon fontos, hogy a különböző eszközökkel számított eredményeket ne kombináljuk.
Egyik eszköz lehetővé teszi a felhasználó számára, hogy a házon belül mért értékekkel bővítse a képzési halmazt, ez kritikus lehet új funkcionális csoportok vagy állványok feltárásakor.
LogD
Az ismert gyógyszerek többsége azonban ionizálható csoportokat tartalmaz, amint azt az alábbi hisztogram mutatja, ez mutatja a kis molekulájú gyógyszerek DrugBankkal való eloszlását, és fiziológiás pH-n valószínűleg töltöttek, a LogP pedig csak a semleges (nem töltött) molekulák megoszlási együtthatóját írja le helyesen.
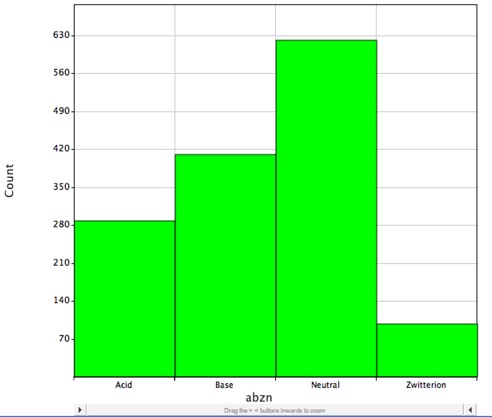
LogD az eloszlási állandó jobban leírja a molekula lipofilitását. Ezt a LogP-hez hasonló módon lehet meghatározni, de víz helyett a vizes fázist pufferrel állítják be egy adott pH-ra. A log D tehát pH-függő, ezért meg kell adni a pH-t, amelynél a log D-t mértük. Különösen érdekes a log D pH = 7,4-nél (a vérszérum fiziológiás pH-ja).
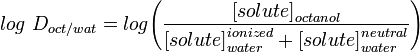
A Marvinhoz hasonló alkalmazások lehetővé teszik a felhasználó számára a log D kiszámítását, de a pH-eloszlási profil megjelenítését is, ahogy az alább látható a warfarin esetében.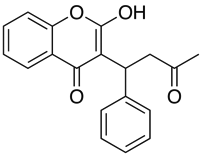
A fiziológiás pH-hoz közeli pKa értékkel rendelkező vegyületek esetében kritikus lehet figyelembe venni, hogy mi lehet valójában a domináns ionizált forma.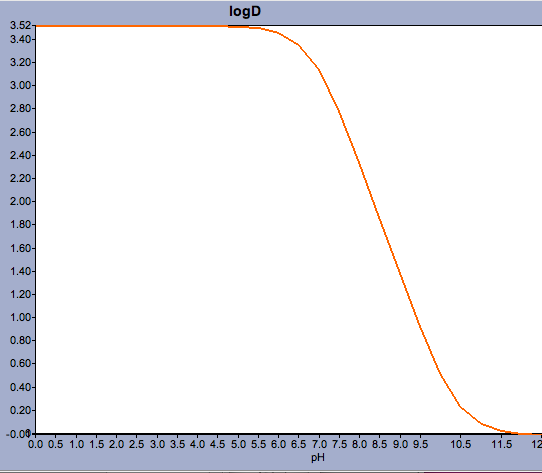
Ez akkor is értékes lehet, ha a tápcsatorna különböző régióiból történő felszívódásra gondolunk, ahol a pH a gyomorban 1-3 és az ileumban 7-8 között változik.
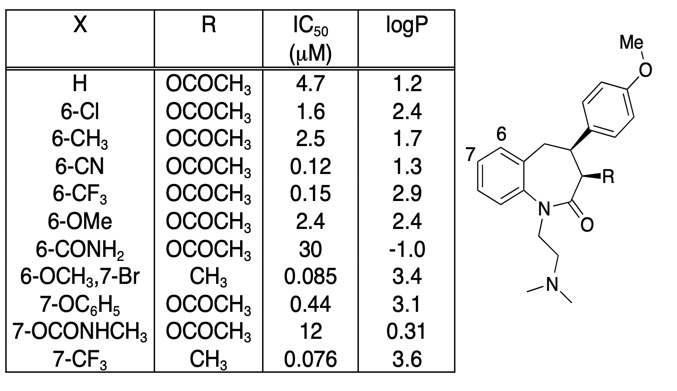
A különböző funkciós csoportok hozzájárulását a LogD-hez “LogD contributions of substituents commonly used in medicinal chemistry” DOI, this study used matched molecular pairs analysis of experimental LogD values from several thousand compounds collected with the shake-flask method at pH = 7,4. Közölték az egyes molekulapárok átlagos deltaLogD-különbségét, és az alábbiakban az eredményeket mutatják be arra az esetre, amikor a funkciós csoport a fenilgyűrű bármely pozíciójában van. Mellékeltem a Chemaxon szoftverrel számított LogD-t is.
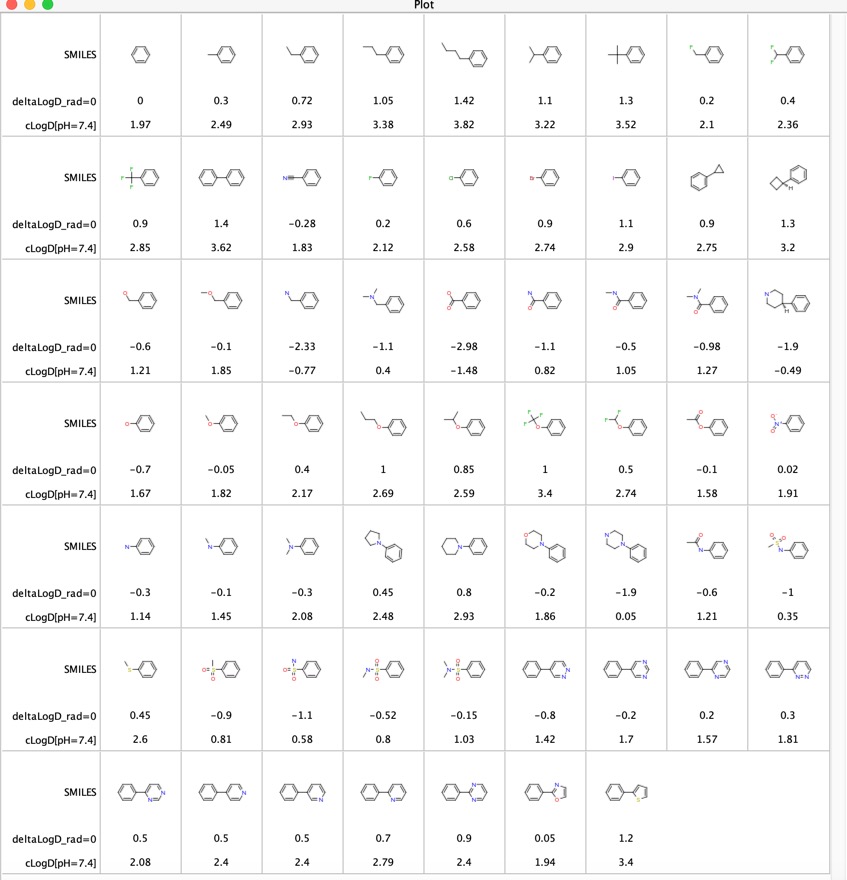
Ez egy hasznos táblázat a funkciós csoportok összehasonlításához, különösen az utolsó 11 bejegyzés hasonlítja össze a különböző heterociklusok hatását a LogD-re. Ezeket a heterociklusokat gyakran használják a fenilgyűrű bioizoszterikus helyettesítésére.
Azt gondoltam, hogy érdekes lehet összehasonlítani az illesztett molekulapárok segítségével meghatározott LogD-különbségeket (deltaLogD_rad=0) a Chemaxon által számított LogD-vel meghatározott értékekkel (deltacLogD). Mint alább látható, elég jó a megfelelés.
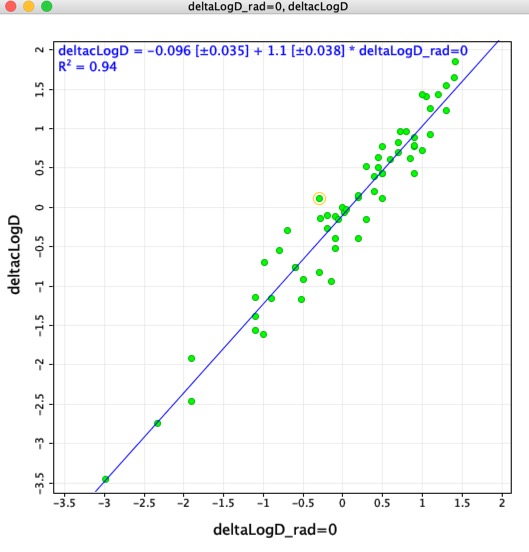
Memlékeztető Mivel a képzési készletek és az algoritmusok alkalmazásonként eltérőek, nagyon fontos, hogy ne kombináljuk a különböző eszközökkel számított eredményeket.
Nagyon fontos körültekintőnek lenni, hogy a kötési affinitás javulása nem kizárólag a LogD növekedésének köszönhető, gyakran hasznos egyszerűen a kötési affinitást a LogD-vel szemben ábrázolni. Az érdekesebb vegyületmódosítások nem feltétlenül azok, amelyek a legnagyobb affinitásnövekedést eredményezik, hanem lehetnek olyanok is, amelyek a lipofilitás megfelelő növekedése nélkül adnak affinitásnövekedést. Ha megnézzük az alábbi táblázatot, számos nagyon nagy affinitású vegyületet találunk.
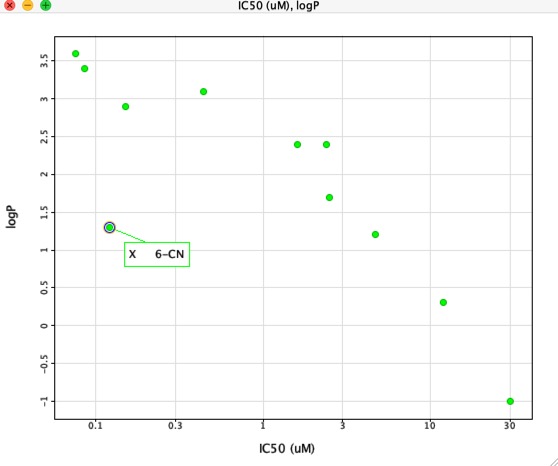
Ha azonban az IC50-et az alábbiakban bemutatott módon ábrázoljuk a LogP-vel szemben, akkor nagyon egyértelmű összefüggés van a LogP és az IC50 között, egy vegyület azonban egyértelműen eltér. A 6-CN szubsztituens az affinitás növekedését eredményezi a LogP megfelelő növekedése nélkül.
A liofilitás szintén fontos összetevő, számos célponton kívüli kötelezettség, beleértve a plazmafehérje kötődést (különösen az albumin), HERG, CYP kölcsönhatások, transzporterek, erős korrelációt mutatnak a liofilitással, és számos tanulmány szerint a magas logP összefügg a vegyületek fejlesztésben való sikertelenségének valószínűségével a rossz ADMET (felszívódás, eloszlás, anyagcsere, kiválasztás és toxicitás) jellemzők miatt. Ezzel szemben gyakran egyértelmű, hogy egy bizonyos méret és lipofilitás szükséges az elfogadható szintű affinitás eléréséhez. E követelmények kiegyensúlyozása kulcsfontosságú kihívás a gyógyszerkutatásban, és az a javaslat, hogy a vegyészek célozzák meg az MWt 250-500 és a LogP 2-4 értékeket. E megközelítés egyik következménye, hogy az alacsony molekulatömegű, kevésbé lipofil vegyületeket kell előnyben részesíteni a szűrés során. A gyógyszerkémia kezdeti fókuszának a jó minőségű kiindulási pontok kiválasztására, majd az optimalizálási folyamat során a fizikai-kémiai tulajdonságok eltolódásának hatékony szabályozására kell irányulnia.
Az olvasásra érdemes
Finding the sweet spot: the role of nature and nurture in medicinal chemistry DOI
Lipophilic efficiency: the most important efficiency metric in medicinal chemistry DOI
Last Updated 12 January 2019
Az utolsó frissítés 2019. január 12.