Mi a PGS, preimplantációs genetikai szűrés?
- A PGS, preimplantációs genetikai szűrés egy vagy több sejt eltávolítását jelenti egy in vitro megtermékenyített embrióból a kromoszóma normál állapotának vizsgálata céljából.
- APGS az embrió normális kromoszómaszámát vizsgálja
- Az embernek 23 kromoszómapárja van – összesen 46
- Az extra vagy hiányzó kromoszóma problémákat okoz
- Egy példa a Down-szindróma, amelynél a 21-es kromoszómaszám extra. Ezt a PGS-sel kell kimutatni.
- A PGS nem vizsgál egy bizonyos betegséget, például a cisztás fibrózist. Ezt az eljárást PGD-nek (preimplantációs genetikai diagnosztika) nevezik.
Sok emberi embrió kromoszómailag rendellenes
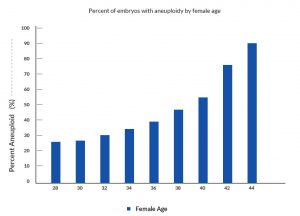
Sok tanulmány kimutatta, hogy összességében az IVF-ből származó emberi preimplantációs embriók mintegy 50%-a kromoszómailag rendellenes. A rendellenességek arányát nagymértékben befolyásolja a nők életkora, amint azt az alábbi grafikon mutatja. Az idősebb nők petesejtjeinek kromoszómáiban jelentősen megnövekedett az abnormalitások aránya.
Mi a teendő, ha az első IVF-kísérlet sikertelen
Az IVF-embriók aneuploidia-szűrésével kapcsolatos korábbi problémák
Az Egyesült Államok egyes klinikáin az 1990-es évek közepétől alkalmazzák az IVF-et és a PGS-t az aneuploidia (a kromoszómák rendellenes száma) vizsgálatára. A vizsgálatok azonban azt mutatták, hogy az embrióbiopszia elvégzése a 3. napon és a genetikai elemzés elvégzése a FISH-technológiával (fluoreszcens in situ hibridizáció) nem eredményezte a páciensek esélyének növekedését a sikeres IVF-ciklusra.
Ezzel a megközelítéssel 2 fő probléma volt.
Néha, miután az IVF során ismételten nem sikerült embriót beültetni, a nők azt mondják;
- A FISH-technológia általában csak 5 kromoszómát vizsgált a 23-ból. Ezért a FISH-teszt számos kromoszóma-rendellenességet kihagyna. Ez azt eredményezte, hogy abnormális embriókat ültettek át, miután a szűrővizsgálat “normális” eredményt hozott.”
- A 3. napon végzett biopsziák során egy sejtet (vagy 2 sejtet) távolítottak el egy 6-10 sejtes embrióból. Ehhez viszonylag nagy lyukat kellett készíteni az embrió héján, majd eltávolítani az embrió “biomasszájának” jelentős százalékát (az embrió egy hatodától egy tizedéig, vagy annál is több).
A legújabb fejlesztések lehetővé teszik az aneuploidia-szűrés utáni jobb IVF sikerességi arányokat
A területen elért fejlődés olyan továbbfejlesztett genetikai technológiák felhasználásához vezetett, amelyek lehetővé teszik mind a 23 kromoszómapár értékelését.
Jelenleg 4 olyan technológia létezik, amely mind a 23 kromoszóma normalitásának értékelésére felhasználható:
- Next Generation Sequencing (NGS)
- Array Comparative Genomic Hybridization (aCGH)
- Single nucleotide polymorphism microarrays (SNP)
- Quantitative real time polymerase chain reaction (qPCR)
Comparative Genomic Hybridization (gyakran CGH-nak nevezik, vagy aCGH) egy olyan microarray-technológia, amelyet ma már gyakran alkalmaznak a régebbi és sokkal kevésbé átfogó FISH helyett. A microarray CGH-val az embrióban lévő tényleges DNS-t hasonlítják össze egy ismert normál DNS-mintával, több ezer specifikus genetikai marker felhasználásával. Ez sokkal pontosabb eredményt ad, és sokkal kevesebb hamis normális vagy hamis abnormális eredményt ad.
Egyes tanulmányok szerint a hibaarány az array CGH technológia alkalmazásával körülbelül 2%. A FISH hibaaránya körülbelül 5-10%. Ezenkívül sok más abnormális embriót a FISH normálisnak jelentene, mivel a rendellenesség olyan kromoszómában volt, amely nem volt része a használt FISH panelnek.
A következő generációs szekvenálás (NGS) egy újabb technológia, amelyet körülbelül 2015 óta egyre gyakrabban használnak az IVF-embriók vizsgálatára. Úgy tűnik, hogy az NGS az aCGH-hoz képest jobban kimutatja a kisebb szegmentális változásokat. Úgy gondolják, hogy a részleges aneuploidia és a kis kiegyensúlyozatlan transzlokációk kimutatásában is jobb. A mozaikosság valószínűleg nagyobb valószínűséggel fedezhető fel az újgenerációs szekvenálással.
Az embrióbiopsziás technikák fejlődése
A tropectoderma biopsziát a blasztociszta stádiumban, az 5. és 6. napon végzik. Ebben a stádiumban már sokkal több sejt van jelen az embrióban. Ez lehetővé teszi több sejt eltávolítását a trophectodermából (a placenta előfutárai). A belső tömegsejtek (a magzat előfutárai) a biopszia során érintetlenül hagyhatók.
A tropektoderma biopszia során körülbelül 5 sejtet vágnak le a genetikai vizsgálathoz. Ez nem gyengíti jelentősen az embriót, mivel ebben a stádiumban körülbelül 70-150 sejtből áll.
Ez a két módosítás (a fejlett genetika és a trophectoderma biopszia) kombinációja jelentősen javította a terhesség sikerességét azon betegek esetében, akik a PGS-t szeretnék igénybe venni az IVF-kezelésükhöz.
Az Egyesült Államokban néhány klinika a trophectoderma biopsziát és az újabb genetikai technológiákat használja az embriók szűrésére néhány IVF-páciensnél. Az egyes IVF-programokban (beleértve a miénket is) tapasztalt eredmények nagyon ígéretesek.
- Lényegesen jobb folyamatos terhességi arányokat látunk azoknál a betegeknél, akiknél trophectoderma biopsziát végeznek a blasztociszta stádiumban, majd ezt követően lefagyasztják az embriókat.
- A fagyasztott, felolvasztott transzferciklusra a kromoszómaelemzés eredményeinek megérkezése után kerül sor
A méh fogékonyságával kapcsolatos problémák
Egy érdekes spekuláció szerint a méhnyálkahártya kevésbé lehet fogékony egy stimulált ciklus során, mint a kontrollált vagy “mesterséges” embriócsere ciklusban.
- Egyes termékenységi orvosok úgy vélik, hogy az embriók átültetése ellenőrzött ciklusban (fagyasztott embriók felhasználásával) magasabb terhességi arányt eredményez, mint a “friss” ciklusban
- Ezt még nem vizsgálták alaposan több ellenőrzött klinikai vizsgálatban
- A blasztociszta biopsziát követően tapasztalt jobb sikerességi arány és átfogó kromoszómaelemzéssel elért jobb eredmény elsősorban a kromoszómailag normális embriók átültetéséből származó előnyöknek köszönhető
- Egyes nőknél további előnyökkel jár, ha az embrió(k) átültetése fagyasztott, felolvasztott ciklusban történik, nem pedig stimulált ciklusban
Mely pároknak kellene aneuploidia-szűrést kínálnunk?
- Ez jelenleg egy fejlődő kérdés a reprodukciós orvostudomány területén
- Egyes potenciális jelöltek lehetnek:
- 35 év feletti (kb.) 35 év feletti nők, akik IVF-et végeznek
- Minden korú páciensek, akiknek több IVF ciklusa sikertelen volt. Válaszokat szeretnének arra, hogy miért nem sikerül. Azt is szeretnék tudni, hogy mit tegyenek annak érdekében, hogy javítsák esélyeiket a gyermekvállalásra. A PGS néha választ ad.
- A PGS a rendellenes embriók “kigyomlálását” is biztosíthatja. Például, ha a 6 embrióból egy kromoszómailag normális, és a 6-ből 5 abnormális – az egyetlen normális embriót ültetjük át, és nagyon jó esélyünk lehet a babára.
- Párok ismétlődő vetélésekkel
- Aki szeretné használni ezt a technológiát embrióinak szűrésére annak érdekében, hogy olyan embriót ültessenek át, amelyik kromoszómailag normálisnak bizonyul – és így nagy eséllyel beültethető és baba születik
A PGD – PGS költségei
A másik kérdés a költség. A PGD költségei az USA-ban körülbelül 3000$-9000$ között mozognak, plusz az összes többi kapcsolódó IVF költség. A PGD-vel kapcsolatos költségek magához az embrióbiopsziás eljáráshoz kapcsolódnak, és a sejtek kromoszómaanalízisét végző genetikai laboratóriumnak is vannak költségei.
- A PGD elvégzéséhez először IVF-et kell végezni (és fizetni) a szokásos IVF költségekért
- Aztán ott vannak a biopszia költségei és a sejtek genetikai elemzése
- Ezután ott vannak a biopszia költségei és a sejtek genetikai elemzése
- Ezután ott vannak az IVF költségei. lehetnek további díjak a fagyasztott embrió transzfer ciklusért, amelyet a genetikai eredmények megérkezése után végeznek
PGD költségek a központunkban
Melyek a legjobb PGD klinikák?
Általában a legjobb klinikák a PGD vagy PGS elvégzésére azok a klinikák lesznek, ahol a legjobb az IVF sikerességi arány. Rendkívül fontos, hogy kiváló tenyésztési rendszerrel rendelkezzenek annak érdekében, hogy a biopsziához maximális számú minőségi blasztocisztát kapjanak.
Az IVF magas sikerességi arányaihoz vezető készségek ugyanazok, amelyek megkönnyítik a blasztociszta tenyésztés, a trophectoderm biopszia, a blasztociszta üvegesítés (fagyasztás) és a sikeres fagyasztott-felolvasztott transzfer ciklusok elvégzését.
- Nézze meg a CDC és a SART oldalakat, hogy találjon egy olyan IVF klinikát a környéken, ahol jó az esetszám és magasak a sikerességi arányok.
- Győződjön meg róla, hogy végeznek-e trophectoderm biopsziát
- Vagy jöjjön csak a mi klinikánkra IVF és PGD céljából
.