INTRODUZIONE
La stenosi del segmento prossimale della coronaria discendente anteriore (pAD) è un sottogruppo speciale della cardiopatia ischemica, dato l’alto profilo di rischio che queste lesioni hanno da sole1,2 o nel contesto della malattia multivasale.3 La quantità e la qualità del miocardio a rischio, che dipende dalla permeabilità della pAD, rende necessario un approccio terapeutico più aggressivo. Studi ecografici in vivo su questo tipo di lesioni hanno dimostrato che il coinvolgimento dei vasi è prevalentemente eccentrico.4 Questo spiegherebbe i peggiori risultati ottenuti dopo l’angioplastica coronarica percutanea transluminale (PTCA) in queste lesioni, a causa del fenomeno della retrazione elastica. Diversi studi hanno confrontato le strategie terapeutiche per queste lesioni, in cui i risultati migliori sono generalmente osservati dopo il trattamento interventista (chirurgia di rivascolarizzazione coronarica con innesto di arteria mammaria interna o rivascolarizzazione percutanea rispetto al trattamento medico convenzionale).5-12 Il presente studio valuta l’efficacia e la sicurezza a lungo termine dell’impianto di stent in questo tipo di lesioni, ed è stato intrapreso a causa della scarsità di studi su questo argomento nella nostra area.
METODI
Popolazione dello studio
Un totale di 98 pazienti consecutivi inviati al nostro laboratorio tra aprile 1995 e aprile 1998 sono stati inclusi per uno studio prospettico, non randomizzato, di follow-up clinico. In questo periodo, sono state eseguite 1136 PTCA e il gruppo di studio rappresenta l’8,6% di tutte le procedure interventistiche eseguite nel nostro laboratorio in questo periodo. Il follow-up si è concluso nel maggio 2000.
Criteri di inclusione ed esclusione
I pazienti che presentavano una stenosi significativa della PAD (stenosi superiore al 70% secondo la stima visiva) prima del primo ramo settale e del ramo diagonale maggiore, con evidenza di ischemia nel territorio dipendente dalla PAD, sono stati considerati idonei allo studio. I pazienti sono stati sottoposti a rivascolarizzazione percutanea programmata con palloncino e impianto di stent. Sono stati esclusi i pazienti riferiti in corso di infarto miocardico acuto (AMI) e le lesioni con un’anatomia inadatta alla procedura a giudizio dell’operatore, in particolare le lesioni con occlusione cronica e calcificazione massiva. Tutti i pazienti hanno firmato un protocollo di consenso informato prima di eseguire la rivascolarizzazione. Il gruppo di studio comprendeva tutti i pazienti con lesioni da pAD trattati nel nostro laboratorio in questo periodo.
Protocollo della procedura (PTCA+impianto di stent)
In tutti i casi la PTCA è stata eseguita con accesso vascolare attraverso l’arteria femorale e lo stent è stato impiantato (dopo dilatazione del palloncino) rilasciandolo ad alta pressione (12-14 atmosfere). Gli stent Palmaz-Schatz e NIR (i modelli più utilizzati) sono stati montati manualmente sul palloncino dell’angioplastica. Nell’ultima fase dello studio, sono stati utilizzati stent premontati sul palloncino. Il “successo angiografico della procedura” è stato definito come l’esistenza di lesioni residue inferiori al 30% mediante valutazione visiva del segmento in cui è stato impiantato lo stent. “Frazione di eiezione depressa (EF)” è stata definita come la presenza di un EF inferiore al 50% nelle valutazioni visive. La “malattia multivasale” è stata definita come la presenza di lesioni coronariche significative (stenosi di più del 70% secondo la valutazione visiva) in due o più vasi. Tutti i pazienti hanno ricevuto un trattamento inibitore dell’aggregazione piastrinica con acido acetilsalicilico a tempo indeterminato e ticlopidina per un mese dopo l’angioplastica. Un bolo i.v. di 7500 a 10 000 UI di eparina è stato somministrato prima della procedura, a seconda del peso del paziente, per ottenere tempi di attivazione della tromboplastina parziale superiori a 300 s.
Protocollo di follow-up
Tutti i pazienti hanno partecipato a un follow-up clinico annuale tramite colloquio personale o telefonico. Tutti sono stati sottoposti a test per rilevare l’ischemia come ordinato dai loro cardiologi curanti. Nei casi con risultati di test dubbi o discrepanze tra i sintomi clinici e i risultati dei test, abbiamo ordinato nuovi test per rilevare l’ischemia (nuovi test da sforzo o studi con radionuclidi). L’ultima visita è stata fatta di persona e sono stati eseguiti la storia clinica, l’esame fisico e l’ECG. I pazienti in cui l’angina persisteva con criteri clinici di gravità sono stati sottoposti a una nuova valutazione angiografica direttamente in laboratorio. La restenosi angiografica è stata definita come la presenza di stenosi superiore al 50% nel segmento di pAD trattato con l’impianto di stent.
Una serie di variabili sono state registrate nel gruppo di studio per la successiva analisi e determinazione dei fattori prognostici nell’evoluzione clinica dei pazienti. Queste variabili erano:
— Cliniche: età, sesso, diagnosi prima del cateterismo, presenza di diabete mellito, ipertensione arteriosa, fumo, dislipidemia. I fattori di rischio multipli sono stati considerati esistenti quando tre o più fattori di rischio classici erano associati.
— Anatomico: presenza di malattia multivasale, disfunzione ventricolare sinistra.
— Procedura: lunghezza e diametro dello stent, numero di stent utilizzati, tipo di stent e presenza di lesione ostiale.
-Eventi finali
Durante il ricovero in ospedale e il successivo follow-up, è stata registrata l’incidenza di eventi cardiaci avversi maggiori (MACE) o complicazioni maggiori, definiti come: morte di origine cardiaca, comparsa di un nuovo IMA e necessità di una nuova rivascolarizzazione della PAD. Sono stati registrati i decessi non cardiaci e la necessità di rivascolarizzazione di vasi diversi dalla pAD.
Analisi statistica
Le diverse variabili sono state compilate in un database Microsoft Access® e analizzate con il programma statistico SPSS®, versione 9.0. Le variabili qualitative sono espresse come percentuali e le variabili quantitative come media±deviazione standard (SD). Le curve attuariali di sopravvivenza libera da morte, sopravvivenza libera da morte cardiaca e sopravvivenza libera da eventi sono state stimate con il metodo Kaplan-Meier. Nell’analisi univariata, le diverse variabili cliniche, angiografiche e procedurali specificate sono state confrontate in base alla presenza o assenza di eventi avversi maggiori alla fine del follow-up, le variabili quantitative sono state confrontate con il test t di Student, e le variabili qualitative con il test Chi-quadrato. Inoltre, le curve di sopravvivenza libera da eventi sono state confrontate con il test di log-rank per le variabili che hanno mostrato una tendenza alla presentazione di eventi (PP P
RISULTATI
Caratteristiche di base
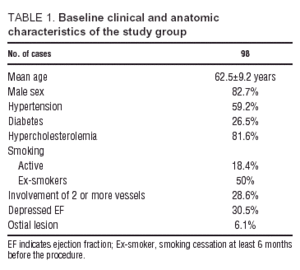
Le caratteristiche cliniche dei pazienti al momento dell’inclusione nello studio e le caratteristiche anatomiche riscontrate nell’arteriografia coronarica sono riportate nella tabella 1. La maggior parte dei pazienti sono stati inviati per angina instabile (87 pazienti angina instabile, 11 angina stabile da sforzo). Ventidue pazienti avevano 3 o più fattori di rischio cardiovascolare; di loro, 20 (91%) erano ipertesi, 19 (86%) erano diabetici, e 21 (95%) avevano dislipidemia, mentre solo 10 (55%) erano fumatori attivi. Il settantuno per cento (71%) dei pazienti aveva una singola lesione del pAD e il 70% di loro non ha evidenziato disfunzioni ventricolari nella ventricolografia.
Procedura
Le variabili della procedura sono riportate nella tabella 2. Il settantasette per cento (77%) dei pazienti aveva lesioni corte del pAD, come riflesso dalla percentuale di stent corti utilizzati (

Evoluzione
Il follow-up medio era 38 ± 11 mesi, essendo inferiore a 24 mesi solo in 2 pazienti che sono morti (a 2 e 9 mesi di inclusione). Nessuna perdita al follow-up si è verificata nel corso dello studio, come mostrato graficamente nella Figura 1. Durante lo studio fino alla finalizzazione, 68 pazienti (69,4%) sono rimasti liberi da angina e non hanno presentato alcun MACE durante il follow-up. Venticinque pazienti (25,5%) hanno avuto un’angina e sono stati sottoposti a una nuova coronarografia. In 7 pazienti è stata osservata una restenosi angiografica, ma non è stata decisa una nuova procedura di rivascolarizzazione percutanea o chirurgica (4 pazienti avevano vasi distali non collegabili e lesioni anatomiche sfavorevoli per una nuova PTCA, e altri 3 avevano una restenosi inferiore al 70% e un adeguato controllo clinico con farmaci antianginosi). Dodici pazienti hanno richiesto una nuova rivascolarizzazione della lesione target: 6 mediante chirurgia coronarica e bypass IMA 3, 6, 6, 9, 13, e 14 mesi, rispettivamente, dopo l’impianto dello stent (in uno, l’intervento è stato eseguito dopo una nuova PTCA della pAD per restenosi precoce a 3 mesi), e 6 mediante una nuova PTCA tra i mesi 5 e 34 di follow-up (in un caso lo stent è stato rimosso a causa della restenosi intrastante). Gli altri 7 pazienti con angina persistente sono stati indirizzati per una nuova rivascolarizzazione con PTCA e impianto di stent in vasi diversi dal pAD, 3 di loro avevano 2 vasi trattati (3 rivascolarizzazioni dell’arteria coronaria destra, 3 della discendente anteriore media e 4 della marginale ottusa). Due pazienti hanno avuto un IMA anteriore (uno silenzioso) rispettivamente 2 e 4 mesi dopo la procedura. La coronarografia non è stata eseguita in seguito perché i test per l’ischemia residua erano negativi.
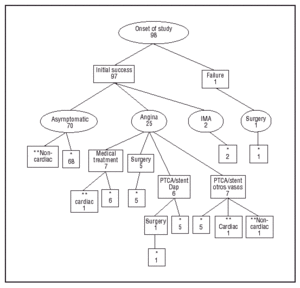
Fig. 1. Diagramma dell’evoluzione dei pazienti (*asintomatico alla fine dello studio, **morte).
Si sono verificati cinque decessi, 2 di origine cardiaca a 2 e 38 mesi di inclusione nello studio, e 3 di origine non cardiaca (1 per malattia neoplastica a 38 mesi di inclusione nello studio, 1 per addome acuto con sanguinamento rettale a 9 mesi, e 1 per ictus ischemico a 24 mesi).
Secondo il test di Kaplan-Meier, la probabilità di rimanere liberi da MACE era dell’83,7% a 60 mesi di follow-up (Figura 2) e le probabilità complessive di non subire morte cardiaca o non cardiaca erano rispettivamente del 98% e del 94,8% (Figura 3).
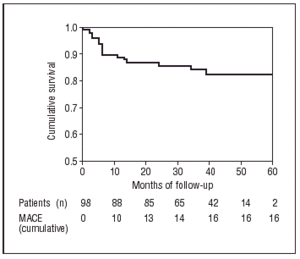
Fig. 2. Curva di Kaplan-Meier di sopravvivenza libera da eventi cardiaci maggiori.
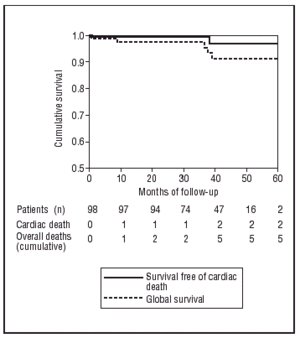
Fig. 3. Curve Kaplan-Meier della sopravvivenza libera da morte e libera da morte di origine cardiaca.
Le variabili cliniche, anatomiche e di procedura, e la loro relazione con l’eventuale comparsa di MACE è mostrata nella tabella 3. L’analisi univariata ha mostrato che l’uso di 2 stent era associato a una maggiore incidenza di MACE (PP=.021), e l’interazione AHT-DM-dislipidemia (OR=3.7; 95% CI, 1.3-10.3; P=.011). Le stenosi ostiali (OR=3.7; 95% CI, 0.8-16.6; P=.09) hanno mostrato una maggiore tendenza al verificarsi di eventi.
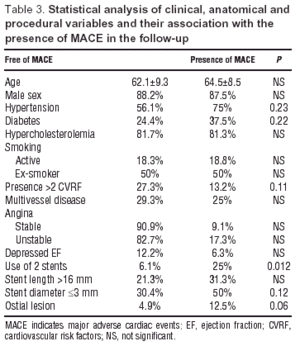
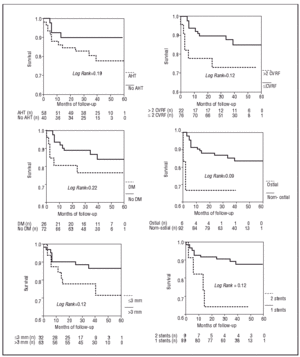
Fig. 4. Curve di Kaplan-Meier della sopravvivenza libera da eventi cardiaci maggiori in base alla presenza di vari fattori clinici e alla procedura. CVRF indica i fattori di rischio cardiovascolare.
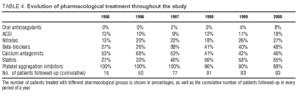
I trattamenti farmacologici ricevuti dai pazienti durante lo studio sono riportati nella tabella 4. Gli inibitori dell’aggregazione piastrinica (acido acetilsalicilico e/o ticlopidina) sono stati spesso utilizzati durante il follow-up, oltre ai calcio antagonisti e ai beta-bloccanti, assunti rispettivamente dal 48% e dal 46% dei pazienti alla fine dello studio. L’uso delle statine è aumentato considerevolmente, dal 27% all’inizio del follow-up al 65% alla finalizzazione.
DISCUSSIONE
Il risultato a lungo termine (follow-up medio e massimo di 38 e 60 mesi, rispettivamente) di questo studio prospettico osservazionale di stenosi del segmento prossimale del PAD trattato con impianto di stent indica che la procedura aveva un alto tasso di successo (98.9%), un basso tasso di nuove rivascolarizzazioni (12,2%), un’alta probabilità di rimanere liberi da MACE (83,7%) e una bassa mortalità. Va notato che una grande percentuale di pazienti aveva lesioni brevi, monovascolari e senza compromissione della funzione ventricolare sinistra.
Confronto con studi precedenti
Studi precedenti hanno dimostrato che il trattamento interventista produce più benefici del trattamento medico farmacologico nella malattia grave del pAD o nella coronaropatia monovascolare.5,6 Tuttavia, il confronto tra le due principali tecniche di rivascolarizzazione (PTCA e innesto IMA) rivela una maggiore incidenza di nuove rivascolarizzazioni nel gruppo trattato con PTCA, una maggiore necessità di farmaci antianginosi e una peggiore tolleranza all’esercizio, con tassi simili di reinfarto e mortalità nei due gruppi.4,7-12 Questa maggiore incidenza di nuove rivascolarizzazioni dopo la PTCA è dovuta al fenomeno della restenosi, che si verifica principalmente nel primo anno dopo la PTCA.13,14 L’incidenza della restenosi dopo la PTCA isolata varia in diverse serie dal 40% al 66%. I fattori che favoriscono la restenosi includono la presenza di lesioni prossimali e il coinvolgimento della coronaria anteriore discendente.15 L’introduzione dell’impianto di stent ha chiaramente modificato questi risultati, riducendo il rischio di restenosi di quasi la metà,9,16-19 con un’incidenza molto bassa di complicanze immediate e un’evoluzione clinica a breve e medio termine molto favorevole (simile a quella ottenuta con l’IMA graft s urgery). Studi precedenti hanno dimostrato una frequenza di fallimento dell’impianto tra gli stent montati manualmente sul palloncino compresa tra l’1,5% e il 6,9% con lo stent Palmaz-Schatz e tra l’1,5% e il 3,1% con lo stent NIR.20,21 Studi recenti sugli stent di seconda generazione, come il registro SPORT-NIR,22 riportano tassi di fallimento dell’impianto di solo 0,4%. Nel nostro studio si è verificato un solo fallimento, con l’impianto dello stent Palmaz-Schatz, che è stato montato manualmente sul palloncino per angioplastica. Questo tasso di fallimento dell’1% coincide con i risultati riportati in studi precedenti.
I tassi di restenosi e la necessità di una nuova rivascolarizzazione dello stent variano in diverse serie dal 19% al 31%.10,16,19,23 I nostri risultati confermano che nuove rivascolarizzazioni della pAD possono verificarsi fino a due anni e mezzo dopo la procedura, anche se la maggior parte dei reinterventi ha avuto luogo nei primi 12 mesi dopo l’impianto dello stent (66,6% dei casi). Abbiamo trovato un’incidenza di nuove rivascolarizzazioni di pAD del 12,2%, anche se la reale incidenza di restenosi significativa e la precocità nella sua comparsa nella nostra serie è sconosciuta poiché non abbiamo valutato sistematicamente i pazienti tramite angiografia.
Predittori di evoluzione
Tra i fattori analizzati, solo l’uso di due stent durante la procedura era un fattore di rischio indipendente per una evoluzione clinica meno favorevole, che coincide con la relazione del gruppo di Bauters et al.24
I fattori che tradizionalmente suggeriscono una prognosi peggiore dopo l’impianto dello stent, come il DM, la malattia multivasale, l’ipertensione o la disfunzione ventricolare sinistra nel follow-up a lungo termine25 non sono stati confermati nell’analisi univariata. Nel caso del DM, si è scoperto che il fenomeno della restenosi è dovuto fondamentalmente a un processo di eccessiva iperplasia intimale rispetto ai pazienti non diabetici,26 in cui questo processo si sviluppa in modo meno aggressivo. Questo fenomeno si esprime con tassi più elevati di restenosi e necessità di nuove procedure di rivascolarizzazione.27 Dei 23 pazienti diabetici del nostro studio, la maggior parte (20 su 23) erano non insulino-dipendenti, il che può spiegare perché il DM non era un fattore predittivo indipendente, dato che studi recenti hanno dimostrato una differenza nell’evoluzione della permeabilità dello stent a seconda del tipo di diabete. La prognosi è peggiore nel DM insulino-dipendente.28,29 Tuttavia, l’associazione di DM, AHT e dislipidemia è stata identificata come associata a una peggiore evoluzione clinica nell’analisi multivariata. Questo ha dimostrato che anche se questi fattori non erano chiaramente legati alla prognosi individualmente (almeno campioni della dimensione studiata qui), la concomitanza di fattori in un paziente deve essere considerata predittiva di un’evoluzione meno favorevole, come avviene nella malattia aterosclerotica in generale.
C’è stato un uso pesante di farmaci durante tutto il follow-up, dovuto fondamentalmente all’alta prevalenza nella popolazione di studio dei tradizionali fattori di rischio cardiovascolare come l’ipercolesterolemia e AHT, e la malattia multivascolare manifestata al momento dell’inclusione (31%) e durante l’evoluzione (7 pazienti hanno presentato progressione della malattia coronarica che richiede la rivascolarizzazione di altri vasi).
Implicazioni cliniche
I risultati del nostro studio confermano la sicurezza dell’impianto di stent nelle lesioni che coinvolgono la pAD e una buona risposta clinica a lungo termine, che in alcuni pazienti ha raggiunto 5 anni di follow-up. I dati ottenuti per la sopravvivenza e l’assenza di MACE coincidono con precedenti studi sull’impianto di stent nella pAD,30 e sono paragonabili a quelli riportati in altri studi in cui è stata eseguita una rivascolarizzazione coronarica con innesto di IMA.7,31
Nella pratica clinica8,32 la decisione di scegliere l’intervento di bypass IMA rispetto alla PTCA e all’impianto di stent deve essere presa individualmente per ogni paziente, tenendo conto dell’opinione del paziente dopo aver ricevuto informazioni su entrambe le alternative terapeutiche, sui loro risultati e rischi, e considerando l’alternativa percutanea come prima scelta nei casi con un’anatomia coronarica favorevole e nei pazienti in cui si può prevedere la necessità di future rivascolarizzazioni (es, I limiti dello studio
La principale limitazione dello studio è stata l’assenza di randomizzazione, che ha precluso l’analisi comparativa diretta con altre strategie di rivascolarizzazione. Il fatto che l’arteriografia coronarica non sia stata eseguita sistematicamente durante il follow-up non ci permette di determinare il vero tasso di restenosi angiografica nel gruppo di studio. La tecnologia utilizzata era efficace a partire dal 1995. L’uso di nuovi materiali e disegni negli stent di generazione successiva e nuovi regimi antiaggreganti con antagonisti dei recettori piastrinici IIb-IIIa dovrebbero migliorare i risultati a breve e a lungo termine. Tuttavia, i risultati ottenuti con questi agenti nel nostro studio non sembrano sostenere il loro uso generalizzato nell’impianto di stent a causa del loro elevato rapporto costo/beneficio.
CONCLUSIONI
Il trattamento della stenosi del segmento prossimale dell’arteria coronaria discendente anteriore con impianto di stent è sicuro nei pazienti con un’anatomia coronarica favorevole a questa procedura. La percentuale di complicazioni è bassa e, in un follow-up prolungato, che in alcuni casi nel nostro studio è di 5 anni, accompagnata da una bassa incidenza di nuove procedure di rivascolarizzazione e un alto tasso di sopravvivenza.
Riconoscimenti
Vorremmo esprimere la nostra più sincera gratitudine ai Dott. V. Climent e J. Sánchez, dei Dipartimenti di Cardiologia e Medicina Preventiva, rispettivamente, dell’Ospedale Generale Universitario di Alicante, per il loro sostegno e la loro guida nello sviluppo di questo articolo.