Il cancro è il risultato della rottura dei controlli che regolano le cellule. Le cause della rottura includono sempre cambiamenti in geni importanti. Questi cambiamenti sono spesso il risultato di mutazioni, cambiamenti nella sequenza del DNA dei cromosomi. Le mutazioni possono essere cambiamenti molto piccoli, che interessano solo pochi nucleotidi, o possono essere molto grandi, portando a grandi cambiamenti nella struttura dei cromosomi.
Mutazioni sia piccole che grandi possono influenzare il comportamento delle cellule. Combinazioni di mutazioni in geni importanti possono portare allo sviluppo del cancro. Il materiale trattato in questa pagina descrive la relazione tra mutazione e cancro, i diversi tipi di mutazioni e cosa le causa. Ulteriori informazioni sugli argomenti di questa pagina possono anche essere trovate nella maggior parte dei libri di testo introduttivi alla biologia, noi raccomandiamo Campbell Biology, 11a edizione.1
Temi trattati in questa pagina:
- Mutazione e cancro
- Mutazioni ereditarie e cancro
- Tipi di mutazione
- Mutazioni puntiformi
- Traslocazioni
- Amplificazione genica
- Inversioni, Delezioni e Duplicazioni
- Aneuploidia
- Cambiamenti Epigenetici
- Cause di Mutazione
- Riassunto di Mutazione
- Conosci il Flusso: Mutazione
Mutazione e cancro
I comportamenti anormali dimostrati dalle cellule cancerose sono il risultato di una serie di mutazioni in geni regolatori chiave. Le cellule diventano progressivamente più anormali man mano che più geni vengono danneggiati. Spesso, i geni che controllano la riparazione del DNA si danneggiano essi stessi, rendendo le cellule ancora più suscettibili a livelli sempre maggiori di caos genetico.
Di seguito un’animazione che dimostra la relazione tra cromosomi, geni e DNA.
Si pensa che la maggior parte dei tumori sorga da una singola cellula precursore mutante. Quando questa cellula si divide, le risultanti cellule “figlie” possono acquisire diverse mutazioni e diversi comportamenti in un certo periodo di tempo. Le cellule che ottengono un vantaggio nella divisione o nella resistenza alla morte cellulare tenderanno a prendere il sopravvento sulla popolazione. In questo modo, le cellule tumorali sono in grado di acquisire una vasta gamma di capacità che non sono normalmente viste nella versione sana del tipo di cellula rappresentata. I cambiamenti nel comportamento visti nelle cellule tumorali sono l’obiettivo della sezione Cancer Biology del sito.
Mutazioni in geni regolatori chiave (soppressori tumorali e proto-oncogeni) alterano il comportamento delle cellule e possono potenzialmente portare alla crescita sregolata vista nel cancro.
Per quasi tutti i tipi di cancro studiati finora, sembra che la transizione da una cellula normale e sana a una cellula tumorale sia una progressione a tappe che richiede molti cambiamenti genetici che si sommano per creare la cellula tumorale. Queste mutazioni si verificano sia sugli oncogeni che sui soppressori tumorali. Questo è uno dei motivi per cui il cancro è molto più diffuso negli individui più anziani. Per generare una cellula tumorale, una serie di mutazioni deve verificarsi nella stessa cellula. Poiché la probabilità che un qualsiasi gene venga mutato è molto bassa, è logico che la possibilità che si verifichino diverse mutazioni nella stessa cellula sia davvero molto improbabile. Per questo motivo, le cellule di un corpo di 70 anni hanno avuto più tempo per accumulare i cambiamenti necessari per formare cellule tumorali, ma quelle di un bambino hanno molte meno probabilità di aver acquisito i cambiamenti genetici richiesti. Naturalmente, alcuni bambini si ammalano di cancro, ma è molto più comune negli individui più anziani. Il grafico qui sotto mostra i tassi di cancro al colon negli Stati Uniti in funzione dell’età. Il grafico è stato ottenuto dal National Cancer Institute. 2
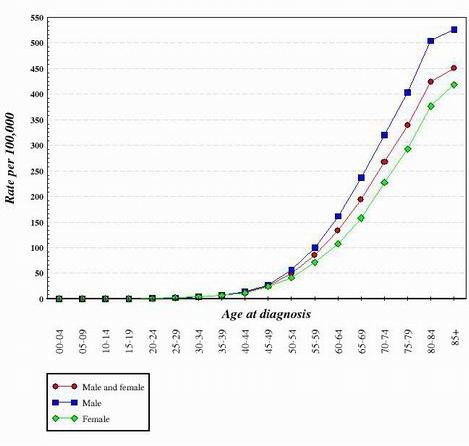
Guardando la forma di curve come quelle mostrate sopra, si è concluso che sono necessari diversi cambiamenti genetici per creare cellule che diventano cancerose.
In laboratorio, i ricercatori hanno cercato di creare cellule tumorali alterando o introducendo proteine regolatrici chiave. Diversi studi hanno tentato di definire il numero minimo di cambiamenti genetici necessari per creare una cellula tumorale, con risultati intriganti.3
In natura, le mutazioni possono accumularsi nelle cellule nel tempo e se il “giusto” gruppo di geni è mutato, il cancro può risultare. Uno studio del 2012 ha dimostrato che le cellule staminali del midollo osseo in un individuo sano accumulano molte mutazioni man mano che la persona invecchia. Solo pochi altri cambiamenti ai geni chiave possono causare il cancro. I risultati implicano che le cellule “normali” e le cellule cancerose potrebbero non essere così diverse in molti casi.4
Mutazioni ereditate nel cancro
Per complicare le cose, è chiaro che i cambiamenti necessari per creare una cellula cancerosa possono essere realizzati in molti modi diversi. Anche se tutti i tumori devono superare lo stesso spettro di funzioni di regolazione per crescere e progredire, i geni coinvolti possono essere diversi. Inoltre, anche l’ordine in cui i geni vengono de-regolati o persi può variare. Per esempio, i tumori del cancro al colon di due individui diversi possono coinvolgere insiemi molto diversi di soppressori tumorali e oncogeni, anche se il risultato (il cancro) è lo stesso.
La grande eterogeneità vista nel cancro, anche quelli dello stesso organo, significa che la diagnosi e il trattamento sono complicati. Gli attuali progressi nella classificazione molecolare dei tumori dovrebbero consentire la progettazione razionale di protocolli di trattamento basati sui geni effettivamente coinvolti in ogni caso dato. I nuovi test diagnostici possono comportare lo screening di centinaia o migliaia di geni per creare un profilo personalizzato del tumore in un individuo. Queste informazioni dovrebbero permettere la personalizzazione dei trattamenti del cancro orientati all’individuo. Per maggiori informazioni su questo vedi la sezione Genomica/Proteomica.
I cambiamenti genetici che portano alla crescita cellulare sregolata possono essere acquisiti in due modi diversi. È possibile che la mutazione si verifichi gradualmente nel corso di un certo numero di anni, portando allo sviluppo di un caso “sporadico” di cancro. In alternativa, è possibile ereditare geni disfunzionali che portano allo sviluppo di una forma familiare di un particolare tipo di cancro. Alcuni esempi di tumori con componenti ereditarie note includono:
- Cancro al seno- L’ereditarietà di versioni mutanti dei geni BRCA1 e BRCA2 sono fattori di rischio noti. Anche se molti, se non la maggior parte, gli individui con il cancro al seno non hanno alterazioni rilevabili in questi geni, avendo una forma mutante aumenta la probabilità di sviluppare il cancro al seno.
- Cancro al colon – Difetti nei geni di riparazione del DNA come MSH2 sono noti per predisporre gli individui al cancro colorettale ereditario non poliposico (HNPCC).
- Retinoblastoma – Difetti nel gene soppressore del tumore Rb sono noti per causare questo cancro agli occhi e diversi altri tipi di cancro. Maggiori informazioni su questa particolare malattia possono essere trovate nella sezione su Rb
Questa è una lista incompleta dei tipi di cancro ereditari conosciuti, ed è certo che altre forme ereditarie di cancro saranno identificate man mano che la genetica dei vari tipi di cancro sarà chiarita.
Più informazioni su questo argomento possono essere trovate nei capitoli 2 e 4 di The Biology of Cancer di Robert A. Weinberg.
Tipi di mutazione
Il processo con cui le proteine sono fatte, la traduzione, è basato sulla ‘lettura’ dell’mRNA che è stato prodotto attraverso il processo di trascrizione. Qualsiasi modifica al DNA che codifica un gene porterà ad un’alterazione dell’mRNA prodotto. A sua volta, l’mRNA alterato può portare alla produzione di una proteina che non funziona più correttamente. Anche cambiare un solo nucleotide lungo il DNA di un gene può portare a una proteina completamente non funzionale.
Ci sono diversi modi in cui il DNA può essere alterato. La sezione seguente descrive i diversi tipi di cambiamento genetico in modo più dettagliato.
Mutazioni puntiformi
Le alterazioni genetiche possono essere collocate in due categorie generali. La prima categoria è composta da cambiamenti che alterano solo uno o pochi nucleotidi lungo un filamento di DNA. Questi tipi di cambiamenti sono chiamati mutazioni puntiformi.
Quando i ribosomi leggono una molecola di RNA messaggero, ogni tre nucleotidi viene interpretato come un amminoacido. Questi codici di tre lettere sono chiamati codoni. Per fare un’analogia con una frase inglese: “Il gatto grasso mangiò il topo” conterrebbe 6 codoni. I cambiamenti causati dalla mutazione possono portare a cose come ‘Il gatto grasso mangiò il topo’ o ‘Il fa’ o ‘Il grasso oca tat her at…’ L’impatto sulla proteina dipende da dove avviene il cambiamento e dal tipo di cambiamento.
I codoni a tre lettere letti dai ribosomi possono essere cambiati dalla mutazione in uno dei tre modi:
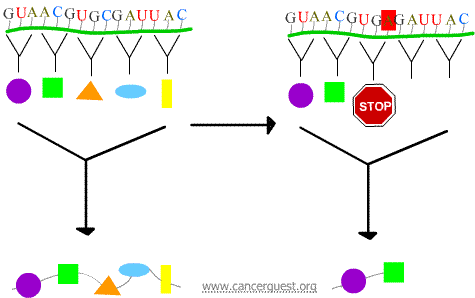
Mutazioni senza senso
Il nuovo codone causa la terminazione prematura della proteina, producendo una proteina che è ridotta e spesso non funziona correttamente o affatto.
Mutazioni missenso
Il nuovo codone causa l’inserimento di un aminoacido sbagliato nella proteina. Gli effetti sulla funzione della proteina dipendono da ciò che viene inserito al posto dell’aminoacido normale.

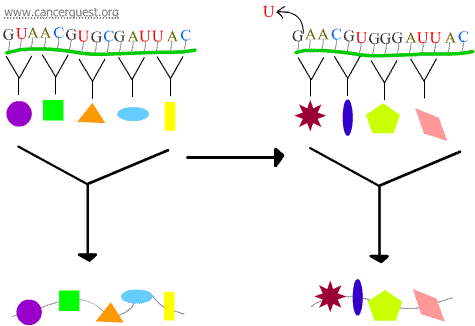
Mutazioni Frameshift
La perdita o il guadagno di 1 o 2 nucleotidi fa sì che il codone interessato e tutti i codoni che seguono siano mal letti. Questo porta ad un prodotto proteico molto diverso e spesso non funzionale.
Errori di trascrizione
Alcuni danni al DNA producono un nucleotide modificato o un piccolo gruppo di nucleotidi che non possono essere ‘letti’ dalla RNA polimerasi. Quando il complesso della RNA polimerasi raggiunge questi punti, a volte bypassa il danno aggiungendo nucleotidi nel tentativo di continuare, anche se ciò significa inserire la cosa sbagliata. Questo processo è noto come mutagenesi trascrizionale e può giocare un ruolo significativo nello sviluppo del cancro.5
Traslocazioni
Un’altra categoria di mutazioni coinvolge alterazioni di grandi quantità di DNA, spesso a livello del cromosoma. Queste sono chiamate traslocazioni e comportano la rottura e lo spostamento di frammenti di cromosoma. Spesso, le rotture in due cromosomi diversi permettono la formazione di due “nuovi” cromosomi, con nuove combinazioni di geni.
Anche se potrebbe sembrare che questo non causi molti problemi, dato che tutti i geni sono ancora presenti, il processo può portare a una crescita cellulare deregolata in diversi modi-
1. I geni possono non essere trascritti e tradotti in modo appropriato nella loro nuova posizione.
2. Lo spostamento di un gene può portare a un aumento o a una diminuzione del suo livello di trascrizione.
3. La rottura e la ricongiunzione possono avvenire anche all’interno di un gene (come mostrato in verde sopra), portando alla sua inattivazione.
Per alcuni tumori, particolari traslocazioni sono molto comuni e possono anche essere usate nella diagnosi della malattia. Le traslocazioni sono comuni nelle leucemie e nei linfomi e sono state meno comunemente identificate nei tumori dei tessuti solidi. Un esempio potrebbe essere uno scambio tra i cromosomi 9 e 22 visto in oltre il 90% dei pazienti con leucemia mieloide cronica (CML). Lo scambio porta alla formazione di una forma accorciata del cromosoma 22 chiamata cromosoma Philadelphia (dal luogo della sua scoperta). Questa traslocazione porta alla formazione di un oncogene dal proto-oncogene abl.67
Altri tumori che sono spesso (o sempre) associati a particolari traslocazioni includono il linfoma di Burkitt, i linfomi a cellule B e diversi tipi di leucemia.
Amplificazione genica
In questo processo molto insolito, il normale processo di replicazione del DNA è seriamente compromesso. Il risultato è che invece di fare una singola copia di una regione di un cromosoma, vengono prodotte molte copie. Questo porta alla produzione di molte copie dei geni che si trovano su quella regione del cromosoma. A volte, vengono prodotte così tante copie della regione amplificata che possono effettivamente formare i propri piccoli pseudocromosomi chiamati cromosomi a doppio minuto.
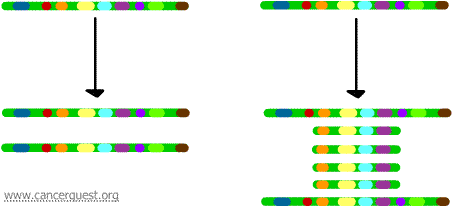
I geni su ciascuna delle copie possono essere trascritti e tradotti, portando a una sovrapproduzione di mRNA e proteine corrispondenti ai geni amplificati come mostrato qui sotto. Le linee grigie rappresentano l’mRNA prodotto attraverso la trascrizione di ogni copia del gene.
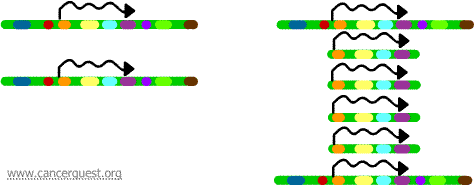
Sebbene questo processo non sia visibile nelle cellule normali, si verifica abbastanza spesso nelle cellule tumorali. Se un oncogene è incluso nella regione amplificata, allora la risultante sovraespressione di quel gene può portare alla crescita deregolata delle cellule. Esempi di questo includono l’amplificazione dell’oncogene myc in una vasta gamma di tumori e l’amplificazione dell’oncogene ErbB-2 o HER-2/neu nei tumori al seno e alle ovaie. Nel caso dell’oncogene HER-2/neu, i trattamenti clinici sono stati progettati per colpire le cellule che sovraesprimono il prodotto proteico.
L’amplificazione genica contribuisce anche a uno dei maggiori problemi nel trattamento del cancro: la resistenza ai farmaci. I tumori resistenti ai farmaci possono continuare a crescere e diffondersi anche in presenza di farmaci chemioterapici. Un gene comunemente coinvolto è chiamato MDR per resistenza multipla ai farmaci. Il prodotto proteico di questo gene agisce come una pompa situata nella membrana delle cellule. È capace di espellere selettivamente le molecole dalla cellula, compresi i farmaci chemioterapici. Questa rimozione rende i farmaci inefficaci.
Questo è discusso più in dettaglio nella sezione sulla resistenza ai farmaci. L’amplificazione di diversi geni può rendere inefficaci altri farmaci chemioterapici.
Inversioni, duplicazioni e delezioni
Inversioni
In queste alterazioni, segmenti di DNA vengono rilasciati da un cromosoma e poi reinseriti nell’orientamento opposto. Come negli esempi precedenti, questo riarrangiamento può portare ad un’espressione genica anormale, attivando un oncogene o disattivando un gene soppressore del tumore.
Duplicazioni/cancellazioni
A causa di errori di replicazione, un gene o un gruppo di geni può essere copiato più di una volta in un cromosoma. Questo è diverso dall’amplificazione genica in quanto i geni non vengono replicati al di fuori del cromosoma e vengono copiati solo una volta in più, non centinaia o migliaia di volte. I geni possono anche essere persi a causa del fallimento del processo di replicazione o di altri danni genetici.

Aneuploidia
L’aneuploidia è il cambiamento genetico che comporta la perdita o l’aumento di interi cromosomi. A causa di problemi nel processo di divisione cellulare, i cromosomi replicati possono non separarsi accuratamente nelle cellule figlie. Questo può portare a cellule che hanno troppi cromosomi o troppo pochi cromosomi. Un esempio di una condizione aneuploide abbastanza comune che non è collegata al cancro è la sindrome di Down, in cui c’è una copia in più del cromosoma 21 in tutte le cellule dell’individuo affetto.
Nell’animazione qui sotto, le copie di due cromosomi sono fatte ma quando la cellula si divide i cromosomi non sono distribuiti uniformemente alle due cellule che si formano (cellule figlie). Il risultato è che una delle cellule ha troppi cromosomi e una non ne ha abbastanza.
Le cellule del cancro sono molto spesso aneuploidi. Gli esseri umani hanno normalmente 46 cromosomi nelle loro cellule, ma le cellule del cancro hanno spesso molti di più, a volte più di 100. La presenza di cromosomi in più rende le cellule instabili e disturba gravemente i controlli sulla divisione cellulare. Attualmente c’è un dibattito in corso sul fatto che tutti i tumori siano o meno aneuploidi. Indipendentemente dal fatto che questo sia il caso, è chiaro che l’aneuploidia è una caratteristica comune delle cellule cancerose.
Cambiamenti epigenetici
Oltre alle alterazioni effettive nella sequenza del DNA, l’espressione genica può essere alterata da cambiamenti al DNA e alla cromatina che non cambiano la sequenza. Poiché questi cambiamenti non alterano la sequenza del DNA nei geni, sono chiamati cambiamenti epigenetici. Due tipi di cambiamenti epigenetici sono descritti di seguito.
Metilazione
In questa alterazione, alcuni nucleotidi nel DNA sono modificati dall’aggiunta di un gruppo metile (-CH3) alla base. La metilazione del DNA è associata all’inattivazione di quella particolare regione di DNA. Modelli anormali di metilazione del DNA sono stati osservati nelle cellule tumorali. Come i cambiamenti descritti, la metilazione altera l’espressione dei geni colpiti.
Acetilazione
In questo cambiamento epigenetico, le proteine istone intorno alle quali è avvolto il DNA vengono modificate dall’aggiunta di gruppi acetile (-CH3CHO). Questa alterazione porta ad un allentamento dell’interazione DNA:istone ed è associata ad un aumento dell’espressione genica. La modifica dei processi di aggiunta e rimozione dei gruppi acetilici al DNA è un’area attiva della ricerca sul trattamento del cancro.
Più sui cambiamenti epigenetici e sui trattamenti del cancro.
Cause della mutazione
Come abbiamo visto, le cellule cancerose si creano da cellule precursori normali attraverso un accumulo di danni genetici. I meccanismi con cui vengono indotti i cambiamenti sono vari. In senso lato, gli agenti del cambiamento genetico (mutazione) rientrano principalmente nelle categorie descritte di seguito e sono discusse in profondità nella sezione seguente.
Mutazioni spontanee
Mutazioni spontanee: Le basi (A, T, G, C) nel DNA sono alterate o perse a causa di errori di replicazione non riparati o eventi molecolari casuali. Per esempio, la perdita di un gruppo amminico dalla citosina, una base normale presente nel DNA, porta alla produzione di uracile, una base che non si trova normalmente nel DNA. Se questo cambiamento non viene rilevato e invertito, può risultare una mutazione. Occasionalmente, un’intera base può essere persa come risultato della scissione del legame tra la spina dorsale del DNA e la base. Questo porta ad un vuoto nella doppia elica del DNA, che, se non riparato, può portare ad una mutazione la prossima volta che il DNA viene copiato (cioè durante la replicazione).
Mutazioni indotte
Mutazioni indotte: Le mutazioni possono essere indotte esponendo organismi (o cellule) a una varietà di trattamenti. Alcuni dei più comuni sono:
Radiazioni- Uno dei primi mutageni conosciuti, le radiazioni sono un potente induttore di mutazioni. Diversi tipi di radiazioni causano diversi tipi di cambiamenti genetici. Le radiazioni ultraviolette (UV) causano mutazioni puntiformi. I raggi X possono causare rotture nella doppia elica del DNA e portare a traslocazioni, inversioni e altri tipi di danni cromosomici. L’esposizione ai raggi UV nella luce del sole è stata collegata al cancro della pelle. Si noti che le proprietà dannose per il DNA delle radiazioni sono state utilizzate in diversi trattamenti contro il cancro basati sulle radiazioni.
Di seguito è mostrato un tipo di mutazione che è causato dalle radiazioni ultraviolette. In questo esempio, il bombardamento della doppia elica del DNA da parte dei raggi UV causa l’unione di due basi. Questo altera la struttura del DNA e può portare a cambiamenti permanenti se non viene riparato.
Un altro tipo di radiazione è l’energia emessa da elementi radioattivi naturali (come il radon e l’uranio) o da fonti artificiali come quelle trovate (e create) nei reattori nucleari. Le radiazioni di questo tipo sono di diversi tipi e possono causare diversi tipi di danni alle cellule e ai tessuti. Le radiazioni possono danneggiare direttamente il DNA o possono causare la formazione di sostanze chimiche (cioè specie reattive dell’ossigeno o ROS) che possono poi danneggiare il DNA o altri componenti cellulari.
L’esposizione alle radiazioni da materiali radioattivi è stata ben documentata. Le analisi dei sopravvissuti alle bombe atomiche sganciate sul Giappone durante la seconda guerra mondiale hanno mostrato grandi aumenti di leucemie poco dopo l’esposizione e poi aumenti di altri tipi di cancro nei decenni successivi.8
Pericolose quantità di materiali radioattivi sono state anche rilasciate accidentalmente dalle centrali nucleari. L’esposizione alle radiazioni dovuta al rilascio accidentale di materiali radioattivi dal reattore nucleare di Chernobyl è stata associata all’aumento del cancro alla tiroide e di altri tumori maligni.9
Anche i macchinari di imaging medico (come macchine a raggi X e scanner CT) espongono i pazienti alle radiazioni. Le quantità usate per ogni singolo test non si pensa che causino quantità significative di cancro, ma l’impatto a lungo termine di molti test su un periodo di anni non è chiaro.10 Allo stesso modo, l’esposizione dei passeggeri di aerei a scansioni di tutto il corpo negli aeroporti non si pensa che ponga un rischio di cancro.11 I passeggeri che viaggiano in aereo sono anche esposti alle radiazioni provenienti dallo spazio, ma ad un livello basso e non si pensa che costituiscano un rischio di cancro, anche per i membri dell’equipaggio di volo.1112
Mutageni chimici – Molte diverse sostanze chimiche sono note per causare mutazioni. Queste sostanze chimiche esercitano il loro effetto legandosi al DNA o agli elementi costitutivi del DNA e interferendo con i processi di replicazione o trascrizione. Alcuni esempi di potenti mutageni sono il benzo-a-pirene, una sostanza chimica che si trova nel fumo di sigaretta, e l’aflatossina, un mutageno che si trova più spesso nei prodotti agricoli conservati in modo improprio.
Infiammazione cronica- L’infiammazione cronica può portare a danni al DNA a causa della produzione di sostanze chimiche mutagene da parte delle cellule del sistema immunitario. Un esempio potrebbe essere l’infiammazione a lungo termine causata dall’infezione con il virus dell’epatite. Per saperne di più su virus e cancro.
Radicali dell’ossigeno- Durante la cattura di energia dal cibo, che avviene nei nostri mitocondri, possono essere generate sostanze chimiche molto reattive e capaci di danneggiare le membrane cellulari e lo stesso DNA. Questi intermedi reattivi dell’ossigeno (ROI) possono anche essere generati dall’esposizione delle cellule alle radiazioni, come mostrato di seguito.
L’attività mutagena di ROI è associata allo sviluppo del cancro così come le attività di diversi trattamenti anticancro, tra cui radiazioni e chemioterapia. 131415
Divisione cellulare anormale
Durante la mitosi, è possibile che il processo di divisione cellulare non riesca a dividere accuratamente i cromosomi replicati in due cellule figlie. Un errore di questo tipo porterà alla produzione di cellule aneuploidi. Le cellule mancheranno o avranno guadagnato un numero significativo di geni. Questo raro processo può creare cellule che sono più inclini alla divisione cellulare sregolata. Come detto in precedenza, una grande percentuale di cancri isolati da esseri umani sono aneuploidi.
Se una cellula ha una mutazione in un gene il cui prodotto proteico è responsabile del “controllo” del processo di divisione, le cose possono andare rapidamente fuori controllo e le cellule figlie di ogni divisione possono diventare sempre più anormali.
Virus come mutageni
Si pensa che i virus siano responsabili di una percentuale significativa di casi di cancro. I virus possono causare il cancro in una varietà di modi e il modo in cui ogni tipo di virus agisce è probabilmente leggermente diverso. Alcuni virus (compresi molti retrovirus) possono causare mutazioni inserendo i loro geni nel genoma della cellula infettata. Il DNA inserito può distruggere o alterare l’attività dei geni interessati.161718
I virus possono anche causare mutazioni in modi indiretti. Come esempio: Un’infezione da virus dell’epatite può durare per molti anni. Durante questo periodo il sistema di difesa del corpo cerca di liberarsi del virus producendo sostanze chimiche tossiche. Queste sostanze chimiche possono causare danni alle cellule “astanti” altrimenti sane, mandandole sulla strada che porta al cancro. Ci sono numerosi altri modi in cui i virus possono causare il cancro.1920
A causa dell’importanza dei virus nello sviluppo di molti tumori abbiamo creato una sezione dedicata a virus e cancro.
Transposoni come mutageni
I trasposoni sono brevi sequenze di DNA che hanno la capacità di spostarsi da una posizione nel DNA ad un’altra posizione. I trasposoni codificano un enzima, la trasposasi, che agisce per giuntare il trasposone in nuove posizioni in un genoma (vedi schema, sotto a sinistra, di un trasposone). I trasposoni sono stati scoperti da Barbara McClintock e lei ha vinto un premio Nobel per il suo lavoro.2122 Il genoma umano contiene molte copie inattivate di trasposoni che hanno perso la loro capacità di muoversi o “saltare” in nuove posizioni. Circa il 50% del genoma umano è composto da trasposoni ‘morti’.23
Il movimento dei trasposoni attivi può portare a mutazioni, alterando l’attività dei geni. Un esempio visibile del movimento dei trasposoni (chiamato trasposizione), è la colorazione dei chicchi nel mais indiano (vedi sotto a destra). I trasposoni che sono attivi negli esseri umani si pensa siano coinvolti nelle malattie umane, compreso il cancro.242526


Riassunto delle mutazioni
Cambiamento genetico (Mutazione) Introduzione
- I comportamenti anormali dimostrati dalle cellule cancerose sono il risultato di una serie di mutazioni nei geni regolatori chiave (cioè i geni di riparazione del DNA).
- Si pensa che la maggior parte dei tumori sorga da una singola cellula precursore che acquisisce mutazioni sufficienti per diventare una cellula cancerosa.
Mutazioni del DNA
- I cambiamenti genetici possono essere piccoli, colpendo solo uno o pochi nucleotidi (mutazioni puntiformi) o possono essere molto grandi, alterando la struttura di uno o più cromosomi.
- Mutazioni puntiformi
- La traduzione è la produzione di una proteina da parte di enzimi che ‘leggono’ tre ‘parole’ nucleotidiche (codoni) lungo un RNA messaggero (mRNA).
- Anche cambiare un singolo nucleotide lungo il DNA di un gene può portare a una proteina completamente non funzionale. Le mutazioni sono raggruppate in base ai cambiamenti che creano nel prodotto proteico risultante del gene interessato.
- Mutazioni nonsense – Il nuovo codone (mutante) causa l’arresto prematuro della sintesi proteica.
- Mutazioni missense – Il codone alterato provoca l’inserimento di un aminoacido errato nella proteina.
- Mutazioni Frameshift – La perdita o l’aumento di 1 o 2 nucleotidi in un mRNA causa una lettura errata dei codoni. Spesso risulta in proteine accorciate e non funzionali.
- Cambiamenti a livello cromosomico
- Traslocazioni – Rottura e (a volte) scambio di frammenti di cromosoma.
- Amplificazione genica – Una replicazione anomala crea copie multiple di una regione di un cromosoma. Alla fine questo porta alla sovrapproduzione delle proteine corrispondenti.
- Inversioni – Segmenti di DNA vengono rilasciati da un cromosoma e poi reinseriti nell’orientamento opposto.
- Duplicazioni/cancellazioni – Un gene o un gruppo di geni può essere perso completamente o copiato più di una volta all’interno di un cromosoma.
- Aneuploidia – Un cambiamento genetico che comporta la perdita o l’aumento di interi cromosomi.
- Mutazioni spontanee possono verificarsi a causa di DNA non riparato o eventi molecolari casuali.
- L’aneuploidia è molto comune nelle cellule tumorali.
Cambiamenti epigenetici
- L’espressione genica può essere alterata da cambiamenti al DNA e alla cromatina che non cambiano la sequenza genetica. Gli esempi includono la metilazione del DNA e l’acetilazione degli istoni.
- Metilazione – Alcuni nucleotidi nel DNA sono modificati dall’aggiunta di un gruppo metile che è associato all’inattivazione di quella regione di DNA
- Acetilazione – L’aggiunta di gruppi acetile allenta il DNA e aumenta l’espressione genica.
Mutazioni indotte
- Le mutazioni possono essere indotte esponendo organismi (o cellule) a una varietà di trattamenti:
- Radiazioni – I raggi UV causano mutazioni puntiformi e i raggi X causano forme multiple di danno.
- Mutageni chimici – Possono legarsi al DNA o agli elementi costitutivi del DNA e interferire con i processi di replicazione o trascrizione.
- Infiammazione cronica – Danno al DNA dovuto alla produzione di sostanze chimiche mutagene da parte delle cellule del sistema immunitario
- Radicali di ossigeno – Risultano dalla produzione di energia di una cellula e possono danneggiare il DNA.
Altri cambiamenti genetici
- La divisione cellulare aberrante con conseguente divisione errata dei cromosomi può portare all’aneuploidia.
- I virus possono causare danni genetici in diversi modi e sono associati a una vasta gamma di tumori.
Mutazione e cancro
- Sembra che la transizione da una cellula normale e sana a una cellula cancerosa sia una progressione graduale.
- Lo sviluppo del cancro richiede cambiamenti genetici in diversi oncogeni e soppressori tumorali.
- Tutti i tumori devono superare lo stesso spettro di funzioni di regolazione per crescere e progredire, ma i geni coinvolti possono essere diversi.
- L’eterogeneità del cancro complica la diagnosi e il trattamento.
- È possibile ereditare geni disfunzionali che portano allo sviluppo di una forma familiare di un particolare tipo di cancro.
Conosci il Flusso: Mutazione
Conosci il Flusso è un gioco interattivo per testare le tue conoscenze. Per giocare:
- Trascina le scelte appropriate dalla colonna a destra e mettile in ordine nelle caselle a sinistra. Nota che userai solo cinque delle sei scelte per completare il gioco.
- Quando hai finito, clicca su ‘Controlla’ per vedere quante ne hai azzeccate.
- Per le risposte sbagliate, clicca su ‘Descrizione’ per rivedere le informazioni sui processi.
- Per riprovare, scegli ‘Reset’ e ricomincia.
-
1
-
2
-
3
-
4
-
5
-
Per saperne di piùUna cellula è nel processo di sintesi del DNA
-
Per saperne di piùSono fatte molte copie di una regione di un cromosoma
-
Per saperne di piùTrascrizione di geni amplificati
-
Per saperne di piùTraslazione di geni amplificati
-
Per saperne di piùSuperproduzione di una porta alla crescita di un tumore resistente ai farmaci
-
Per saperne di piùLa duplicazione si verifica
Gioca di nuovo
- 1. Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). Campbell Biology (11 ° ed.). Pearson.
- 2. Surveillance, Epidemioloy, and End Results (SEER) rappresentato dal National Cancer Institute
- 3. Hahn WC, Counter CM, Lundberg AS, Beijerbergen RL, Brooks MW, Weinberg RA. “Creazione di cellule tumorali umane con elementi genetici definiti”. Nature 400: 464-468
- 4. Welch JS, Ley TJ, Link DC, Westervelt P, Walter MJ, Graubert TA, DiPersio JF, Ding L, Mardis ER, Wilson RK et al. L’origine ed evoluzione delle mutazioni nella leucemia mieloide acuta. Cell, 20 luglio 2012
- 5. Brégeon D, Doetsch PW. Mutagenesi trascrizionale: cause e coinvolgimento nello sviluppo del tumore. Nat Rev Cancer. 2011 Mar;11(3):218-27.
- 6. Nowell PC, Hungerford DA. “Studi cromosomici su leucociti umani normali e leucemici”. J Natl Cancer Inst (1960). 25: 85-100.
- 7. Rowley JD. “Una nuova anomalia cromosomica coerente nella leucemia mieloide cronica identificata dalla fluorescenza chinacrina e dalla colorazione Giemsa”. Natura (1973). 243: 290-293.
- 8. Ozasa K, Shimizu Y, Sakata R, Sugiyama H, Grant EJ, Soda M, Kasagi F, Suyama A. RISCHIO DI CANCRO E MALATTIE NON-CANCRO NEI SOPRAVVISSUTI ALLA BOMBA ATOMICA. Radiat Prot Dosimetria. 2011 Apr 18.
- 9. Cardis E, Hatch M. L’incidente di Chernobyl – una prospettiva epidemiologica. Clin Oncol (R Coll Radiol). 2011;23(4):251-260. doi:10.1016/j.clon.2011.01.510 Mar 9.
- 10. Fazel R, Krumholz HM, Wang Y, Ross JS, Chen J, Ting HH, Shah ND, Nasir K, Einstein AJ, Nallamothu BK. Esposizione a basse dosi di radiazioni ionizzanti da procedure di imaging medico. N Engl J Med. 2009 Aug 27;361(9):849-57.
- 11. a. b. Mehta P, Smith-Bindman R. Airport Full-Body Screening: Qual è il rischio? Arch Intern Med. 2011 Mar 28.
- 12. Bagshaw M. Radiazione cosmica nell’aviazione commerciale. Travel Med Infect Dis. 2008 maggio;6(3):125-7. Epub 2007 Nov 26.
- 13. Kang DH. “Stress ossidativo, danni al DNA e cancro al seno”. AACN Clin Issues. (2002). 13:540-549
- 14. Athar M. “Stress ossidativo e carcinogenesi sperimentale”. Indian J. Exp. Biol. (2002). 40:656-667
- 15. Marnett LJ. “Radicali Oxy, perossidazione lipidica e danni al DNA”. (2002)181-182:219-222
- 16. Nair V. Oncogenesi indotta da retrovirus e sicurezza dei vettori retrovirali. Curr Opin Mol Ther. 2008 Oct;10(5):431-8.
- 17. Brady G, Macarthur GJ, Farrell PJ. Il virus di Epstein-Barr e il linfoma di Burkitt. Postgrad Med J. 2008 Jul;84(993):372-7.
- 18. Ruprecht K, Mayer J, Sauter M, Roemer K, Mueller-Lantzsch N. Retrovirus endogeni e cancro. Cell Mol Life Sci. 2008 Nov;65(21):3366-82.
- 19. Lupberger J, Hildt E. Oncogenesi indotta dal virus dell’epatite B. World J Gastroenterol. 2007 Jan 7;13(1):74-81.
- 20. Castello G, Scala S, Palmieri G, Curley SA, Izzo F. HCV-carcinoma epatocellulare correlato: Dall’infiammazione cronica al cancro. Clin Immunol. 2010 Mar;134(3):237-50. Epub 2009 Nov 11.
- 21. McClintock B. L’origine e il comportamento dei loci mutabili nel mais. Proc Natl Acad Sci U S A. 1950 Jun;36(6):344-55.
- 22. McClintock, Barbara Nobel lecture
- 23. Burns KH, Boeke JD. Tettonica dei trasposoni umani. Cell. 2012 maggio 11;149(4):740-52.
- 24. Kozeretska IA, Demydov SV, Ostapchenko LI. Elementi genetici mobili e cancro. Dalle mutazioni alla terapia genica. Exp Oncol. 2011 Dec;33(4):198-205.
- 25. Solyom S, Kazazian HH Jr. Elementi mobili nel genoma umano: implicazioni per la malattia. Genoma Med. 2012 Feb 24;4(2):12.
- 26. Iskow RC, McCabe MT, Mills RE, Torene S, Pittard WS, Neuwald AF, Van Meir EG, Vertino PM, Devine SE. Mutagenesi naturale dei genomi umani da retrotrasposoni endogeni. Cell. 2010 Jun 25;141(7):1253-61.