Ossidi di ammina e l’eliminazione di Cope
Gli ossidi di ammina sono preparati ossidando 3º-ammine o piridine con perossido di idrogeno o peracidi (es.ZOOH, dove Z=H o acile).
\
Gli ossidi di ammina sono basi relativamente deboli, pKa circa 4,5, rispetto all’ammina madre. La funzione coordinata covalente N-O è polare, e l’ossigeno è un potente accettore di legami a idrogeno. Se uno dei sostituenti alchilici consiste in una catena lunga, come C12H25, l’ossido di ammina risultante è un tensioattivo anfotero e trova uso in shampoo e altri detergenti delicati.
Una reazione di eliminazione, complementare all’eliminazione di Hofmann, avviene quando gli ossidi di 3º-ammina sono riscaldati a temperature da 150 a 200 ºC. Questa reazione è conosciuta come eliminazione di Cope. Viene comunemente effettuata tramite l’aggiunta a goccia di una soluzione di ossido di ammina in un tubo riscaldato e riempito con piccole perle di vetro. Un flusso di azoto gassoso che scorre attraverso la colonna trasporta i prodotti volatili dell’alchene a un ricevitore raffreddato. Il prodotto contenente azoto è un’ammina idrossile. A differenza dell’eliminazione di Hofmann, questa reazione avviene tramite una riorganizzazione ciclica concertata, come mostrato nel seguente diagramma. Per un tale meccanismo, le moieties di beta-idrogeno e di ossido di ammina hanno necessariamente una sin-relazione.
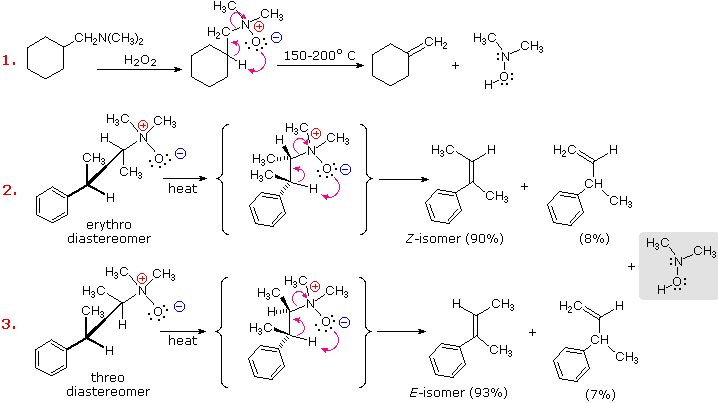
L’eliminazione diope di ossidi di ammina diastereomerici, come quelli mostrati negli esempi #2 & 3 sopra, forniscono la prova della sin-relazione dei gruppi beta-idrogeno e ossido di ammina. Questi esempi dimostrano anche una forte regioselettività che favorisce il doppio legame più stabile.
Sineliminazioni pirolitiche
Gli ossidi di ammina non sono le uniche funzioni che subiscono una sin-eliminazione unimolecolare al riscaldamento. Per vedere esempi di altri casi Clicca Qui