24th Annual Glaucoma Report
Volg de onderstaande links om andere artikelen te lezen uit annual update on glaucoma:
Glaucoom Care with Laser Precision
MIGS Madness: An Atlas of Options
Comanaging Invasive Glaucoma Surgeries
Glaucoma: Lifestyles of the Antioxidant Rich and Famous (Verdien 2 CE Credits)
Deskundigen hebben nog geen consensus bereikt over een universeel aanvaarde etiologie van glaucoom. Ze zijn het echter wel eens over het volgende: verlaging van de intraoculaire druk (IOP) is de enige modificeerbare risicofactor om de progressie van glaucoom te vertragen. Topische farmacotherapie is de traditionele eerstelijnsbenadering, en de opties zijn talrijker dan ooit.
Dit artikel, deel drie van onze Take Charge of Glaucoom-serie, verkent de vele medicijnen die artsen kunnen gebruiken, met advies over wanneer welke therapie te gebruiken voor welke patiënten.
Early Autonomics
Medicijnen die inwerken op het autonome zenuwstelsel (d.w.z., cholinergica en adrenergica) vormen sinds de jaren 1800 de basis van de glaucoomtherapie.1,2 Cholinergica wekken miosis op, waardoor het trabeculaire netwerk (TM) wordt uitgerekt en gestimuleerd om de waterafvoer daar en naar het kanaal van Schlemm te vergroten.3 Tot deze klasse behoren pilocarpine, carbachol, fysostigmine, neostigmine en ecothiofaat. Daarvan wordt alleen pilo nog routinematig gebruikt. De behandeling vertoont een dosisafhankelijke respons met een daling van de IOP met ongeveer 20% indien QID voorgeschreven.4
Take Charge of Glaucoma
Volg de onderstaande links om andere artikelen uit onze vierdelige glaucoomreeks te lezen:
Part One: Glaucoma: A Primary Care Crusade
Part Two: Prepping Your Diagnostic Toolbox
Part Four: Speel een rol in de postoperatieve zorg voor glaucoom
Hoewel het gebruik van cholinerge middelen effectief is, wordt het beperkt door de oculaire en systemische bijwerkingen. Deze omvatten spasmen van de ciliaire spier (met de bijbehorende hoofdpijn en geïnduceerde myopie), miosis, corneatoxiciteit, roodheid, uveïtis, mogelijke cataractvorming, ademhalingsdepressie en gastro-intestinaal ongemak. Bovendien hebben nieuwere geneesmiddelen een grotere IOP-verlagende werkzaamheid, waardoor cholinergica gereserveerd blijven voor specifieke gevallen waarin het miotische effect een bijkomend voordeel kan hebben, zoals acute hoeksluiting.
Adrenerge agonisten daarentegen beïnvloeden de alfa of bèta adrenerge receptoren (of beide indien niet-selectief). Epinefrine, het belangrijkste niet-selectieve middel, vermindert de IOP door eerst de productie van waterige vloeistof te verminderen en vervolgens de uitstroom door het TM te verhogen.5 Helaas wordt dit middel slechts in beperkte mate toegepast vanwege de aanzienlijke systemische bijwerkingen. Dipivefrine, een in de jaren zeventig ontwikkelde prodrug van epinefrine, maakt het gebruik van veel lagere concentraties van de oorspronkelijke stof mogelijk, met minder systemische effecten.6 Niet-selectieve adrenergica worden tegenwoordig nauwelijks meer gebruikt, behalve in gevallen waarin andere geneesmiddelen gecontra-indiceerd zijn.
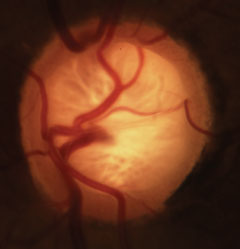
Glaucomateuze cupping met karakteristiek verlies van de neuroretinale rand, lamina en verandering van de vasculatuur. Klik op de afbeelding voor een vergroting.
Bètablokkers
Adrenerge antagonisten, of bèta (β)-blokkers, remmen de productie van kamerwater en vormen de norm waarmee nieuwe geneesmiddelen worden vergeleken. Specifiek verminderen β-blokkers de ultrafiltratie, waardoor de beschikbaarheid van substraat voor de overdracht van kamervocht naar de achterkamer wordt beperkt.1,7,8 Deze geneesmiddelen kunnen niet-selectief zijn, wat betekent dat ze beide isovormen van de β-adrenerge receptoren (β1 en β2) remmen, of cardioselectief, wat betekent dat ze een veel grotere affiniteit voor de β1-receptor hebben. β2 is de belangrijkste adreno-receptor van het oog, zodat niet-selectieve middelen een groter effect op de IOP-controle zullen hebben.9,10
Topische β-blokkers zijn timolol, levobunolol, metipranolol, carteolol en betaxolol. Alleen betaxolol is cardioselectief, waardoor het bij bepaalde contra-indicaties nuttig is, maar het kan minder effectief zijn bij het verlagen van de IOP.11β-blokkers verlagen de IOP met 20% tot 30% en kunnen tweemaal daags worden gedoseerd. Ze kunnen ook eenmaal daags worden gedoseerd, vooral wanneer gelvormende oplossingen worden gebruikt vanwege de langere contacttijd met de ogen.12,13 Adrenerge antagonisten hebben mogelijk minder effect tijdens de slaap, dus is voorzichtigheid geboden wanneer β-blokkers vlak voor het slapengaan worden gedoseerd, vooral wanneer ze eenmaal daags worden voorgeschreven.14,15 Als patiënten systemische β-blokkers gebruiken, vermindert het oculaire hypotensieve effect van topische β-blokkers, en kunnen andere klassen van topische medicatie worden overwogen.16
Hoewel deze klasse van medicatie meestal moet worden vermeden bij pulmonale of cardiale aandoeningen, kan het in selectieve gevallen redelijk zijn om bètablokkeringstherapie te overwegen. Dit dient echter te gebeuren met toestemming van de desbetreffende specialist (cardioloog of longarts).
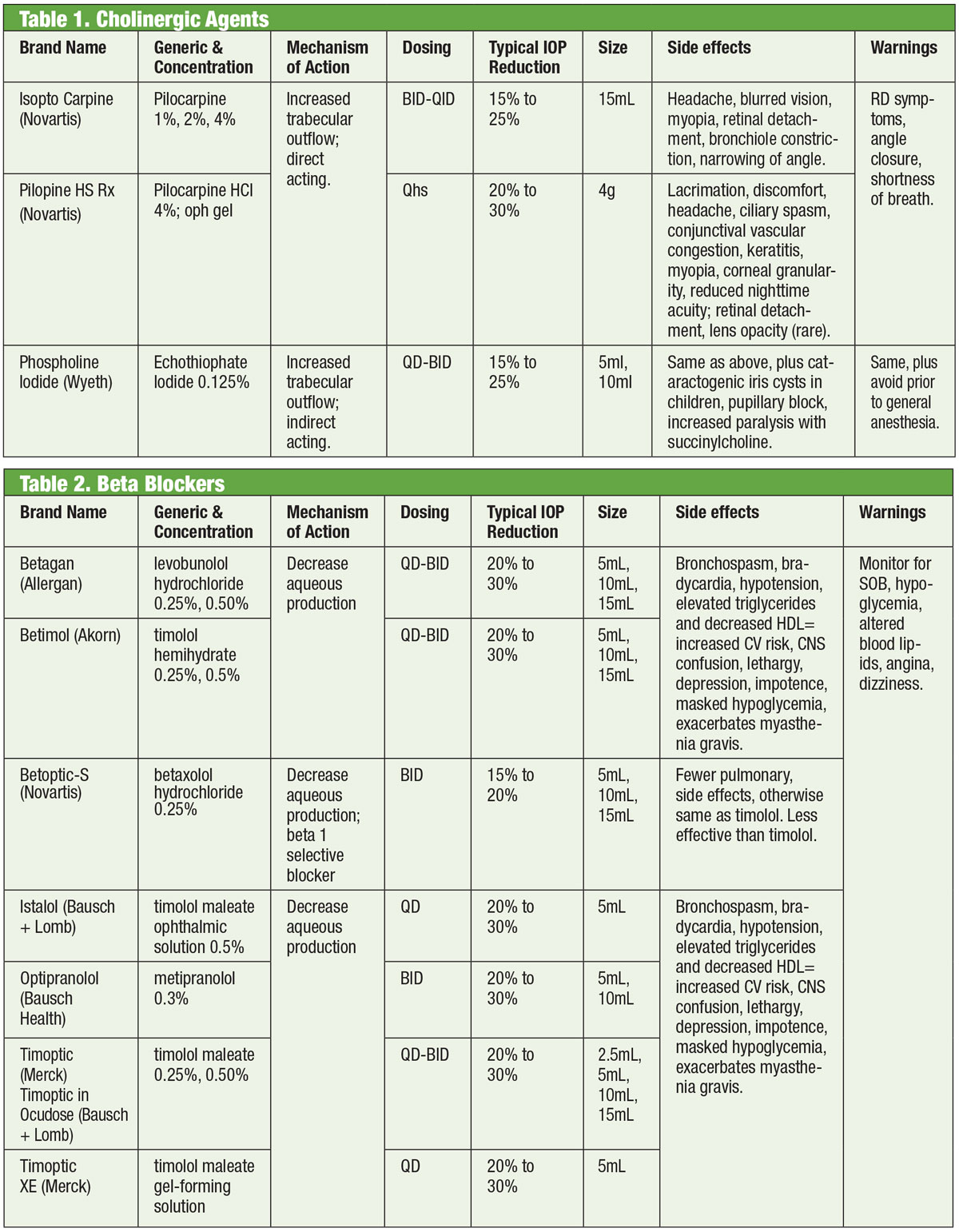
Tabellen: Bruce Onofrey, OD, RPh. Klik op afbeelding om te vergroten.
In het algemeen moet het gebruik van β-blokkers echter worden vermeden bij personen met een atrioventriculair blok, sinusbradycardie en obstructieve longaandoeningen.17
Carbonzuuranhydraseremmers
Onderzoekers erkennen al sinds de jaren vijftig dat orale koolzuuranhydraseremmers (CAI’s) de IOP kunnen verlagen.18 Zij doen dit door de productie van water te onderdrukken.18 Systemische bijwerkingen (zoals vermoeidheid, maag- en darmstoornissen en paresthesie) beperken echter het chronische gebruik ervan bij glaucoom.18 Orale CAI’s worden nog steeds gebruikt in gevallen waarin topische CAI’s overgevoeligheid veroorzaken of wanneer het gebruik van druppels is uitgesloten, evenals in gevallen van acute hoeksluiting.18 Pogingen om een topische variant te formuleren slaagden met de introductie van dorzolamide in het midden van de jaren negentig en, kort daarna, brinzolamide.19
Er zijn ten minste zeven verschillende isoenzymen van koolzuuranhydrase (CA), waarbij CA-II in de ciliaire processen voornamelijk betrokken is bij de productie van water.18 Zowel dorzolamide als brinzolamide zijn krachtige remmers van dit isoenzym, maar zij hebben verscheidene klinisch relevante verschillen. Zo heeft dorzolamide een pH van 5,6 terwijl brinzolamide een pH van 7,5 heeft. Bovendien is brinzolamide beschikbaar als suspensie. Dit zijn slechts enkele van de eigenschappen die de individuele bijwerkingen van de producten kunnen verklaren, waaronder prikken in het geval van dorzolamide en wazig zien in het geval van brinzolamide.19
Hoewel de geneesmiddelen FDA gelabeld zijn voor TID dosering, kiezen sommige practici voor BID toediening. Voor brinzolamide wordt in fase III studies klinisch gelijkwaardige IOP-reducties gerapporteerd met zowel BID- als TID-regimes.20 Anderen rapporteren geen statistisch significante verschillen tussen BID- of TID-dosering met dorzolamide.18 Weer anderen pleiten voor TID-dosering voor monotherapie en BID-dosering bij gebruik als aanvullende therapie.21
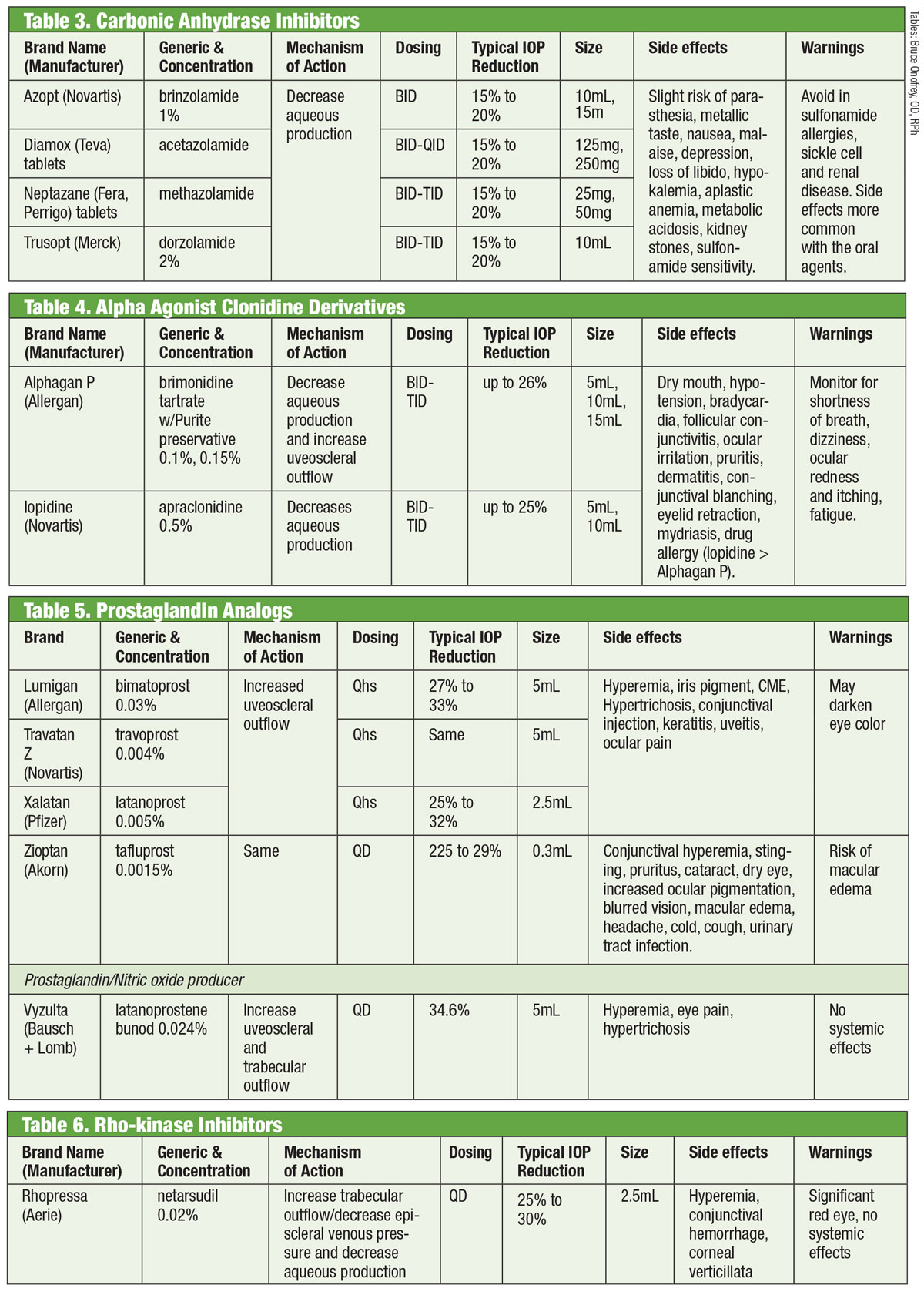
Tabellen: Bruce Onofrey, OD, RPh. Klik op afbeelding om te vergroten.
Alpha-agonisten
Clonidine was de eerste alfa-agonist (AA) die effectief was voor het verlagen van IOP. Zelfs in een topische vorm veroorzaakte deze stof echter ernstige systemische bijwerkingen, zoals bradycardie, sedatie en hypotensie.22 De vervanging van de amidegroep door apraclonidine verminderde de penetratie van de bloed-hersenbarrière, en daarmee ook de bijwerkingen. Helaas beperken de verminderde werkzaamheid na verloop van tijd en een verhoogde incidentie van oculaire allergie het gebruik tot de korte termijn.
Geïntroduceerd in 1997, is brimonidine een krachtige AA met 32 keer meer selectiviteit voor β2 adrenoreceptoren dan apraclonidine.22 Het verlaagt IOP door een tweeledig mechanisme van verlaging van de waterproductie en verhoging van de uveosclerale uitstroom.23 Net als zijn voorganger heeft het een opmerkelijk allergiepercentage (tot 20%), dat kan optreden tot acht maanden na het begin van de therapie.22 Er zijn drie formuleringen ontwikkeld, elk met een vergelijkbare werkzaamheid: 0,2% met benzalkoniumchloride (BAK); en 0,15% en 0,1% met het conserveermiddel Purite.24 Allergan is sindsdien gestopt met de met BAK geconserveerde formulering.
The Straight Dope
Medische marihuana is de laatste tijd erg in het nieuws gekomen, dankzij een aantal wetswijzigingen in de Verenigde Staten. Hoewel het al sinds de jaren zeventig van de vorige eeuw wordt onderzocht als een methode om IOP te verlagen, hebben onderzoekers ontdekt dat het alleen gedurende korte perioden IOP kan verlagen. Dat, in combinatie met de nogal heftige bijwerkingen, maakt het een slechte kandidaat voor behandeling. Uit onderzoek blijkt echter dat het een rol kan spelen voor “eindstadium-glaucoompatiënten bij wie maximale medische behandeling en chirurgie zijn mislukt of die slechte chirurgische kandidaten zijn.”
Sun X, Xu C, Chadha N,et al. Marijuana for glaucoma: a recipe for disaster or treatment? Yale J Biol Med. 2015 Sep; 88(3): 265-9.
Hoewel bijwerkingen meestal correleren met prostaglandinegebruik, toont de literatuur brimonidine-geïnduceerde anterieure uveïtis.25 Duur varieerde van zeven dagen tot vijf jaar met een gemiddelde van bijna 20 maanden.
Prostaglandine-analogen
Deze zorgen voor de meest robuuste IOP-verlaging van alle druppels door de uveosclerale uitstroom van waterig water te bevorderen. Prostaglandine-analogen (PGA’s) binden zich aan receptoren in het ciliaire lichaam en induceren ontspanning van de gladde spieren, en veranderen de extracellulaire matrix in de ciliaire spier om de uitstroom van water via uveosclerale routes te bevorderen.26 PGA’s worden eenmaal daags toegediend, gewoonlijk voor het slapen gaan, en leveren een IOP-verlaging van 30% tot 35% op; tot de mogelijkheden behoren latanoprost, bimatoprost, travoprost en tafluprost (geleverd in een eenmalige dosis, zonder conserveermiddel).26 De meest voorkomende bijwerking van PGA’s is conjunctivale hyperemie, vaak in de eerste paar weken na het begin van de behandeling.26 Oogirritatie, verergering van bestaande ontstekingsaandoeningen (maculair oedeem, iritis), atrofie van het periorbitale vetkussen, pigmentatie van de perioculaire huid, wimpers en iris en hypertrichose kunnen ook worden waargenomen.26
Een nieuwe variant in de categorie prostaglandine-analogen is latanoprostene bunod 0,024%. Deze verbinding heeft een tweeledig mechanisme: het verhogen van de uveosclerale uitstroom en het verbeteren van de trabeculaire meshwork uitstroom door het effect van stikstofmonoxide.27 Het oog breekt latanoprostene bunod tweemaal af om de actieve componenten latanoprost zuur en stikstofmonoxide te verkrijgen.28 Het laatste heeft een effect op een signaalroute die de contractiele componenten in het TM ontspant, waardoor de uitstroom toeneemt.28 Het extra effect verlaagt de IOP >1 mm Hg vergeleken met latanoprost alleen over meerdere tijdstippen, met een totale IOP-verlaging die varieert van 7,5 mm Hg tot 9,1 mm Hg. Bijwerkingen met latanoprostene bunod waren vergelijkbaar met die van latanoprost alleen, met mogelijk minder perioculaire pigmentatie en hypertrichose, aldus de onderzoekers.28,29
ROCK Inhibitors
In een normaal oog is de belangrijkste drainageleiding voor kamervocht het TM. De weerstand van het waterige vocht door deze structuur is verhoogd bij patiënten met glaucoom, waardoor de IOP stijgt.30 Tot voor kort slaagden glaucoommedicijnen er niet in deze structuur aan te pakken. Dat veranderde in 2017 met de introductie van Rhopressa (netarsudil 0,02%, Aerie), een rho-kinase (ROCK) remmer.
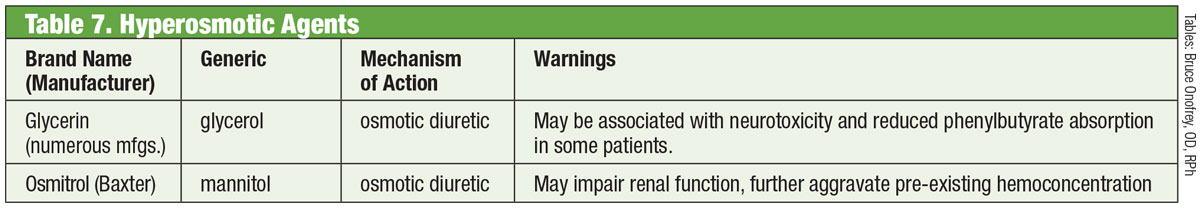
Tabel: Bruce Onofrey, OD, RPh. Klik op afbeelding om te vergroten.
Rho-kinase komt op grote schaal tot expressie in vele weefsels, waaronder het TM, waar het de assemblage van actine-stressvezels bevordert en de samentrekking van de cellen reguleert.31 ROCK-remmers verhogen de waterafvoer door de door actine en myosine gestuurde cellulaire contractie te verminderen en de productie van extracellulaire matrixeiwitten te verminderen.32 Rhopressa heeft ook een remmende werking op de noradrenaline-transporter (NET), waardoor het een ROCK/NET-remmer is. Het NET-mechanisme kan het gevolg zijn van een verminderde bloedtoevoer naar het ciliaire lichaam door noradrenaline-geïnduceerde vasoconstrictie, wat resulteert in een verminderde productie van water.33 Bovendien verlaagt netarsudil ook de episclerale veneuze druk (EVP), waardoor meerdere wegen voor IOP-verlaging worden geopend.32 De meest voorkomende oculaire bijwerking is oculaire hyperemie (ongeveer de helft van de behandelde patiënten), die voor het grootste deel mild, van voorbijgaande aard en zelfoplossend is.32
Opgemerkt moet worden dat rho zelf een belangrijke rol speelt bij de groei en geleiding van axonen en bij de regulering van het overleven en afsterven van neuronen.34 Onderzoekers ontdekten dat, na letsel aan de oogzenuw, de topische toepassing van netarsudil het afsterven van retinale ganglioncellen vermindert en de regeneratie van axonen bevordert.34
Getting in the Mix
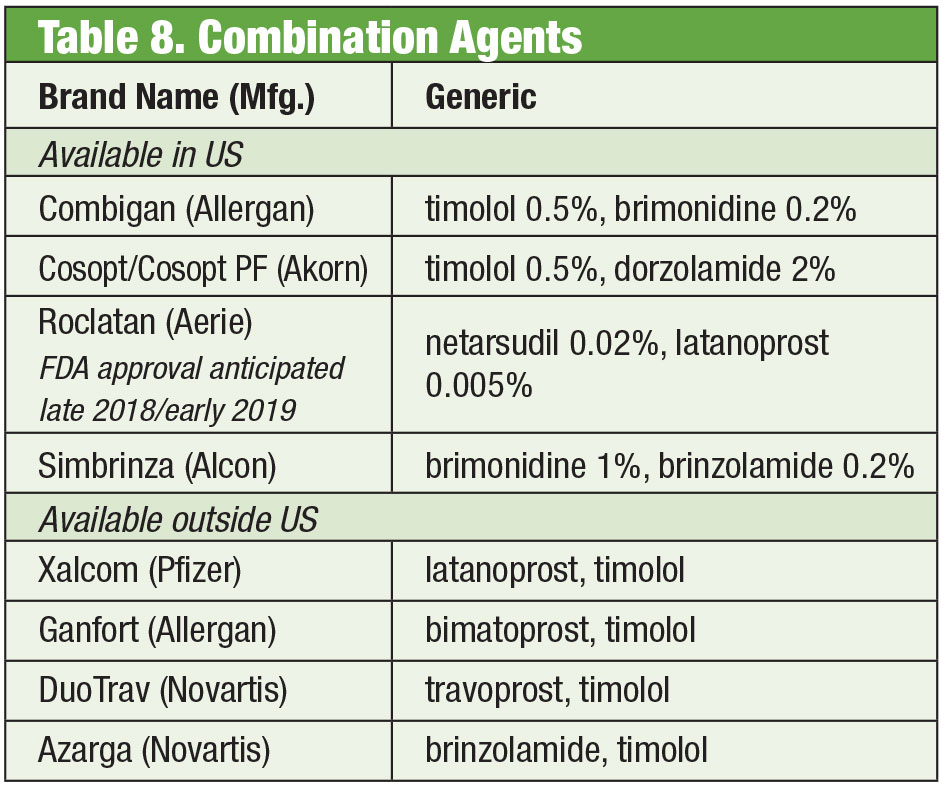
Soms hebben patiënten meer nodig dan wat kant-en-klare producten te bieden hebben. Gevoeligheid van de patiënt of toxiciteit van het oogoppervlak door chronisch gebruik van conserveermiddelen kan leiden tot een zoektocht naar alternatieven. Sommige samengestelde geneesmiddelen zijn conserveermiddelvrij verkrijgbaar. Als therapietrouw een probleem is, kunnen deze mengsels tot vier geneesmiddelen in één flesje bevatten. Bovendien worden veel vaste combinaties buiten de Verenigde Staten doeltreffend gebruikt, maar zijn zij momenteel niet goedgekeurd door de FDA; door magistrale bereidingen krijgen artsen in de VS toegang tot deze schema’s. Als de kosten een beperking vormen, kan magistrale bereidingen een extra voordeel zijn. Hoewel het magistrale bereidingsproduct vaak niet door de verzekering van de patiënt wordt gedekt, kan de prijs van één of twee combinatieproducten voordeliger zijn dan die van meerdere enkelvoudige geneesmiddelen, zelfs generieke formuleringen. Twee bereidingsapotheken bieden meerdere vooraf ingestelde variaties aan: Simple Drops van Imprimis Pharmaceuticals en de Omni productlijn van Ocular Science. Extra maatwerk is ook mogelijk bij elk van hen.
Hoewel de individuele middelen door de FDA zijn goedgekeurd, zijn bepaalde combinaties dat mogelijk niet. Het is aan de arts om de risico’s en voordelen van naleving af te wegen.
Gesamengestelde Glaucoomproducten:
Simple Drops (Imprimis Pharmaceuticals)
Alle verkrijgbare conserveermiddelvrije.
– Tim-Lat PF (timolol/latanoprost)
– Brim-Dor PF (brimonidine/dorzolamide)
– Tim-Brim-Dor PF (timolol/brimonidine/dorzolamide)
– Tim-Dor-Lat PF (timolol/dorzolamide/latanoprost)
– Tim-Dor-Lat PF (timolol/dorzolamide/latanoprost)
– Brim-Dor-Dor PF (timolol/dorzolamide/latanoprost)
.Brim-Dor-Lat PF (timolol/brinzolamide/dorzolamide/latanoprost)
– Dor-Tim (dorzolamide/timolol)
– Dorzolamide PF
– Latanoprost PF
Omni Druppels (Ocular Science)
Bevatten benzalkoniumchloride, maar in lagere concentraties (0.001%) dan de gebruikelijke generieke formuleringen (0,002%).
– Timolol/latanoprost
– Timol/brimonidine/dorzolamide (AM-formule)*
– Timol/brimonidine/dorzolamide/latanoprost (PM-formule)*
* Bedoeld om in combinatie met elkaar te worden gebruikt, waarbij in de AM-versie de prostaglandine ontbreekt, die gewoonlijk slechts eenmaal per dag wordt toegediend.
Vaste combinatieproducten
Ondanks de werkzaamheid van deze afzonderlijke producten is het bij veel glaucoompatiënten gebruikelijk dat zij meerdere therapieën nodig hebben om hun aandoening onder controle te houden.35 Wanneer een dubbele behandeling noodzakelijk is, kan het het beste zijn om dezelfde dispenser aan te bieden, wat de therapietrouw bevordert en de impact van toxiciteit op het oogoppervlak vermindert.36 Timolol wordt gecombineerd met brimonidine (als Combigan, Allergan) en dorzolamide (als Cosopt, Akorn), beide tweemaal daags gedoseerd, waarbij een conserveermiddelvrije optie beschikbaar is voor het timolol-dorzolamide product. Een andere tweemaal daagse combinatie – Simbrinza – koppelt brimonidine aan dorzolamide. De vaste combinaties tonen een goede werkzaamheid, zowel als primaire therapie als in aanvulling op PGA’s. De bijwerkingen zijn vergelijkbaar met die van de afzonderlijke componenten.
Trouw/Patiënt Perceptie
Hoewel de beslissing om een behandeling aan te bevelen complex kan zijn en van vele factoren afhangt, moeten, zodra de arts en de patiënt het eens zijn over het starten van een therapie, bepaalde achtergrondfeiten worden erkend en basisprincipes worden gehanteerd.
Klik op de afbeelding om te vergroten.
Vooruitgang van het gezichtsveld en de ernst van de ziekte hangen samen met slechte therapietrouw.37 Patiënten met chronische medische aandoeningen gebruiken gemiddeld 30% tot 70% van de voorgeschreven dosis geneesmiddelen en 50% stopt met de behandeling binnen de eerste maanden, zo blijkt uit één onderzoek.38 De therapietrouw bij glaucoommedicatie is vergelijkbaar met die bij andere chronische aandoeningen.38 Bijgevolg kan er een kloof bestaan tussen werkzaamheid en doeltreffendheid, waarbij, hoewel in grote klinische studies is aangetoond dat topische medicatie doeltreffend is, deze in de praktijk ondoeltreffend kan zijn omdat de patiënt zich er niet aan houdt.39
Belangrijke factoren die bijdragen tot slechte therapietrouw bij glaucoom zijn onder meer: bijwerkingen van medicatie, kosten van de therapie, voorlichting van de patiënt en de arts-patiënt relatie.40 Bovendien kan de ziekte asymptomatisch zijn tot laat in het beloop, waarbij men zich niet bewust is van gezichtsvelduitval.41
En nu iets heel anders
Medicijnen vormen al meer dan een eeuw de ruggengraat van de behandeling van glaucoom, en de ontwikkeling van nieuwe geneesmiddelen gaat onverminderd door. Maar sommige onderzoekers zijn op zoek naar alternatieven buiten de fles. Een bril met een elektromagnetisch spiraaltje, in combinatie met een contactlens die een spoor van goud bevat, zou ooit kunnen helpen om de IOP te verlagen. De combinatie, die is ontwikkeld door het bedrijf Bionode, is bedoeld om een elektrische stroom op te wekken die door de trilharen vloeit om de natuurlijke drainagepaden te stimuleren en de IOP te verlagen.
American Academy of Oogheelkunde. Bril kan op een dag glaucoom behandelen. www.aao.org/eye-health/news/eyeglasses-for-glaucoma-treatment. Accessed July 3, 2018.
Een extra barrière voor therapietrouw is het probleem met het inbrengen van druppels en het doseringsschema.42 80% van de patiënten verontreinigt zijn druppels door hun gezicht aan te raken, 61% brengt niet precies één druppel in en, het allerbelangrijkste, 37% mist het oog met de druppel.43 De arts mag er nooit van uitgaan dat de patiënt bedreven is in het inbrengen van druppels. Alvorens een druppelbehandeling te starten, moet u de patiënt leren hoe hij druppels moet toedienen en hem het toedienen laten demonstreren voor hij de praktijk verlaat. Dit kan efficiënt worden gedelegeerd aan een optometrische technicus en versterkt met een educatieve hand-out over techniek (afdrukbare PDF op www.glaucoma.org/treatment/eyedrop-tips.php), evenals het gebruik van video’s, zoals een geproduceerd door de Glaucoma Research Foundation (www.glaucoma.org/treatment/putting-in-eye-drops.php).
Als de patiënt grote moeite heeft met het toedienen van oogdruppels, kan een mechanisch doseringshulpmiddel de kans op succes vergroten. De therapietrouw aan het juiste doseringsschema verbetert door het gebruik van geautomatiseerde, op telecommunicatie gebaseerde herinneringen en herinneringsapps op smartphone en tablet.44,45 Een combinatie van in-office educatie, het stellen van doelen, een vereenvoudigd druppelschema en technologie moet worden omarmd om de therapietrouw te verbeteren.46 Het aanpakken van bekende barrières voor therapietrouw aan medicatie is een noodzakelijke eerste stap op weg naar succes.
Dropping the Pressure
IOP is de enige bekende modificeerbare risicofactor voor glaucoom, en het is onbetwistbaar bewezen dat het verlagen ervan het risico op ziekteprogressie vermindert.47,48 Het effectief verlagen van IOP wordt dus het doel bij de behandeling van patiënten met glaucoom. Nadat de ziekte nauwkeurig is geclassificeerd, wordt doorgaans een therapeutisch doel vastgesteld. In de Verenigde Staten wordt in de praktijk de voorkeur gegeven aan een IOP-doelbereik waarvan de arts denkt dat het het levenslange risico op blindheid van de patiënt zal verminderen en tegelijkertijd de belasting die de behandeling met zich meebrengt tot een minimum zal beperken.49-52
Hoewel meerdere methoden kunnen helpen bij het bepalen van een initieel doel IOP (drempel IOP, berekend, one size fits all), is de eenvoudigste en meest empirisch onderbouwde methode het verlagen van de IOP met een percentage ten opzichte van de dagpiek IOP op baseline waarbij schade aan de oogzenuw optreedt. IOP is dynamisch en vertoont korte- en langetermijnfluctuaties, waardoor de momenteel beschikbare tonometrie niet perfect reproduceerbaar is. Daarom wordt aanbevolen dat de arts vóór het begin van de behandeling meerdere IOP-metingen op verschillende tijdstippen van de dag verricht om te proberen een dagpiek IOP vast te stellen waarop het streefbereik kan worden gebaseerd.53-55 Maar als er niet meerdere 24-uurs IOP-curven worden verkregen, is het onwaarschijnlijk dat er ooit een echte piek kan worden gemeten. De arts zal uiteindelijk het succes van de behandeling moeten afmeten aan de mate waarin de structurele en functionele tests de progressie verminderen.48,56,57
Aanbevolen verminderingen van het IOP-percentage variëren van 20% tot 50%, afhankelijk van de aandoening (d.w.z, glaucoomverdachte, oculaire hypertensie, normale spanningsglaucoom, hoge spanningsglaucoom, hoeksluitingsglaucoom) basislijn ernst van ziekte, en levensverwachting.58-61
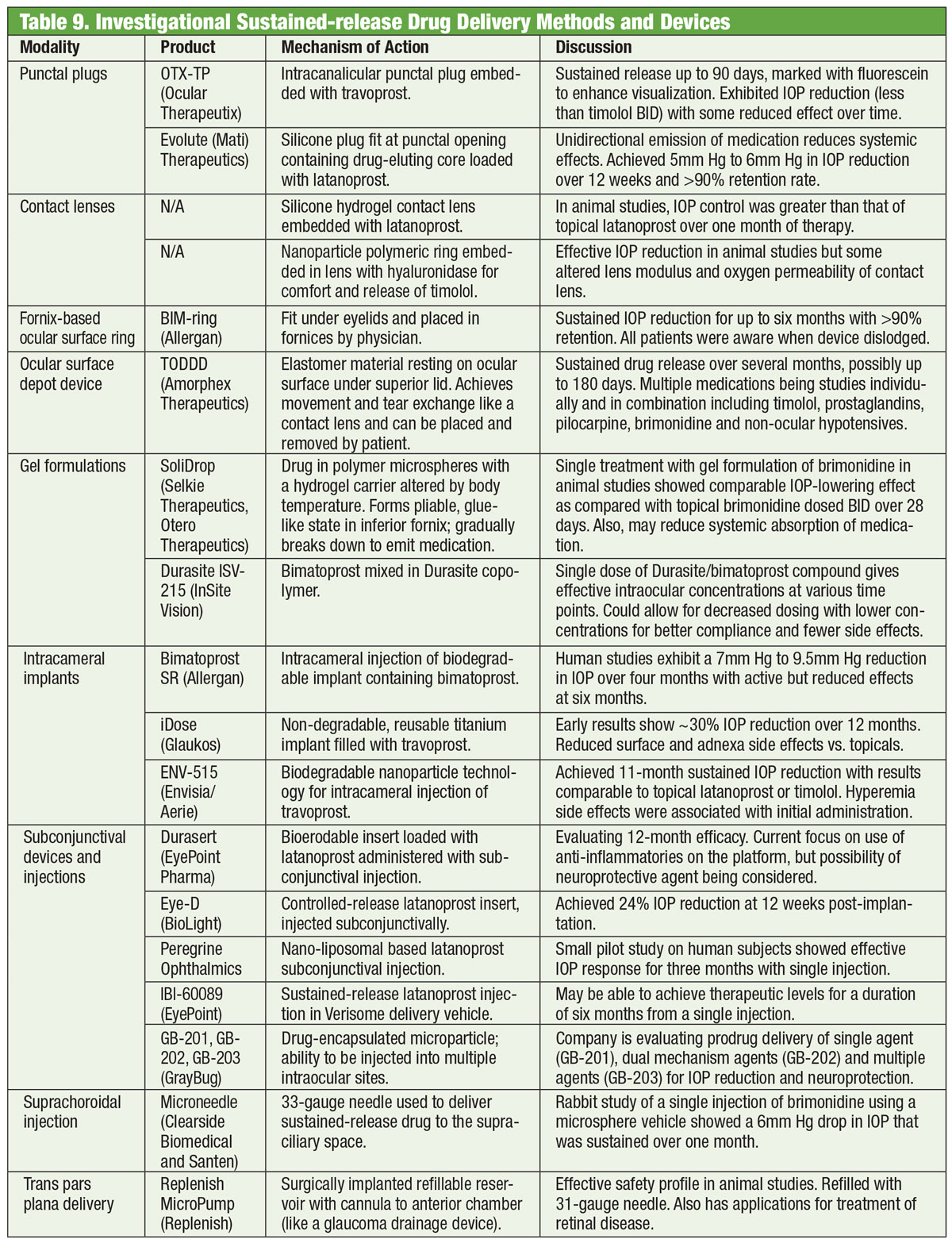
Tabel: Bruce Onofrey, OD, RPh. Klik op afbeelding om te vergroten.
Getting Started
PGA’s zijn goedgekeurd voor eerstelijnsbehandeling in de Verenigde Staten en zijn effectiever in het verlagen van IOP, hebben een relatief beperkt bijwerkingenprofiel en worden minder frequent (eenmaal daags) gedoseerd dan andere klassen van medicatie.62,63
Als een specifiek middel is gekozen, moet de patiënt na maximaal vier weken opnieuw worden gezien om de effectiviteit van de druppel te meten, eventuele bijwerkingen te voorkomen, de therapietrouw van de patiënt te waarborgen en de waarde van de behandeling te versterken.
Ultimately, proper education and vigilant follow-up with structural and functional testing will help minimize vision loss.
Dr. Dorkowski is klinisch coördinator voor het programma voor verpleeghuizen en begeleid wonen bij SCO.
Dr. Williamson is supervisor van de opleiding bij het Memphis VA Medical Center.
Dr. Rixon is arts-assistent bij de Memphis VA en is lid van de Optometric Glaucoma Society.
Dr. Onofrey is auteur van The Ocular Therapeutics Handbook.
1. Zimmerman TJ, William P. BogerIII. The beta-adrenergic blocking agents and the treatment of glaucoma. Surv Ophthalmol. 1979;23(6):347-62.
2. Realini T. A history of glaucoma pharmacology. Optom Vis Sci. 2011;88(1):36-8.
3. Erickson KA, Schroeder A. Direct effects of muscarinic agents on the outflow pathways in human eyes. Invest Ophthalmol Vis Sci. 2000;41(7):1743-8.
4. Drance S, Nash P. The dose response of human intraocular pressure to pilocarpine. Can J Ophthalmol. 1971;6(1):9-13.
5. Sears M. The mechanism of action of adrenergic drugs in glaucoma. Investig Opthalmology Vis Sci. 1966;5:115-9.
6. Mandell AI, Stentz F, Kitabchi AE. Dipivalyl epinephrine: a new pro-drug in the treatment of glaucoma. Ophthalmology. 1978;85(3):268-75.
7. Neufeld AH. Experimentele studies over het werkingsmechanisme van timolol. Surv Ophthalmol. 1979;23(6):363-70.
8. Coakes RL, Brubaker RF. The mechanism of timolol in lowering intraocular pressure: In the normal eye. Arch Ophthalmol. 1978;96(11):2045-8.
9. Trope GE, Clark B. Beta adrenergic receptors in pigmented ciliary processes. Br J Ophthalmol. 1982;66:788-92.
10. Wax MB, Molinoff PB. Distribution and properties of beta-adrenergic receptors in human iris-ciliary body. Invest Ophthalmol Vis Sci. 1987;28(3):420-30.
11. Allen RC, Hertzmark E, Walker AM, Epstein DL. A double-masked comparison of betaxolol vs timolol in the treatment of open-angle glaucoma. Am J Ophthalmol. 1986;101(5):535-41.
12. Novack GD. Ophthalmic beta-blockers since timolol. Surv Ophthalmol. 1987;31(5):307-27.
13. Soll DB. Evaluatie van timolol bij chronisch open-hoek glaucoom: Eenmaal daags versus tweemaal daags. Arch Ophthalmol. 1980;98(12):2178-81.
14. Topper JE, Brubaker RF. Effects of timolol, epinephrine, and acetazolamide on aqueous flow during sleep. Invest Ophthalmol Vis Sci. 1985;26(10):1315-9.
15. Krag S, Andersen HB, Sorensen T. Circadian intraocular pressure variation with beta-blockers. Acta Ophthalmol Scand. 1999;77(5):500-3.
16. Schuman JS. Effecten van systemische bètablokkertherapie op de werkzaamheid en veiligheid van topische brimonidine en timolol. Brimonidine Studiegroepen 1 en 2. Ophthalmology. 2000;107(6):1171-7.
17. Salim S, Shields MB. Glaucoom en systemische ziekten. Surv Ophthalmol. 2010;55(1):64-77.
18. Sugrue MF. Pharmacological and ocular hypotensive properties of topical carbonic anhydrase inhibitors. Prog Retin Eye Res. 2000;19(1):87-112.
19. Loftsson T, Jansook P, Stefansson E. Topical drug delivery to the eye: dorzolamide. Acta Ophthalmol. 2012;90(7):603-8.
20. Lester M. Brinzolamide ophthalmic suspension: a review of its pharmacology and use in the treatment of open angle glaucoma and ocular hypertension. Clin Ophthalmol. 2008;2(3):517-23.
21. Petounis A, Mylopoulos N, Kandarakis A, et al. Comparison of the additive intraocular pressure-lowering effect of latanoprost and dorzolamide when added to timolol in patients with open-angle glaucoma or ocular hypertension: a randomized, open-label, multicenter study in Greece. J Glaucoma. 2001;10(4):316-24.
22. Williams GC, Orengo-Nania S, Gross RL. Incidentie van brimonidine allergie bij patiënten die voorheen allergisch waren voor apraclonidine. J Glaucoma. 2000;9(3):235-8.
23. Lee DA, Gornbein JA. Effectiveness and safety of brimonidine as adjunctive therapy for patients with elevated intraocular pressure in a large, open-label community trial. J Glaucoma. 2001;10(3):220-6.
24. Cantor LB, Safyan E, Liu C-C, Batoosingh AL. Brimonidine-puriet 0,1% versus brimonidine-puriet 0,15% tweemaal daags bij glaucoom of oculaire hypertensie: een 12 maanden durend gerandomiseerd onderzoek. Curr Med Res Opin. 2008;24(7):2035-43.
25. Beltz J, Zamir E. Brimonidine geïnduceerde anterieure uveitis. Ocul Immunol Inflamm. 2016;24(2):128-33.
26. Toris CB, Gabelt BT, Kaufman PL. Update on the mechanism of action of topical prostaglandins for intraocular pressure reduction. Surv Ophthalmol. 2008;53 Suppl1:S107-20.
27. Liu JHK, Slight JR, Vittitow JL, Scassellati Sforzolini B, Weinreb RN. Efficacy of latanoprostene bunod 0.024% compared with timolol 0.5% in lowering intraocular pressure over 24 hours. Am J Ophthalmol. 2016;169:249-57.
28. Kaufman PL. Latanoprostene bunod ophthalmic solution 0.024% voor IOP verlaging bij glaucoom en oculaire hypertensie. Expert Opin Pharmacother. 2017;18(4):433-44.
29. Medeiros FA, Martin KR, Vrede J, Scassellati Sforzolini B, Vittitow JL, Weinreb RN. Comparison of latanoprostene bunod 0.024% and timolol maleate 0.5% in open-angle glaucoma or ocular hypertension: De LUNAR studie. Am J Ophthalmol. 2016;168:250-9.
30. Abu-Hassan DW, Acott TS, Kelley MJ. Het trabeculaire meshwork: A basic review of form and function. J Ocul Biol. 2014. fulltextarticles.avensonline.org/JOCB-2334-2838-02-0017. Accessed June 29, 2018.
31. Sturdivant JM, Royalty SM, Lin C-W, et al. Discovery of the ROCK inhibitor netarsudil for the treatment of open-angle glaucoma. Bioorg Med Chem Lett. 2016;26(10):2475-80.
32. Serle JB, Katz LJ, McLaurin E, et al. Two phase 3 clinical trials comparing the safety and efficacy of netarsudil to timolol in patients with elevated intraocular pressure: rho kinase elevated iop treatment trial 1 and 2 (ROCKET-1 and ROCKET-2). Am J Ophthalmol. 2018;186:116-27.
33. Lin C-W, Sherman B, Moore LA, et al. Discovery and preclinical development of netarsudil, a novel ocular hypotensive agent for the treatment of glaucoma. J Ocul Pharmacol Ther. 2018;34(1-2):40-51.
34. Shaw PX, Sang A, Wang Y, et al. Topische toediening van een rock/net inhibitor bevordert retinale ganglionceloverleving en axonregeneratie na oogzenuwletsel. Exp Eye Res. 2017;158:33-42.
35. Schmier JK, Hulme-Lowe CK, Covert DW. Adjunctieve therapiepatronen bij glaucoompatiënten die prostaglandine-analogen gebruiken. Clin Ophthalmol. 2014;8:1097-104.
36. Fechtner BYRD, Khouri AS. Vaste combinaties. Glaucoom Today. 2016;14(6)33-6.
37. Rossi G, Pasinetti G, Scudeller L, et al. Do adherence rates and glaucomatous visual field progression correlate? Eur J Ophthalmol. 2011;21(4):410-4.
38. Friedman DS, Quigley HA, Gelb L, et al. Using pharmacy claims data to study adherence to glaucoma medications: methodology and findings of the Glaucoma Adherence and Persistency Study (GAPS). Investig Ophthalmol Vis Sci. 2007;48(11):5052-7.
39. Jampel HD, Chon BH, Stamper R, et al. Effectiveness of intraocular pressure-lowering medication determined by washhout. JAMA Ophthalmol. 2014;132(4):390-5.
40. Susanna R, De Moraes CG, Cioffi GA, Ritch R. Waarom worden mensen (nog steeds) blind van glaucoom? Transl Vis Sci Technol. 2015;4(2):1.
41. Crabb DP. Een visie op glaucoom – Zien we het duidelijk? Eye. 2016;30(2):304-13.
42. Newman-Casey PA, Robin AL, Blachley T, et al. The most common barriers to glaucoma medication adherence: Een cross-sectioneel onderzoek. Ophthalmology. 2015;122(7):1308-16.
43. Davis SA, Sleath B, Carpenter DM, Blalock SJ, Muir KW, Budenz DL. Drop instillation and glaucoma. Curr Opin Ophthalmol. 2018;29(2):171-7.
44. Boland M, Chang DS, Frazier T, et al. Automated telecommunication-based reminders and adherence with once-daily glaucoma medication dosing: The automated dosing reminder study. JAMA Ophthalmol. 2014;132(7):845-50.
45. Waisbourd M, Dhami H, Zhou C, et al. De Wills eye glaucoma app: Interest of patients and their caregivers in a smartphone-based and tablet-based glaucoma application. J Glaucoma. 2016;25(9):e787-e791.
46. Joseph A, Pasquale LR. Attributen geassocieerd met adherentie aan glaucoom medische therapie en de effecten daarvan op glaucoom uitkomsten: An evidence-based review and potential strategies to improve adherence. Semin Ophthalmol. 2017;32(1):86-90.
47. Clement CI, Bhartiya S, Shaarawy T. New perspectives on target intraocular pressure. Surv Ophthalmol. 2014;59(6):615-26.
48. Sit AJ, Pruet CM. Personalizing intraocular pressure: Target intraocular pressure in the setting of 24-hour intraocular pressure monitoring. Asia-Pacific J Ophthalmol. 2016;5(1):17-22.
49. Jampel HD. Streefdruk bij glaucoomtherapie. J Glaucoma. 1997;6(2):133-8.
50. Fingeret M. Care of the patient with open-angle glaucoma. Am Optom Assoc. 2011;1:1-161.
51. Singh K, Shrivastava A. Early aggressive intraocular pressure lowering, target intraocular pressure, and a novel concept for glaucoma care. Surv Ophthalmol. 2008;53(6 SUPPL.):33-8.
52. Prum Jr. BE, Rosenberg LF, Gedde SJ, et al. Primary open-angle glaucoma Preferred Practice Pattern guidelines. Oogheelkunde. 2016;123(1):P41-P111.
53. Realini T, Weinreb RN, Wisniewski SR. Diurnal intraocular pressure patterns are not repeatable in the short term in healthy individuals. Ophthalmology. 2010;117(9):1700-4.
54. Florent Aptel, MD, PhDemail, Antoine Lesoin, MSc, Christophe Chiquet, MD, PhD, Nishal Aryal-Charles, MSc, Christian Noel, MD, Jean-Paul Romanet M. Long-term reproducibility of diurnal intraocular pressure patterns in patients with glaucoma. Ophthalmology. 2014:1998-2003.
55. Rotchford AP, Uppal S, Lakshmanan A, King AJ. Dag-tot-dag variabiliteit in intraoculaire druk bij glaucoom en oculaire hypertensie. Br J Ophthalmol. 2012;96(7):967-70.
56. Barkana Y, Anis S, Liebmann J, Tello C, Ritch R. Clinical utility of intraocular pressure monitoring outside of normal office hours in patients with glaucoma. Arch Ophthalmol. 2006;124(6):793-7.
57. Konstas AGP, Quaranta L, Mikropoulos DG, et al. Peak intraocular pressure and glaucomatous progression in primary open-angle glaucoma. J Ocul Pharmacol Ther. 2012;28(1):26-32.
58. Kass MA, Heuer DK, Higginbotham EJ, et al. The Ocular Hypertension Treatment Study: a randomized trial determines that topical ocular hypotensive medication delays or prevents the onset of primary open-angle glaucoma. Arch Ophthalmol. 2002;120(6):701-30.
59. Heijl A, Cristina Leske M, Bengtsson B, et al. Reduction of Intraocular Pressure and Glaucoma Progression: Results from the Early Manifest Glaucoma Trial. Arch Ophthalmol. 2002 Oct;120(10):1268-79.
60. AGIS7. De geavanceerde glaucoom interventie studie (AGIS): The relationship between control of intraocular pressure and visual field deterioration. Am J Ophthalmol. 2010;130:429-440.
61. Musch DC, Gillespie BW, Lichter PR, et al. Visual field progression in the collaborative initial glaucoma treatment study. The impact of treatment and other baseline factors. Ophthalmology. 2009;116(2):200-207.e1.
62. Albert A. Latanoprost in de behandeling van glaucoom. Clin Ophthalmol. 2014;(8):1967-85.
63. Stein JD, Shekhawat N, Talwar N, Balkrishnan R. Impact of the introduction of generic latanoprost on glaucoma medication adherence. Ophthalmology. 2015;122(4):738-47.
64. Weinreb RN, Ong T, Sforzolini BS, et al. A randomised, controlled comparison of latanoprostene bunod and latanoprost 0.005% in the treatment of ocular hypertension and open angle glaucoma: De VOYAGER studie. Br J Ophthalmol. 2015;99(6):738-45.