Lipofilie is wellicht de belangrijkste fysisch-chemische eigenschap van een potentieel geneesmiddel; zij speelt een rol bij de oplosbaarheid, de absorptie, de membraanpenetratie, de plasma-eiwitbinding, de distributie, de CNS-penetratie en de partitionering in andere weefsels of organen, zoals de lever, en is van invloed op de klaringsroutes. Het is belangrijk bij de ligandherkenning, niet alleen aan het doeleiwit, maar ook bij CYP450-interacties, HERG-binding en PXR-gemedieerde enzyminductie.
LogP is een onderdeel van Lipinski’s Regel van 5, een vuistregel om de oplosbaarheid en permeabiliteit te voorspellen die een surrogaat is geworden voor de geneesmiddelleeftijd.
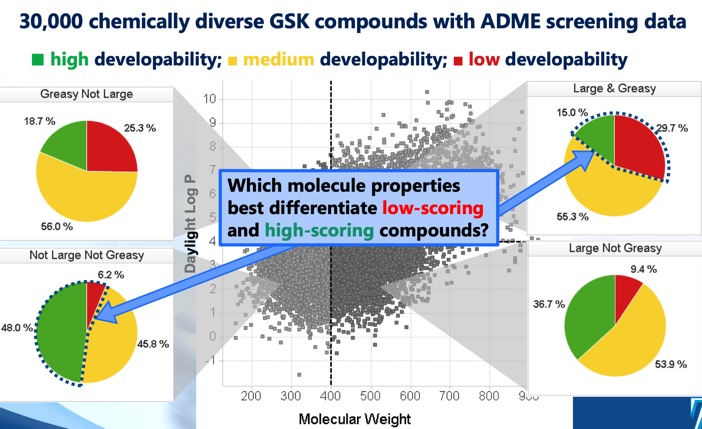
De ontwikkelingsscore DOI identificeert vier verschillende cLog P/moleculairgewicht-regio’s die de optimale en suboptimale chemische ruimte definiëren, en een ontwikkelingsscore die is afgeleid van regressiemodellen met behulp van screeningsgegevens over oplosbaarheid, permeabiliteit, eiwitbinding en 3A4-inhibitie. Hoewel de sector MWt <400, cLogP <4 de grootste kans op succes liet zien, werd opgemerkt dat zelfs de sector MWt >400, cLogP >4 enkele moleculen bevatte die voor ontwikkeling in aanmerking kwamen, zij het met een veel lagere kans op succes.
De meest gebruikte maat voor lipofiliteit is LogP, dit is de verdelingscoëfficiënt van een molecule tussen een waterige en lipofiele fase, gewoonlijk octanol en water.
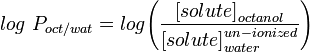
De meting van de LogP kan op verschillende manieren worden uitgevoerd; de meest gebruikelijke is de schudkolfmethode, waarbij een deel van de opgeloste stof in kwestie wordt opgelost in een volume octanol en water, gedurende enige tijd wordt geschud en vervolgens de concentratie van de opgeloste stof in elk oplosmiddel wordt gemeten. Dit kan tijdrovend zijn, vooral als er geen snelle spectroscopische methode is om de concentratie van het molecuul in de fasen te meten. Een snellere methode voor de bepaling van de log P maakt gebruik van hogedrukvloeistofchromatografie. De log P van een oplosmiddel kan worden bepaald door zijn retentietijd te correleren met soortgelijke verbindingen met een bekende log P waarde doi.
Berekening van de lipofiliteit
Over het algemeen is het niet praktisch om de log P van elke gemaakte verbinding experimenteel te bepalen (en het kan van belang zijn om de log P voorafgaand aan de synthese te berekenen) en dus worden berekende resultaten gebruikt, er zijn een aantal softwarehulpmiddelen beschikbaar, zowel desktop als online (niet gebruiken voor vertrouwelijke verbindingen).
Veel van deze toepassingen werken met behulp van een grote training data-set van bekende waarden voor het bepalen van fragment bijdragen voor substructuren en functionele groepen, maar logP is niet een eenvoudig additieve eigenschap en correctie termen zijn nodig om voor nabijheidseffecten, H-bonding, elektronische effecten, enz. zoals weergegeven in de voorbeelden hieronder.
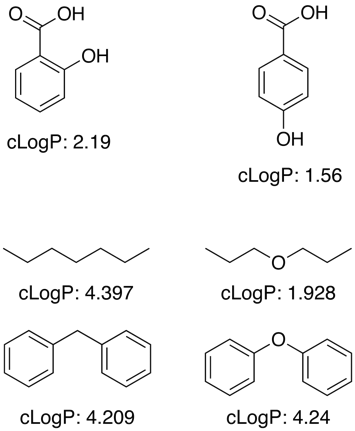
Voor onbekende functionele groepen de programma’s vaak bij benadering met behulp van individuele atoom bijdragen.
De verschillende methodologieën om logP te berekenen kunnen in drie verschillende benaderingen worden onderverdeeld.
Atomair (b.v. “AlogP”, ) &Versterkt Atomisch/Hybride (“XlogP”, “SlogP”)
Fragment (“ClogP”, KlogP, ACD/logP)
Op eigenschappen gebaseerde methoden (“MlogP”, “VlogP”, “MClogP”, “TlogP”)
Atomaire logP gaat ervan uit dat elk atoom een bijdrage levert aan de logP, en dat de bijdragen aan de uiteindelijke waarde zuiver additief zijn. Het is echter duidelijk dat een stikstof in een amide anders is dan een stikstof in een amine of pyridine, zodat Atomic rekening houdt met het atoomtype.
Fragmentmethoden maken gebruik van een grote trainingsdataset van bekende waarden om fragmentbijdragen voor substructuren en functionele groepen te bepalen, samen met correctietermen om rekening te houden met nabijheidseffecten. Deze methoden vallen vaak terug op atomaire modellen voor nieuwe functionele groepen.
Property-based methoden hebben de neiging om computationeel veeleisend en niet echt geschikt voor het testen van grote datasets.
Omdat de training sets en de algoritmen variëren tussen toepassingen is het zeer belangrijk niet te combineren berekende resultaten met behulp van verschillende tools.
Enkele van de tools stellen de gebruiker in staat om de trainingsset uit te breiden met behulp van in huis gemeten waarden, dit kan van cruciaal belang zijn bij het verkennen van nieuwe functionele groepen of scaffolds.
LogD
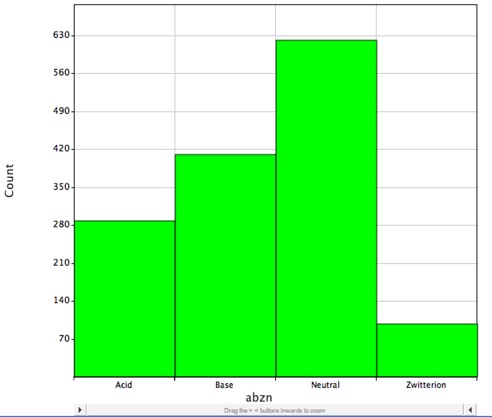
Het merendeel van de bekende geneesmiddelen bevat echter ioniseerbare groepen, zoals te zien is in het histogram hieronder, dit toont de verdeling van kleine moleculegeneesmiddelen met DrugBank en zijn waarschijnlijk geladen bij fysiologische pH en LogP beschrijft alleen correct de verdelingscoëfficiënt van neutrale (niet-geladen) moleculen.
LogD de verdelingsconstante is een betere descriptor van de lipofiliteit van een molecuul. Deze kan op soortgelijke wijze worden bepaald als LogP, maar in plaats van met water wordt de waterige fase met behulp van een buffer op een specifieke pH gebracht. Log D is dus pH-afhankelijk, zodat moet worden aangegeven bij welke pH de log D is gemeten. Van bijzonder belang is de log D bij pH = 7,4 (de fysiologische pH van bloedserum).
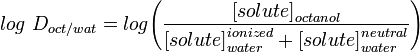
Applicaties zoals Marvin stellen de gebruiker in staat de log D te berekenen, maar ook het pH-distributieprofiel weer te geven, zoals hieronder getoond voor Warfarin.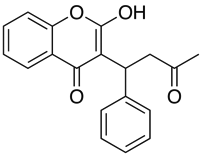
Voor verbindingen met een pKa dicht bij de fysiologische pH kan het van cruciaal belang zijn na te gaan wat eigenlijk de overheersende geïoniseerde vorm zou kunnen zijn.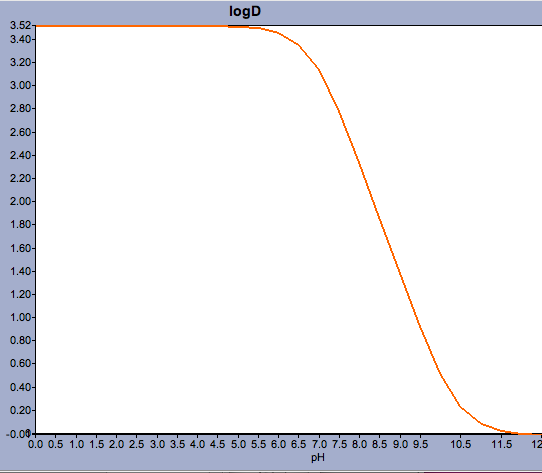
Dit kan ook waardevol zijn bij absorptie uit de verschillende delen van het spijsverteringskanaal, waar de pH varieert van 1-3 in de maag tot 7-8 in de ileum.
De bijdragen van verschillende functionele groepen aan LogD zijn onderzocht “LogD contributions of substituents common used in medicinal chemistry” DOI, deze studie maakte gebruik van gematchte moleculaire parenanalyse van experimentele LogD-waarden van enkele duizenden verbindingen die met de shake-flask-methode bij pH = 7,4 waren verzameld. Zij rapporteerden het gemiddelde deltaLogD-verschil voor bepaalde moleculaire paren en de resultaten worden hieronder getoond voor het geval dat de functionele groep zich op een willekeurige plaats aan de fenylring bevindt. Ik heb ook de berekende LogD met Chemaxon software bijgevoegd.
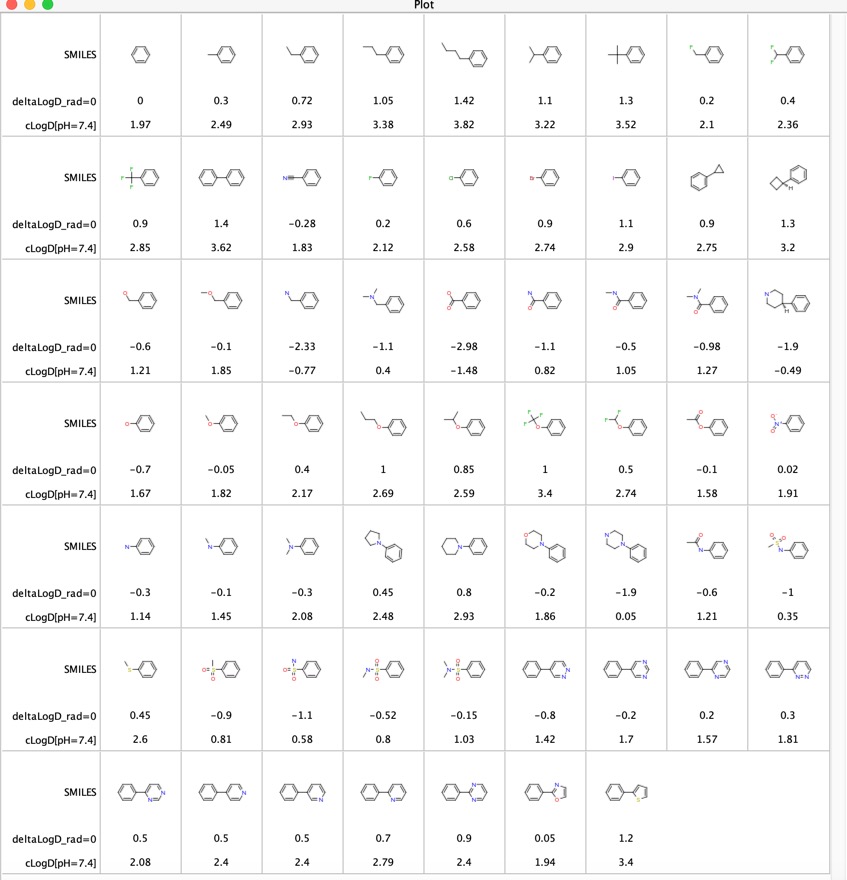
Dit is een nuttige tabel voor het vergelijken van functionele groepen, met name de laatste 11 regels vergelijken de invloed van verschillende heterocyclische groepen op de LogD. Deze heterocyclen worden vaak gebruikt als bio-isosterische vervangers voor een fenylring.
Ik dacht dat het misschien interessant zou zijn om de LogD verschillen bepaald met behulp van de gematchte moleculaire paren (deltaLogD_rad=0) te vergelijken met de waarden bepaald met behulp van de Chemaxon berekende LogD (deltacLogD). Zoals u hieronder kunt zien, is er een vrij goede overeenkomst.
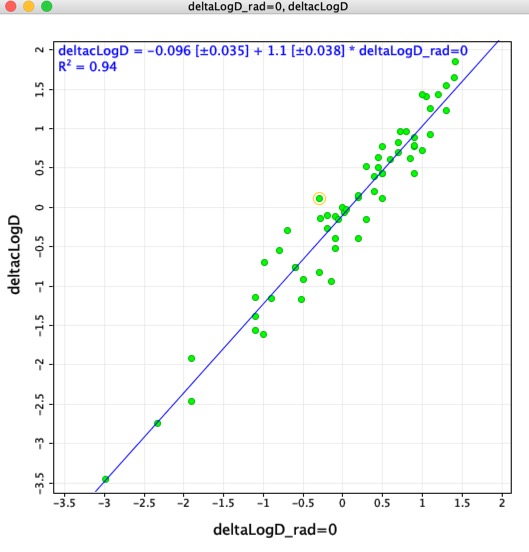
Omdat de trainingssets en de algoritmen per toepassing verschillen, is het zeer belangrijk om berekende resultaten met verschillende tools niet te combineren.
Het is belangrijk om er omzichtig mee om te gaan dat een verbetering van de bindingsaffiniteit niet volledig wordt aangedreven door een toename van de LogD, het is vaak nuttig om gewoon de bindingsaffiniteit tegen LogD uit te zetten. De interessantste modificaties van verbindingen zijn niet noodzakelijk die welke de grootste toename van de affiniteit geven, maar kunnen die zijn welke een toename van de affiniteit geven zonder een overeenkomstige toename van de lipofiliteit. In onderstaande tabel staan een aantal verbindingen met een zeer hoge affiniteit
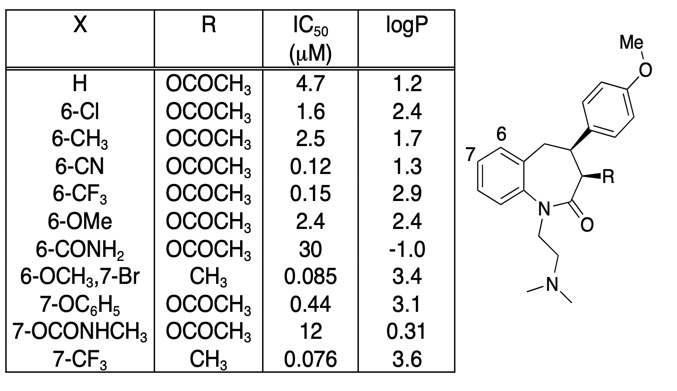
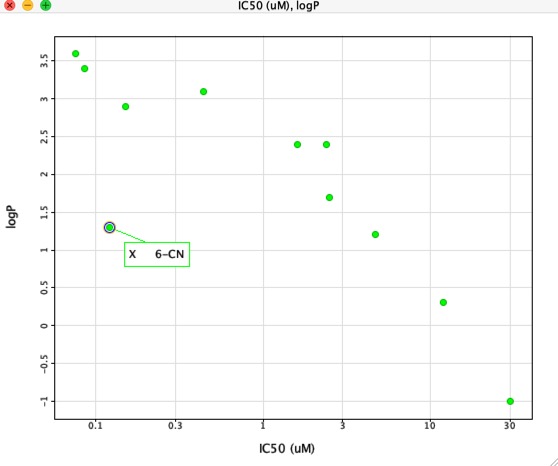
Maar als we IC50 uitzetten tegen LogP, zoals hieronder te zien is, is er een zeer duidelijke correlatie tussen LogP en IC50, hoewel één verbinding duidelijk anders is. De 6-CN substituent geeft een toename in affiniteit zonder een overeenkomstige toename in LogP.
Lipofilie is ook een belangrijke component Veel van de off-target passiva, waaronder binding aan plasma-eiwitten (met name albumine), HERG, CYP-interacties, transporters, hebben een sterke correlatie met lipofilie, en er is een aantal studies geweest waarin een hoge logP in verband wordt gebracht met de waarschijnlijkheid dat verbindingen in de ontwikkeling mislukken als gevolg van slechte ADMET-kenmerken (absorptie, distributie, metabolisme, uitscheiding en toxiciteit). Daarentegen is het vaak duidelijk dat een bepaalde grootte en lipofiliteit vereist is om een redelijk niveau van affiniteit te bereiken. Het vinden van een evenwicht tussen deze eisen is een belangrijke uitdaging bij het ontdekken van geneesmiddelen en de suggestie is dat chemici zich richten op de sweet spot MWt 250-500 en LogP 2-4. Een gevolg van deze aanpak is dat bij screening prioriteit moet worden gegeven aan verbindingen met een laag molecuulgewicht en minder lipofiele verbindingen. De eerste focus van de medicinale chemie zou moeten liggen op het selecteren van startpunten van goede kwaliteit en vervolgens op het effectief controleren van verschuivingen in fysisch-chemische eigenschappen tijdens het optimalisatieproces.
Worth reading
Finding the sweet spot: the role of nature and nurture in medicinal chemistry DOI
Lipophilic efficiency: the most important efficiency metric in medicinal chemistry DOI
Last Updated 12 January 2019