US Pharm. 2018;43(12):HS-2-HS-6.
ABSTRACT: Gastro-intestinale bloedingen (GIB’s) zijn een belangrijke bron van ziekenhuisopnames in de Verenigde Staten. GIB’s worden ingedeeld in twee typen: gastro-intestinale bloedingen in de bovenbuik en gastro-intestinale bloedingen in de onderbuik. Elk type kan zich presenteren met verschillende kenmerkende presentaties en vereisen een verschillende behandeling. Bovenste GIB is afhankelijk van endoscopische therapie en kan baat hebben bij verschillende farmacologische behandelingen in specifieke scenario’s, zoals protonpompremmers en macroliden. De behandeling van lagere GIB is gericht op colonoscopie en mechanische behandeling van bloedingen, met weinig farmacologische interventie. Apothekers kunnen deze patiënten op meerdere punten van de patiëntenzorg effectief van dienst zijn.
Gastro-intestinale bloedingen (GIB) zijn een relatief vaak voorkomend medisch probleem, dat jaarlijks een aanzienlijk deel van de morbiditeit, ziekenhuisopnames en zelfs mortaliteit in de Verenigde Staten veroorzaakt. Het ruwe geschatte tarief van ziekenhuisopname secundair aan om het even welk type van GIB in de V.S. wordt geschat op ongeveer 375 per 100.000 per jaar.1-3 Voor acute GIB-gebeurtenissen identificeren sommige studies een 30-dagen mortaliteitspercentage van 14%, terwijl andere een bereik tussen 6% en 10% per jaar rapporteren, met percentages die toenemen bij patiënten met gevorderde leeftijd en een hoger aantal geassocieerde onderliggende comorbiditeiten.4-7 Geschat wordt dat jaarlijks meer dan 2,5 miljard dollar wordt uitgegeven voor de intramurale behandeling van GIB.8
Gezien de aard van GIB is het belangrijk om de ziektetoestand te onderscheiden, aangezien de plaats van de bloeding zowel de presentatie als de behandeling kan dicteren (TABELLEN 1-3). Historisch werd het onderscheid tussen upper GIB (UGIB) en lower GIB (LGIB) gebaseerd op de plaats van de bloeding ten opzichte van het ligament van Treitz.9,10 Met deze definitie wordt een bloeding proximaal van het ligament van Treitz gecategoriseerd als een UGIB, terwijl een bloeding distaal van het ligament van Treitz wordt gecategoriseerd als een LGIB. Hoewel in sommige literatuur andere definities bestaan, is deze definitie in de meeste praktijken algemeen gangbaar.11,12



Bij de presentatie is de workup van elk verdacht GIB in eerste instantie gelijk, ongeacht de oorsprong van de bloeding. Onmiddellijke evaluatie moet zich richten op de hemodynamische stabiliteit van de patiënt. Deze prioriteit is goed vastgesteld in andere hemorragische modellen en blijft waar in gevallen van GIB.16-18 Lichamelijke beoordeling van bloeddruk, hartslag en orthostatische status moet worden uitgevoerd, en reanimatie moet worden uitgevoerd indien nodig. Deze reanimatie moet beginnen met intraveneuze vloeistoffen, maar kan ook transfusies van verpakte rode bloedcellen vereisen.
Toegevoegde beoordeling van patiënten die zich presenteren met GIB moet een gerichte anamnese van de patiënt omvatten, gericht op het identificeren van de aard, de duur en de mogelijke bron van de bloeding, evenals laboratoriumonderzoek (CBC, BMP, stollingsonderzoek).17,18 Bij de evaluatie van deze patiënten vanuit het oogpunt van de apotheker is het belangrijk om huidig of recent medicatiegebruik op te merken dat het risico op bloedingen kan verhogen, met inbegrip van middelen zoals niet-steroïde anti-inflammatoire geneesmiddelen, antiplateletmiddelen en/of anticoagulantia. Vroegtijdige identificatie van deze factoren kan zowel de diagnose als de juiste behandeling bespoedigen.
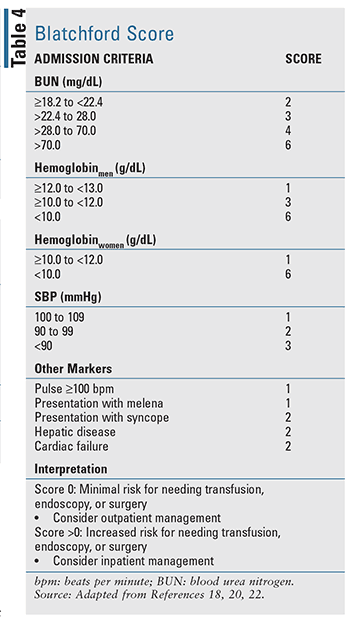
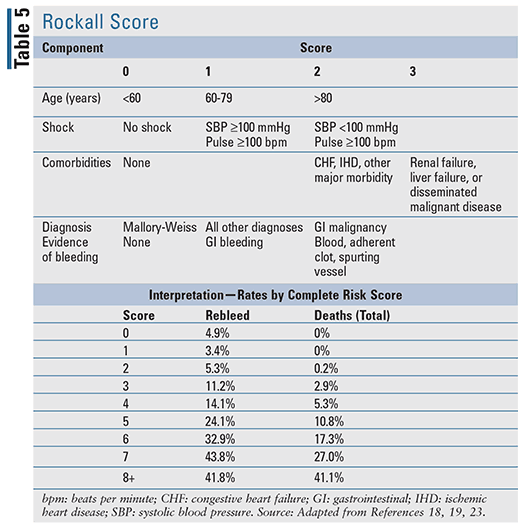
Risicobeoordeling en -stratificatie is klinisch nuttig om patiënten met een hoog en laag risico op ongunstige uitkomsten te helpen onderscheiden.17,18 Door patiënten in geëvalueerde risicogroepen te stratificeren, kan een eerste geïnformeerde besluitvorming worden gemaakt. Stratificatie kan met name inzicht verschaffen in factoren zoals het tijdstip van endoscopie of colonoscopie, het noodzakelijke niveau van zorg en het tijdstip van ontslag. Voor patiënten met acute UGIB zijn er verschillende klinische voorspellingsinstrumenten ontwikkeld, waaronder twee goed geëvalueerde instrumenten die worden aangehaald in evidence-based richtlijnen: de Blatchford-score (TABEL 4) en de Rockall-score (TABEL 5).17-20 De Rockall-score maakt gebruik van klinische gegevens onmiddellijk bij de presentatie.19 Factoren die de ernst van de bloeding beoordelen, zoals systolische bloeddruk en hartslag, worden beoordeeld naast patiëntkenmerken, zoals leeftijd en comorbide aandoeningen, wat resulteert in een instrument om prognostische uitkomsten en mogelijk mortaliteit te beoordelen. Op dezelfde manier maakt de Blatchford-score gebruik van zowel klinische als laboratoriumgegevens om het risico op interventie en mortaliteit te helpen voorspellen.20 Voor acute LGIB zijn de beschikbare prognostische regels om het risico te beoordelen beperkt en minder gevalideerd in vergelijking met UGIB.22
Farmacotherapie voor bovenste gastro-intestinale bloedingen
Protonpompremmers (PPI’s) zijn de geneesmiddelenklasse die het meest geassocieerd wordt met de behandeling van UGIB. Bij een UGIB-patiënt kan maagzuur de aggregatie van bloedplaatjes remmen en de potentiële coagulatie verzwakken, wat leidt tot een verminderd stoppen van de bloeding. Om dit proces te remmen, kan remming van de maagzuursecretie, bedoeld om de pH-waarde van de maag te verhogen tot 6 of hoger, helpen om stolsels te stabiliseren en de klinische uitkomsten te verbeteren.24
PPI’s zijn uniek in die zin dat ze zowel pre- als postendoscopie potentiële toepassing hebben. In de setting van pre-endoscopie vormen richtlijnen geen consensus over hun gebruik, maar ze kunnen het aandeel van patiënten met een hoog risico op stigmata van bloeding op het moment van de procedure verminderen.25 Ondanks potentieel voordeel in deze populatie, suggereert bewijs dat het gebruik van PPI’s geen invloed heeft op rebloedingen, noodzakelijke chirurgie of mortaliteit, wat leidt tot enige klinische controverse over hun toepassing. Bij patiënten bij wie endoscopie niet kan worden uitgevoerd of wordt uitgesteld, is echter aangetoond dat het gebruik van PPI’s het risico op een nabloeding kan verlagen. Er zijn aanwijzingen dat PPI’s de incidentie van hoogrisicostigmata van bloedingen op het moment van endoscopie verminderen, maar geen invloed hebben op herbloeding, noodzakelijke chirurgie of mortaliteit.17,26 PPI’s kunnen na endoscopische therapie zowel acuut als chronisch worden gebruikt.17
Continue infusie Versus Intermitterende PPI
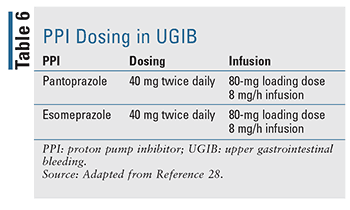
De juiste dosering en toediening van PPI’s zijn de laatste jaren nauwkeurig geëvalueerd (TABEL 6). Een IV-bolusdosis gevolgd door een infuus was lang de normale therapie en blijft de voorkeursbehandeling in de momenteel beschikbare richtlijnen, maar uit gegevens blijkt dat tweemaal daags IV-bolusdosering niet inferieur is wat betreft rebloedingen, mortaliteit en verblijfsduur in het ziekenhuis.17,27 Recente literatuur heeft aangetoond dat intermitterend gebruik van PPI niet inferieur was en een duidelijk voordeel biedt wat betreft geneesmiddeldosering, kosten en gebruik van middelen. De auteurs stellen voor dat de richtlijnen worden bijgewerkt om intermitterende PPI-therapie aan te bevelen bij endoscopisch behandelde GIB.27 In de praktijk geven veel instellingen nu de voorkeur aan intermitterende dosering om het gebruik van middelen en de totale kosten te verlagen.
Intraveneuze PPI Versus Intraveneuze H2-antagonisten
Omdat H2-antagonisten (H2A’s) met vergelijkbare intentie worden gebruikt in andere ziektetoestanden, is hun gebruik bij UGIB onderzocht naast PPI’s. Een meta-analyse uit 2015 waarin de twee klassen werden geëvalueerd in de setting van UGIB, vond dat terwijl het verschil in mortaliteit niet significant werd gevonden, uitkomsten zoals recidiefbloedingspercentage en het percentage dat chirurgie onderging een duidelijk voordeel lieten zien bij PPI’s. Dit tekort is waarschijnlijk te wijten aan de inferioriteit van H2A’s bij het handhaven van de pH-waarde van de maag boven 6,0, de pH-waarde bij benadering waarbij stollingsprocessen kunnen functioneren.29
Macroliden
In een poging om de visualisatie tijdens endoscopie te verbeteren en zo de noodzaak van herhaalde endoscopie te verminderen, wordt IV erytromycine, een antimicrobiële macrolide die ook werkt als een prokinetisch middel, vaak gebruikt. Een eenmalige dosis van 250 mg of 3 mg/kg wordt over het algemeen goed verdragen.17,30 Een meta-analyse uit 2016 concludeerde dat het gebruik van erytromycine voorafgaand aan endoscopie de noodzaak voor second-look endoscopie en de lengte van het ziekenhuisverblijf aanzienlijk verminderde, en daarom draagt het een aanbeveling om te worden gebruikt in de European Society of Gastrointestinal Endoscopy-richtlijnen.30,31
Het is eerlijk om zich af te vragen of het mogelijke voordeel een klasse-effect is of specifiek voor erytromycine. Azitromycine, een macrolide die over het algemeen vaker wordt gebruikt, is geëvalueerd en lijkt een niet-inferieur alternatief voor erytromycine te zijn. Azitromycine kan enkele logistieke voordelen hebben, zoals het feit dat het niet opnieuw moet worden samengesteld en over het algemeen beter beschikbaar is door het gebruik ervan bij de empirische behandeling van pneumonie.32
H pylori Behandeling
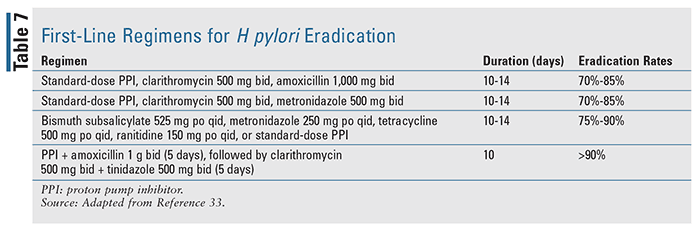
Patiënten bij wie een bloeding wordt vastgesteld die gepaard gaat met een Helicobacter pylori-infectie, moeten worden behandeld via eradicatietherapie op basis van richtlijnen, met als doel de infectie volledig op te lossen.17 Uit de beschikbare literatuur blijkt dat eradicatie van H pylori aanzienlijk doeltreffender is dan alleen antisecretiebehandeling bij patiënten met UGIB. De eerstelijnsregimes voor H pylori-eradicatie worden beschreven in TABEL 7, gebaseerd op de richtlijnen van het American College of Gastroenterology voor de behandeling van H pylori-infectie.33 Zodra de infectie is opgelost, hoeft deze groep patiënten doorgaans geen onderhoudsantisecretoire therapie te krijgen, tenzij zij niet-steroïde anti-inflammatoire geneesmiddelen of antitrombotische therapie nodig hebben, waarbij langdurige antisecretoire therapie noodzakelijk is, aangezien het gebruik ervan het risico op een nabloeding aanzienlijk kan verhogen.17,18
Behandelingsoverzicht
Na de initiële beoordeling en risicostratificatie en zodra de patiënt hemodynamisch stabiel is, is colonoscopie voorafgegaan door colonreiniging de initiële diagnostische procedure voor de meeste patiënten die zich presenteren met een LGIB.21 De behandeling van LGIB omvat meestal niet-farmacologische interventies; er zijn echter nog steeds mogelijkheden voor apothekers om betrokken te zijn bij de patiëntenzorg.
PPI-toepassing bij LGIB
In tegenstelling tot UGIB toont de beschikbare literatuur die PPI-gebruik bij LGIB evalueert, geen voordeel aan. Trials die UGIB en LGIB evalueren, hebben aangetoond dat PPI’s geen betere resultaten opleveren bij LGIB, maar dat ze het risico op LGIB kunnen verhogen.34 De theoretische mechanismen voor dit verhoogde risico zijn vaak gericht op mogelijke veranderingen in de microbiota, en kunnen dus het mogelijke risico van NSAID’s versterken. Deze uitkomsten zijn controversieel gebleken; zij bieden echter bewijs dat patiënten met LGIB geen baat hebben bij PPI-therapie. Dit potentiële risico moet zorgvuldig worden beoordeeld bij patiënten, met name die met een risico op UGIB, omdat risico versus voordeel zorgvuldig moet worden afgewogen.34
Rol van de apotheker
Pharmaceuten van vele specialismen bevinden zich in een unieke positie om te helpen bij de behandeling en het beheer van GIB-patiënten. Poliklinische apothekers bevinden zich in een uitstekende positie om proactief te letten op potentiële risicofactoren bij patiënten, waaronder hoge doses NSAID’s en anticoagulantia, en de kans op GIB in de frontlinie te verkleinen. Bovendien kunnen zij belangrijke adviezen geven en de dosis voor patiënten optimaliseren, zowel voor als na de diagnose van GIB. Op dezelfde manier kunnen klinische apothekers in ziekenhuizen een grote rol spelen bij de behandeling van GIB. Zij kunnen op meerdere gebieden assisteren tijdens de initiële evaluatie en behandeling. De initiële medicatie reconciliatie kan details aan het licht brengen die relevant zijn voor de diagnose en behandeling van patiënten, zoals het identificeren van poliklinisch gebruik van NSAID of anticoagulantia. Apothekers kunnen ook aanbevelingen doen aan het zorgteam over welke medicatie voordeel kan bieden voor elk GIB-geval.
1. El-Tawil A. Trends in gastro-intestinale bloedingen en mortaliteit: waar staan we? World J Gastroenterol. 2012;18(11):1154-1158.
2. Zhao Y, Encinosa W. Ziekenhuisopnames voor gastro-intestinale bloedingen in 1998 en 2006. Statistical Brief #65. Healthcare Cost and Utilization Project (HCUP) statistical briefs. December 2008.
3. Whelan CT, Chen C, Kaboli P, et al. Upper versus lower gastrointestinal bleeding: a direct comparison of clinical presentation, outcomes, and resource utilization. J Hosp Med. 2010;5(3):141-147.
4. Wilcox CM, Cryer BL, Henk HJ, et al. Mortality associated with gastrointestinal bleeding events: comparing short-term clinical outcomes of patients hospitalized for upper GI bleeding and acute myocardial infarction in a US managed care setting. Clin Exp Gastroenterol. 2009;2:21-30.
5. Garcia Rodriguez LA, Ruigómez A, Hasselgren G, et al. Comparison of mortality from peptic ulcer bleed between patients with or without peptic ulcer antecedents. Epidemiologie. 1998;9(4):452-456.
6. Wilcox CM, Clark WS. Causes and outcome of upper and lower gastrointestinal bleeding: the Grady Hospital experience. South Med J. 1999;92:44-50.
7. Yavorski RT, Wong RK, Maydonovitch C, et al. Analysis of 3,294 cases of upper gastrointestinal bleeding in military medical facilities. Am J Gastroenterol. 1995;90:568-573.
8. Johanson JF. Het beteugelen van de kosten van GI bloedingen. Am J Gastroenterol. 1998;93:1384-1385.
9. Scottish Intercollegiate Guidelines Network (SIGN). Management van acute bovenste en onderste gastro-intestinale bloedingen. September 2008. www.sign.ac.uk/assets/sign105.pdf.
10. Kim, SK, Cho CD, Wojtowycz AR. Het ligament van Treitz (het opschortende ligament van het duodenum): anatomische en radiografische correlatie. Abdom Imaging. 2008;33:395-397.
11. Matthew B, et al. Diagnosis of gastrointestinal bleeding: a practical guide for clinicians. World J Gastrointest Pathophysiol. 2014;5(4):467-478.
12. Raju GS, et al. American Gastroenterological Association (AGA) Institute medical position statement on obscure gastro-intestinale bloedingen. Gastroenterology. 2007;133(5):1694-1696.
13. Tielleman T, Bujanda D, Cryer B, et al. Epidemiologie en risicofactoren voor bovenste gastro-intestinale bloedingen. Gastrointest Endosc Clin N Am. 2015;25(3):415-428.
14. Rodriguez-Hernandez H, Rodríguez-Morán M, González JL, et al. Risicofactoren geassocieerd met bovenste gastro-intestinale bloedingen en met mortaliteit. Rev Med Inst Mex Seguro Soc. 2009;47(2):179-184.
15. Strate L. Lagere gastro-intestinale bloedingen: epidemiologie en diagnose. Gastroenterol Clin North Am. 2005;34(4):643-664.
16. Cocchi MN, Kimlin E, Walsh M, et al. Identification and resuscitation of the trauma patient in shock. Emerg Med Clin N Am. 2007;25:623-642.
17. Laine L, Jensen DM. Management of patients with ulcer bleeding. Am J Gastroenterol. 2012;107:345-360.
18. Siau K, Chapman W, Sharma N, et alManagement of acute upper gastrointestinal bleeding: an update for the general physician. J R Coll Physicians Edinb. 2017;47:218-230.
19. Rockall T, Logan R, Devlin H, et al. Risk assessment after acute upper gastrointestinal haemorrhage. Gut. 1996;38:316-321.
20. Blatchford O, Murray W, Blatchford M. A risk score to predict need for treatment for uppergastrointestinal haemorrhage. Lancet. 2000;356:1318-1321.
21. Recio-Ramirez, JM, Sánchez-Sánchez Mdel P, Peña-Ojeda JA, et al. De voorspellende capaciteit van de Glasgow-Blatchford score voor de risicostratificatie van bovenste gastro-intestinale bloedingen op een spoeddienst. Revista Española de Enfermedades Digestivas. 2015;107(5):262-267.
22. Strate L, Grainek IM. ACG Klinische Richtlijn: Management of Patients With Acute Lower Gastrointestinal Bleeding. Am J Gastroenterol. Advance online publication March 1, 2016. 2016;111:459-474.
23. Bessa X, O’Callaghan E, Balleste B, et al. Toepasbaarheid van de Rockall-score bij patiënten die endoscopische therapie ondergaan voor een bovenste gastro-intestinale bloeding. Dig Liver Dis. 2006;38:12-17.
24. Chaimoff C, Creter D, Djaldetti M. The effect of pH on platelet and coagulation factor activities. Am J Surg. 1978;136(2):257-259.
25. Sreedharan A, Martin J, Leontiadis GI, et al. Proton pump inhibitor treatment initiated prior to endoscopic diagnosis in upper gastrointestinal bleeding. Cochrane Database Syst Rev. 2010(7):CD005415.
26. Leontiadis GI , Sharma VK , Howden CW. Proton pump inhibitor therapy for peptic ulcer bleeding: Cochrane collaboration meta-analysis of randomized controlled trials. Mayo Clin Proc. 2007;82:286-296.
27. Sachar H, Vaidya K, Laine L, et al. Intermittent vs continuous proton pump inhibitor therapy for high-risk bleeding ulcers: a systematic review and meta-analysis. JAMA Intern Med. 2014;174(11):1755-1762.
28. Cheng H, Sheu B. Intraveneuze protonpompremmers voor peptische ulcusbloedingen: klinische voordelen en beperkingen. World J Gastrointest Endosc. 2011;3(3):49-56.
29. Zhang YS, Li Q, He BS, et al. Proton pump inhibitors therapy vs H2 receptor antagonists therapy for upper gastrointestinal bleeding after endoscopy: a meta-analysis. World J Gastroenterol. 2015;21(20):6341-6351.
30. Rahman R, Nguyen D, Sohail U, et al. Pre-endoscopische erytromycine toediening bij bovenste gastro-intestinale bloedingen: een geactualiseerde meta-analyse en systematische review. Ann Gastroenterol. 2016,29:312-317.
31. Gralnek IM, Dumonceau JM, Kuipers EJ, et al. Diagnosis and management of nonvariceal upper gastrointestinal hemorrhage: Richtlijn van de European Society of Gastrointestinal Endoscopy (ESGE). Endoscopie. 2015;47:1-46.
32. Issa D, Solomon S, Di Pace B, et al. A Comparison of Azithromycin to Erythromycin Infusions in Improving Visualization of Endoscopy for Upper Gastrointestinal Bleeding. Wereldcongres op ACG2017. Sessie 2A.
33. Chey WD, Wong BC. Commissie Praktijkparameters van het American College of Gastroenterology. Richtlijn van het American College of Gastroenterology over de behandeling van Helicobacter pylori-infectie. Am J Gastroenterol. 2007; 102:1808-1825.
34. Luée A, Lanas A. Behandeling met protonenpompremmers en lagere gastro-intestinale bloedingen: afweging van risico’s en voordelen. World J Gastroenterol. 2016;22(48):10477-10481.