Introduction
Chronic kidney disease (CKD) is highly prevalent worldwide. In China heeft bijna 1 op de 10 mensen een zekere mate van nierdisfunctie, wat neerkomt op bijna 150 miljoen patiënten (1). Bloedarmoede en secundaire hyperparathyroïdie zijn de twee meest voorkomende complicaties geassocieerd met CKD (2, 3). Er is zelfs gemeld dat bijna 90% van de patiënten met gevorderde CKD (geclassificeerd als stadium 4 en 5 CKD) aan bloedarmoede lijden (4). Er is aangetoond dat het begin en de ernst van anemie goed gecorreleerd is met de afname van de glomerulaire filtratiesnelheid (4). Vroegtijdige identificatie, evaluatie en behandeling van anemie kan de morbiditeit en mortaliteit verminderen, evenals de kwaliteit van leven verbeteren, bij CKD-patiënten.
Secondaire hyperparathyreoïdie wordt gekenmerkt door verhoogde serum parathyroïdhormoon (PTH) niveaus. Een teveel aan PTH kan de erytropoëse aantasten door een direct toxisch effect op erytroïde progenitorcellen en een indirect effect door beenmergfibrose-inductie (5, 6). Bovendien kan de lage hemoglobineconcentratie bij uremische patiënten het gevolg zijn van een toename van de osmotische kwetsbaarheid van de erytrocyten als gevolg van de hoge PTH-concentratie (7). Er is een omgekeerde correlatie vastgesteld tussen PTH en hemoglobinegehalte (8-10). Meytes et al. ontdekten dat PTH-concentraties van 7,5-30 U/mL, vergelijkbaar met serum PTH-niveaus bij uremische patiënten, een significante remming veroorzaakten van de groei van burst-vormende eenheden-erythroïden (BFU-E) in muriene beenmergkweken, wat een mogelijke route suggereert voor de betrokkenheid van een teveel aan PTH bij het ontstaan van de anemie van uremie (11).
Erytropoëse-stimulerende middelen (ESA’s) zijn een kenmerk geworden van de anemietherapie bij patiënten met CKD en zijn de meest voorgeschreven medicatie bij dialysepatiënten, met >95% gebruik in China (1). Het eerste recombinant humaan erytropoëtine, epoëtine-alfa, werd in 1988 in de Verenigde Staten toegelaten (12). Epoëtine-alfa en epoëtine-beta zijn kortwerkende en kosteneffectieve therapeutische middelen en worden bij de meerderheid van de CKD-patiënten één tot drie keer per week toegediend. De dosering neemt echter toe met een verlengd doseringsinterval om een streefniveau voor hemoglobine te bereiken of te handhaven. Epiao®(3.000 μ/tube) is een soort epoëtine-alfa dat veel gebruikt wordt in China, terwijl Recormon®(2.000 μ/tube) een soort epoëtine-beta is dat meer gebruikt wordt in Europa, en in China ongeveer 4 jaar gebruikt wordt.
Vindingen van recente klinische studies hebben aangetoond dat doses die hoge hemoglobine streefwaarden bereiken aanleiding geven tot bezorgdheid over een verhoogd risico op overlijden of ongunstige uitkomsten zoals trombo-embolische voorvallen en beroerte (13-16). Andrews et al. vonden dat een verhoogde doseringsfrequentie bij een hoge dosis de incidentie van trombotische toxiciteiten verhoogde in vergelijking met dieren die minder frequent werden gedoseerd in lagere dosisgroepen, ondanks een vergelijkbaar hoog hematocriet in alle groepen (17), wat suggereert dat een hoog hematocriet niet de enige oorzakelijke factor is die leidt tot ESA-gerelateerde toxiciteiten, maar dat het ook samenhangt met dosisniveau, doseringsfrequentie en doseringsduur. Er moet dus veel aandacht worden besteed aan ESA-gerelateerde toxiciteiten die onafhankelijk zijn van een hoog hematocriet.
Op dit moment zijn er beperkte gegevens beschikbaar over de mogelijke relatie tussen de dosis ESA’s en PTH bij uremische patiënten die op regelmatige hemodialyse worden gehouden. Deze retrospectieve studie was gericht op het onderzoeken van de associatie tussen de dosis ESA’s en intact-PTH-niveaus (iPTH) bij hemodialysepatiënten op basis van klinische gegevens in ons ziekenhuiscomputerdatabasesysteem.
Materialen en methoden
Patiënten en procedures
Deze retrospectieve cohortstudie werd uitgevoerd van februari 2015 tot mei 2015 in Xiamen Zhongshan Hospital, Xiamen University, China. Deze studie omvatte uremische patiënten op onderhouden hemodialyse gedurende ten minste 3 maanden, die ESA’s gebruikten voor de behandeling van anemie. Patiënten die voldeden aan de volgende criteria werden uitgesloten van de studie: (1) leeftijd <18 jaar; (2) patiënten met actieve infectie, maligniteit, ijzergebreksanemie (gedefinieerd als ferritine <100 ng/mL en saturatie <20%), of actieve bloedingen binnen 3 maanden; (3) patiënten met onvolledige gegevens. In aanmerking komende patiënten werden ingedeeld in twee groepen, gebaseerd op de gebruikte ESA: Recormon groep en Epiao groep.
Data Collection
Data werden verkregen uit Jinshida, het computer databasesysteem van Xiamen Zhongshan Hospital, dat de klinische gegevens van 376 hemodialysepatiënten recodeerde. De volgende gegevens werden verzameld: leeftijd, geslacht, droog gewicht, diagnose van primaire ziekten, bloed ureum stikstof (BUN), serum creatinine (Scr), hemoglobine, calcium, fosfor, albumine, iPTH, serum ferritine, transferrine saturatie, en dosering van ESAs. Deze gegevens werden ’s morgens op de dag van de hemodialyse (vóór de dialyse) gemeten. In overeenstemming met de richtlijnen van Kidney Disease Improving Global Outcomes (KDIGO), werd een normaal hemoglobinegehalte gedefinieerd als een gehalte tussen 110 en 130 g/L bij uremische patiënten met gehandhaafde hemodialyse (8). Referentiewaarden voor serumcalcium en -fosfor werden gedefinieerd als waarden binnen 2,1-2,54 en 1,1-1,78 mmol/L, respectievelijk (18). Patiënten werden verder geclassificeerd op basis van iPTH niveaus: 150, 300, 600, en 1.500 pg/mL (19, 20).
Study Ethics
Deze studie werd uitgevoerd door het analyseren van de retrospectieve gegevens verkregen uit het Electronic Patient Record System van ons ziekenhuis. Het studieprotocol over menselijk onderzoek werd goedgekeurd door de Ethische Commissie van het Zhongshan Ziekenhuis, Xiamen University. Schriftelijke geïnformeerde toestemming werd verkregen van alle proefpersonen.
Statistische analyse
Statistische analyse werd uitgevoerd met behulp van SPSS voor Windows software versie 17.0. De gegevens werden uitgedrukt in percentages of gemiddelde ± Standard Error of Mean (SEM). Demografische gegevens en laboratoriummetingen tussen groepen werden vergeleken door Pearson’s chi-kwadraattest, Fisher’s exact-test, of Yate’s correctie voor continuïteit. Een P-waarde <0,05 werd als statistisch significant beschouwd.
Resultaten
Karakteristieken van uremische patiënten die op regelmatige hemodialyse werden gehouden
Er werden in totaal 240 uremische patiënten die op regelmatige hemodialyse werden gehouden in deze studie opgenomen. De basiskenmerken van de patiënten zijn weergegeven in tabel 1. Er waren geen significante verschillen in leeftijd, geslacht, drooggewicht, primaire ziekten, BUN, Scr, hemoglobine, serumfosfaat, calcium, albumine, serumferritine, en transferrineverzadiging tussen de Recormon- en Epiao-groepen (tabel 1, P > 0,05).

Tabel 1. Baseline kenmerken van de patiënten.
Het gemiddelde hemoglobinegehalte van alle proefpersonen was 103,15 ± 1,07 g/L. Patiënten met een hemoglobinegehalte tussen 110 en 130 g/L vormden 30,4% (n = 84). Anemie werd onderverdeeld in vijf klassen op basis van hemoglobinegehalte, volgens de ernst van de anemie (21, 22): hemoglobinegehalte <60 g/L (2,1%, n = 5), hemoglobinegehalte ≥60 en <90 g/L (21,7%, n = 52), hemoglobinegehalte ≥90 en <110 g/L (38.7%, n = 93), hemoglobinegehalte ≥110 en <130 g/L (30,4%, n = 73), en hemoglobinegehalte ≥130 g/L (7,1%, n = 17).
Relatie tussen de graad van anemie en iPTH
De relatie tussen verschillende graden van anemie en iPTH werd geanalyseerd. Uit de resultaten bleek dat het hemoglobinegehalte negatief geassocieerd was met iPTH (figuur 1A; tabel 2; P < 0,05). Er werd echter geen significant verband gevonden tussen bloedarmoede en serumcalcium of fosforgehalte (Figuur 1B; Tabel 2; P > 0,05 voor beide).
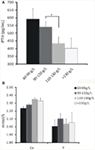
Figuur 1. De relatie tussen hemoglobineconcentraties en iPTH, serumcalcium of fosforgehalte. (A) De hemoglobineconcentratie nam toe naarmate de iPTH-spiegel afnam door stratificatie. (B) Er werd geen significant verband gevonden tussen de hemoglobineconcentratie en de serumcalcium- of fosforspiegel. De gegevens werden berekend met een t-test. *P < 0.05.

Tabel 2. Metingen van serum calcium, fosfor en iPTH niveaus op basis van hemoglobine waarden per stratificatie.
Patiënten met 150-300 pg/mL iPTH hadden de hoogste niveaus van hemoglobine, serumferritine, en transferrineverzadiging
Wanneer het iPTH-niveau tussen 150-300 pg/mL lag, hadden hemodialysepatiënten de hoogste gemiddelde niveaus van hemoglobine, serumferritine, en transferrineverzadiging; deze waren 106.25 g/L, 248,98 μg/L, en 30,97%, respectievelijk (figuur 2).
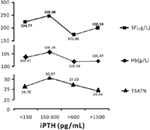
Figuur 2. Patiënten met iPTH-niveaus binnen 150-300 pg/mL hadden de hoogste niveaus van hemoglobine, serumferritine, en transferrineverzadiging. De gegevens worden uitgedrukt in percentages of gemiddelde ± SEM.
Vergelijking van Recormon vs. Epiao bij de behandeling van bloedarmoede
Patiënten die werden behandeld met Recormon en Epiao hadden vergelijkbare hemoglobinespiegels (103,54 ± 1,72 g/L, n = 98 vs. 102,59 ± 1,38 g/L, n = 142, P > 0,05; figuur 3A). De dosering van Recormon (3.853,66 ± 225,13 μ/week, n = 98) voor de behandeling van bloedarmoede was echter significant lager dan Epiao (7.083,33 ± 264,93 μ/week, n = 142, P < 0,05; figuur 3B, tabel 1).
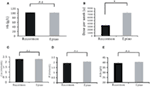
Figuur 3. Vergelijking van Recormon vs. Epiao bij de behandeling van anemie. (A) Patiënten die werden behandeld met Recormon en Epiao hadden vergelijkbare hemoglobinespiegels (103,54 ± 1,72 g/L, n = 98 vs. 102,59 ± 1,38 g/L, n = 142, P > 0,05). (B) De dosering van Recormon voor de behandeling van bloedarmoede was aanzienlijk lager dan Epiao, 3.853,66 ± 225,13 μ/week, n = 98 vs. 7.083,33 ± 264,93 μ/week, n = 142. (C-E) Er waren geen significante verschillen in calciumgehalte (C), fosforgehalte (D) en albuminegehalte (E) tussen de Recormon- en Epiao-groepen. Gegevens werden berekend door t-test; P > 0,05.
Calcium, fosfor, en albumine serumspiegels waren niet significant verschillend tussen de Recormon en Epiao groepen (respectievelijk, 2.27 ± 0,47 vs. 2,29 ± 0,01 mmol/L, P > 0,05; 1,94 ± 0,10 vs. 2,06 ± 0,04 mmol/L, P > 0,05; 39,5 ± 0,44 vs. 40,2 ± 0.35 g/L, P > 0,05; figuren 3C-E; tabel 1).
De relatie tussen de doses ESA’s en iPTH-spiegels
Voor alle hemodialysepatiënten was het iPTH-niveau in de Recormon-groep lager dan in de Epiao-groep (336.66 ± 57,76 pg/mL, n = 98 vs. 531,05 ± 39,57 pg/mL, n = 142; P < 0,05; Figuur 4A; Tabel 1). Een soortgelijke trend werd gevonden bij hemodialysepatiënten met hemoglobinegehalten tussen 110 en 130 g/L (319,50 ± 74,9 pg/mL in de Recormon-groep, n = 28 vs. 499,5 ± 64,38 pg/mL in de Epiao-groep, n = 45; P < 0,05; figuur 4A).
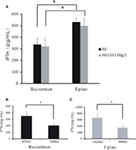
Figuur 4. Het verband tussen de dosis ESA’s en de iPTH-spiegel. (A) Het iPTH-niveau in de Recormon- en Epiao-groepen. (B) In de Recormon-groep, iPTH-niveaus bij patiënten die werden behandeld met Recormon met 2.000 versus 4.000 μ/week. (C) In de Epiao-groep, iPTH-niveaus bij patiënten die werden behandeld met Epiao bij 3.000 en >6.000 μ/week. De gegevens werden berekend met een t-test; *P < 0,05.
Onder de patiënten met een hemoglobinegehalte tussen 110 en 130 g/L, was het iPTH-niveau 201,54 ± 42.67 pg/mL (n = 10) bij patiënten die werden behandeld met Recormon bij 2.000 μ/week, wat significant lager was dan bij patiënten die werden behandeld met Recormon bij 4.000 μ/week (348,16 ± 117,9 pg/mL, n = 13; P < 0,05, figuur 4B). Evenzo was het gemiddelde iPTH-niveau bij patiënten die werden behandeld met Epiao bij 3.000 μ/week significant lager dan bij patiënten die werden behandeld met Epiao >6.000 μ/week (347,15 ± 75,94 pg/mL, n = 12 vs. 661,01 ± 198,45 pg/mL, n = 27; P < 0,05, figuur 4C).
Discussie
Deze retrospectieve studie is de eerste die bewijs levert dat hogere doses ESA’s (Epoëtine-alfa en -bèta) geassocieerd kunnen zijn met hogere iPTH-spiegels bij uremische patiënten die op regelmatige hemodialyse worden gehouden. Bovendien vonden we dat patiënten met iPTH-spiegels binnen 150-300 pg/mL de hoogste niveaus van hemoglobine, serumferritine en transferrineverzadiging hadden, wat consistent was met het aanbevolen niveau van iPTH op basis van de KDIGO-richtlijnen (9).
Anemie is een van de meest voorkomende complicaties van CKD. De Wereldgezondheidsorganisatie heeft bloedarmoede gedefinieerd als het hebben van een hemoglobineconcentratie lager dan 13,0 g/dl bij mannen en postmenopauzale vrouwen, of een hemoglobineconcentratie <12,0 g/dl bij andere vrouwen. Het gebruik van ESA’s heeft het leven van veel bloedarmoede-patiënten met CKD aanzienlijk verbeterd. Er is echter aangetoond dat hoge doses ESA’s geassocieerd zijn met een verhoogd risico op ongunstige uitkomsten bij volwassenen en kinderen met CKD. Patiënten die worden behandeld met hoge doses ESA’s hebben een 1,2-1,5 verhoogd risico op sterfte (23). In deze studie vonden we een significante omgekeerde associatie tussen iPTH-niveaus en hemoglobineconcentraties bij hemodialysepatiënten die werden behandeld met ESA’s, wat consistent is met bevindingen uit eerdere studies (8-10).
In deze studie vertoonden patiënten in de Recormon- en Epiao-groepen vergelijkbare hemoglobineconcentraties; de gebruikte dosering voor Recormon was echter significant lager dan Epiao. Wij vonden ook dat het iPTH-niveau in de Recormon-groep significant lager was dan in de Epiao-groep. Om het verband tussen de dosis ESA’s en de iPTH-spiegel verder te bepalen, analyseerden we de klinische gegevens van patiënten die afzonderlijk met Recormon of Epiao werden behandeld. De iPTH-spiegel was opmerkelijk lager bij patiënten die werden behandeld met Recormon met 2.000 μ/week dan bij patiënten die werden behandeld met Recormon met 4.000 μ/week. Een soortgelijke trend werd gevonden bij patiënten die werden behandeld met Epiao in een dosering van 3.000 of 6.000 μ/week, hetgeen suggereert dat hoge doses ESA’s in verband kunnen worden gebracht met hoge iPTH-spiegels. Deze bevindingen wijzen erop dat ESA-toxiciteit niet uitsluitend kan worden verklaard door een hoog hematocriet. Aangezien hoge doses ESA’s in verband kunnen worden gebracht met hoge iPTH-spiegels bij patiënten met dialyse, kunnen patiënten met nierinsufficiëntie in het eindstadium het beste worden behandeld door de dosis ESA’s te minimaliseren of te verlagen, met name bij patiënten met recente cardiovasculaire of cerebrovasculaire aandoeningen, hypertensieve noodsituaties of acute trombo-embolische aandoeningen. Gezien het verhoogde risico op cardiovasculaire voorvallen bij bijna normale hemoglobineconcentraties en hoge doses ESA’s bij CKD, wordt in Taiwan in feite niet aanbevolen om onevenredig hoge doses ESA’s te gebruiken om een hemoglobinegehalte van 100-110 g/L te bereiken (24).
Hoewel de pathogenese van anemie bij CKD multifactorieel is, is het gebrek aan erytropoëtine de belangrijkste oorzaak van anemie bij CKD-patiënten (25). Bijkomende factoren die bijdragen aan CKD-geassocieerde anemie zijn ijzertekort, ontstekingsanemie, onderdrukking van erytropoëse, verkorting van de overleving van rode bloedcellen door uremische toxinen, en bloedverlies zoals gastro-intestinale bloedingen. Aangezien ijzertekort ook een veel voorkomende oorzakelijke factor voor bloedarmoede is, werd intraveneuze ijzersuppletie eerder in Taiwan in 1996 aangemoedigd. Op basis van de ervaring met het beheer van CKD-anemie in Taiwan, kan een redelijk hemoglobine-doel worden bereikt door de laagst mogelijke ESA-dosis en intraveneuze ijzersuppletie te gebruiken (24).
Onze studie heeft verschillende beperkingen. Ten eerste, deze observationele studie is een single center studie. Ten tweede, gezien de mogelijke confounding en selectie bias door indicatie, voorzichtige interpretatie van deze gegevens nodig is. Onze waarnemingen over het verband tussen iPTH en ESA’s moeten verder worden onderzocht door longitudinale prospectieve studies. Ten derde is er een overwicht in het aantal met Epiao behandelde patiënten (142 voor Epiao vs. 98 voor Rocormon), wat waarschijnlijk te wijten is aan de relatief goedkope prijs van Epiao in vergelijking met Recormon (tabel 1). Ten vierde kunnen farmacologische interventies zoals antihypertensiva hebben geleid tot voorbijgaande schommelingen of zelfs interferentie in iPTH- of hemoglobinespiegels.
Concluderend toont deze studie aan dat hogere doses ESA’s geassocieerd kunnen zijn met hogere iPTH-spiegels bij uremische patiënten die op regelmatige hemodialyse worden gehouden. De betrokkenheid van hogere doses ESAs bij de pathogenese van secundaire hyperparathyreoïdie blijft onduidelijk en behoeft wellicht nader onderzoek. Onze bevindingen suggereren dat het gebruik van de laagst mogelijke ESA dosis de potentiële risico’s kan minimaliseren, terwijl een redelijke hemoglobine doelstelling wordt bereikt.
Bijdragen van de auteurs
Het manuscript is door alle auteurs beoordeeld en goedgekeurd, en wordt niet overwogen voor publicatie elders in een vergelijkbare vorm en in enige taal.
Conflict of Interest Statement
De auteurs verklaren dat het onderzoek werd uitgevoerd in afwezigheid van enige commerciële of financiële relaties die zouden kunnen worden opgevat als een potentieel belangenconflict.
Funding
Dit onderzoek werd ondersteund door het Medical Innovation Program Fund van de provincie Fujian (No. 2011027).
Afkortingen
BUN, bloedureumstikstof; CKD, chronische nierziekte; ESA, erytropoëse-stimulerend middel; Hb, hemoglobine; iPTH, intact-parathyroïdhormoon; Scr, serumcreatinine.
1. Zhang L, Wang F, Wang L, Wang W, Liu B, Liu J, et al. Prevalentie van chronische nierziekte in China: een cross-sectioneel onderzoek. Lancet (2012) 379:815-22. doi: 10.1016/S0140-6736(12)60033-6
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Martin KJ, Gonzalez EA. Metabolic bone disease in chronic kidney disease. J Am Soc Nephrol (2007) 18:875-85. doi:10.1681/ASN.2006070771
PubMed Abstract | CrossRef Full Text | Google Scholar
3. Rodriguez M, Nemeth E, Martin D. The calcium-sensing receptor: a key factor in the pathogenesis of secondary hyperparathyroidism. Am J Physiol Renal Physiol (2005) 288:F253-64. doi:10.1152/ajprenal.00302.2004
PubMed Abstract | CrossRef Full Text | Google Scholar
4. Levin A, Thompson CR, Ethier J, Carlisle EJ, Tobe S, Mendelssohn D, et al. Left ventricular mass index increase in early renal disease: impact of decline in hemoglobin. Am J Kidney Dis (1999) 34:125-34. doi:10.1016/S0272-6386(99)70118-6
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Kwack C, Balakrishnan VS. Managing erythropoietin hyporesponsiveness. Semin Dial (2006) 19:146-51. doi:10.1111/j.1525-139X.2006.00141.x
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Gallieni M, Corsi C, Brancaccio D. Hyperparathyroidism and anemia in renal failure. Am J Nephrol (2000) 20:89-96. doi:10.1159/000013563
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Wu SG, Jeng FR, Wei SY, Su CZ, Chung TC, Chang WJ, et al. Red blood cell osmotic fragility in chronically hemodialyzed patients. Nephron (1998) 78:28-32. doi:10.1159/000044878
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Baradaran A, Nasri H. Intensivering van anemie door secundaire hyperparathyreoïdie bij hemodialysepatiënten. Med J Islam Acad Sci (2001) 14(4):161-6.
Google Scholar
9. Sliem H, Tawfik G, Moustafa F, Zaki H. Verband tussen geassocieerde secundaire hyperparathyreoïdie en serum fibroblast groeifactor-23 in eindstadium nierziekte: een case-control studie. Indian J Endocrinol Metab (2011) 15:105-9. doi:10.4103/2230-8210.81939
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Trovato GM, Carpinteri G, Spina S, Squatrito G, Catalano D, Iannetti E. Hyperparathyroidism, anaemia and erythropoietin: effects on systolic function of dialysis patients. Abstracts of 31 st Congress of European Renal Association/European dialysis ND Transplantation Association, 5-8 september 1999 Madrid. Nephrol Dial Transpl (1999) 14:190.
Google Scholar
11. Meytes D, Bogin E, Ma A, Dukes PP, Massry SG. Effect of parathyroid hormone on erythropoiesis. J Clin Invest (1981) 67:1263-9. doi:10.1172/JCI110154
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Eschbach JW, Abdulhadi MH, Browne JK, Delano BG, Downing MR, Egrie JC, et al. Recombinant humaan erytropoëtine bij anemische patiënten met nierinsufficiëntie in het eindstadium. Resultaten van een fase III multicenter klinisch onderzoek. Ann Intern Med (1989) 111(12):992-1000. doi:10.7326/0003-4819-111-12-992
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Besarab A, Bolton WK, Browne JK, Egrie JC, Nissenson AR, Okamoto DM, et al. The effects of normal as compared with low hematocrit values in patients with cardiac disease who are receiving hemodialysis and epoetin. N Engl J Med (1998) 339:584-90. doi:10.1056/NEJM199808273390903
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Singh AK. Should we keep hemoglobin levels as a viable outcome measure? Nephrol News Issues (2010) 24(15-6):18.
PubMed Abstract | Google Scholar
15. Phrommintikul A, Haas SJ, Elsik M, Krum H. Mortality and target haemoglobin concentrations in anaemic patients with chronic kidney disease treated with erythropoietin: a meta-analysis. Lancet (2007) 369:381-8. doi:10.1016/S0140-6736(07)60194-9
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Regidor D, McClellan WM, Kewalramani R, Sharma A, Bradbury BD. Changes in erythropoiesis-stimulating agent (ESA) dosing and haemoglobin levels in US non-dialyse chronic kidney disease patients between 2005 and 2009. Nephrol Dial Transplant (2011) 26:1583-91. doi:10.1093/ndt/gfq573
PubMed Abstract | CrossRef Full Text | Google Scholar
17. Andrews DA, Pyrah ITG, Boren BM, Tannehill-Gregg SH, Lightfoot-Dunn RM. High hematocrit resulting from administration of erythropoiesis-stimulating agents is not fully predictive of mortality or toxicities in preclinical species. Toxicol Pathol (2014) 42:510-23. doi:10.1177/0192623313486317
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Kidney Disease: Improving Global Outcomes (KDIGO) CKD-MBD Werkgroep. KDIGO clinical practice guideline for the diagnosis, evaluation, prevention, and treatment of Chronic Kidney Disease-Mineral and Bone Disorder (CKD-MBD). Kidney Int Suppl (2009) 113:S1-130. doi:10.1038/ki.2009.188
CrossRef Full Text | Google Scholar
19. Tentori F, Blayney MJ, Albert JM, Gillespie BW, Kerr PG, Bommer J, et al. Mortality risk for dialysis patients with different levels of serum calcium, phosphorus, and PTH: the Dialysis Outcomes and Practice Patterns Study (DOPPS). Am J Kidney Dis (2008) 52(3):519-30. doi:10.1053/j.ajkd.2008.03.020
PubMed Abstract | CrossRef Full Text | Google Scholar
20. National Kidney Foundation. K/DOQI clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Am J Kidney Dis (2002) 39(2 Suppl 1):S1-266.
Google Scholar
21. Pisoni RL, Bragg-Gresham JL, Young EW, Akizawa T, Asano Y, Locatelli F, et al. Anemie management and outcomes from 12 countries in the Dialysis Outcomes and Practice Patterns Study (DOPPS). Am J Kidney Dis (2004) 44(1):94-111. doi:10.1053/j.ajkd.2004.08.005
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Kidney Disease: Improving Global Outcomes (KDIGO) Anemie Werkgroep. KDIGO klinische praktijkrichtlijn voor anemie bij chronische nierziekte. Kidney Int Suppl (2012) 2:279-335.
Google Scholar
23. Suttorp MM, Hoekstra T, Mittelman M, Ott I, Krediet RT, Dekker FW, et al. Behandeling met hoge dosis erytropoëse-stimulerende middelen en mortaliteit: analyse met een sequentiële Cox-benadering en een marginaal structureel model. Pharmacoepidemiol Drug Saf (2015) 24(10):1068-75. doi:10.1002/pds.3855
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Hung SC, Kuo KL, Tarng DC, Hsu CC, Wu MS, Huang T-P. Beheer van anemie bij patiënten met chronische nierziekte: Richtlijnen voor de Taiwanese praktijk. Nephrology (Carlton) (2014) 19:735-9. doi:10.1111/nep.12332
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Randolph JF, Scarlett JM, Stokol T, MacLeod JN. Clinical effi-cacy and safety of recombinant canine erythropoietin in dogs with anemia of chronic renal failure and dogs with recombinant human erythropoietin-induced red cell aplasia. J Vet Intern Med (2004) 18:81-91. doi:10.1111/j.1939-1676.2004.tb00139.x
CrossRef Full Text | Google Scholar