EINLEITUNG
Die Stenose des proximalen Abschnitts der vorderen absteigenden Koronararterie (pAD) ist eine besondere Untergruppe der ischämischen Herzkrankheit, da diese Läsionen allein1,2 oder im Kontext einer Mehrgefäßerkrankung ein hohes Risikoprofil aufweisen.3 Die Quantität und Qualität des gefährdeten Herzmuskels, die von der Permeabilität der pAD abhängt, macht einen aggressiveren therapeutischen Ansatz erforderlich. In-vivo-Ultraschallstudien zu dieser Art von Läsionen haben gezeigt, dass die Gefäße überwiegend exzentrisch betroffen sind.4 Dies würde die schlechteren Ergebnisse erklären, die nach einer perkutanen transluminalen Koronarangioplastie (PTCA) bei diesen Läsionen aufgrund des Phänomens der elastischen Retraktion erzielt werden. In verschiedenen Studien wurden die Therapiestrategien für diese Läsionen verglichen, wobei im Allgemeinen bessere Ergebnisse nach einer interventionellen Behandlung (koronare Revaskularisationschirurgie mit internem Mammaria-Graft oder perkutane Revaskularisation gegenüber konventioneller medizinischer Behandlung) beobachtet wurden.5-12 Die vorliegende Studie bewertet die Wirksamkeit und langfristige Sicherheit der Stent-Implantation bei dieser Art von Läsionen und wurde durchgeführt, da es in unserem Gebiet kaum Studien zu diesem Thema gibt.
METHODEN
Studienpopulation
In eine prospektive, nicht-randomisierte, klinische Follow-up-Studie wurden insgesamt 98 konsekutive Patienten aufgenommen, die zwischen April 1995 und April 1998 in unser Labor überwiesen wurden. In diesem Zeitraum wurden 1136 PTCA durchgeführt, und die Studiengruppe stellt 8,6 % aller in diesem Zeitraum in unserem Labor durchgeführten Eingriffe dar. Die Nachbeobachtung endete im Mai 2000.
Einschluss- und Ausschlusskriterien
Patienten, die eine signifikante pAVK-Stenose (Stenose von mehr als 70 % nach visueller Einschätzung) vor dem ersten Septalast und dem größeren Diagonalast aufwiesen und bei denen eine Ischämie in dem von der pAVK abhängigen Gebiet nachgewiesen wurde, kamen für die Studie in Frage. Die Patienten unterzogen sich einer geplanten perkutanen Ballonrevaskularisation und Stentimplantation. Ausgeschlossen wurden Patienten, die im Rahmen eines akuten Myokardinfarkts (AMI) überwiesen wurden, sowie Läsionen, die nach dem Urteil des Operateurs für das Verfahren ungeeignet waren, insbesondere Läsionen mit chronischem Verschluss und massiver Verkalkung. Alle Patienten unterzeichneten vor der Revaskularisierung eine Einverständniserklärung. Die Studiengruppe umfasste alle Patienten mit pAVK-Läsionen, die in diesem Zeitraum in unserem Labor behandelt wurden.
Protokoll des Verfahrens (PTCA+Stent-Implantation)
In allen Fällen wurde die PTCA über einen Gefäßzugang durch die Arteria femoralis durchgeführt und der Stent wurde (nach Ballondilatation) durch Freisetzung unter hohem Druck (12-14 Atmosphären) implantiert. Palmaz-Schatz- und NIR-Stents (die am häufigsten verwendeten Modelle) wurden manuell auf den Angioplastieballon montiert. In der letzten Phase der Studie wurden Stents verwendet, die auf dem Ballon vormontiert waren. Der „angiografische Erfolg des Verfahrens“ wurde definiert als das Vorhandensein von Restläsionen von weniger als 30 % durch visuelle Beurteilung des Segments, in das der Stent implantiert wurde. „Unterdrückte Ejektionsfraktion (EF)“ war definiert als das Vorhandensein einer EF von weniger als 50 % bei visueller Beurteilung. „Mehrgefäßerkrankung“ wurde definiert als das Vorhandensein signifikanter koronarer Läsionen (Stenosen von mehr als 70 % bei visueller Beurteilung) in zwei oder mehr Gefäßen. Alle Patienten erhielten nach der Angioplastie einen Monat lang einen Thrombozytenaggregationshemmer in Form von Acetylsalicylsäure und Ticlopidin. Vor dem Eingriff wurde je nach Gewicht des Patienten ein i.v.-Bolus von 7500 bis 10 000 IE Heparin verabreicht, um partielle Thromboplastin-Aktivierungszeiten von über 300 s zu erreichen.
Nachuntersuchungsprotokoll
Alle Patienten nahmen an einer jährlichen klinischen Nachuntersuchung durch persönliche oder telefonische Befragung teil. Alle unterzogen sich den vom behandelnden Kardiologen angeordneten Tests zum Nachweis einer Ischämie. Bei zweifelhaften Testergebnissen oder Diskrepanzen zwischen den klinischen Symptomen und den Testergebnissen ordneten wir neue Tests zum Nachweis einer Ischämie an (neue Belastungstests oder Radionuklidstudien). Der letzte Besuch fand persönlich statt, und es wurden eine Anamnese, eine körperliche Untersuchung und ein EKG durchgeführt. Die Patienten, bei denen die Angina pectoris mit klinischen Kriterien für den Schweregrad fortbestand, wurden direkt im Labor erneut angiografisch untersucht. Als angiografische Restenose wurde das Vorhandensein einer Stenose von mehr als 50 % in dem mit einem Stent behandelten pAVK-Segment definiert.
Eine Reihe von Variablen wurde in der Studiengruppe für die spätere Analyse und Bestimmung prognostischer Faktoren für die klinische Entwicklung der Patienten erfasst. Diese Variablen waren:
— Klinisch: Alter, Geschlecht, Diagnose vor der Katheterisierung, Vorhandensein von Diabetes mellitus, arterieller Hypertonie, Rauchen, Dyslipidämie. Von multiplen Risikofaktoren wurde ausgegangen, wenn drei oder mehr klassische Risikofaktoren vorlagen.
— Anatomisch: Vorhandensein einer Mehrgefäßerkrankung, linksventrikuläre Dysfunktion.
— Verfahren: Länge und Durchmesser des Stents, Anzahl der verwendeten Stents, Art des Stents und Vorhandensein einer ostialen Läsion.
Schlussereignisse
Während der Krankenhausaufnahme und der späteren Nachbeobachtung wurde das Auftreten von schwerwiegenden unerwünschten kardialen Ereignissen (MACE) oder schwerwiegenden Komplikationen erfasst, definiert als: Tod kardialen Ursprungs, Auftreten einer neuen AMI und Notwendigkeit einer erneuten pAD-Revaskularisierung. Nicht kardiale Todesfälle und die Notwendigkeit einer Revaskularisierung anderer Gefäße als der pAVK wurden erfasst.
Statistische Analyse
Die verschiedenen Variablen wurden in einer Microsoft Access®-Datenbank erfasst und mit dem Statistikprogramm SPSS®, Version 9.0, analysiert. Die qualitativen Variablen werden als Prozentsätze und die quantitativen Variablen als Mittelwert±Standardabweichung (SD) angegeben. Die versicherungsmathematischen Kurven für das todesfreie Überleben, das todesfreie Überleben am Herzen und das ereignisfreie Überleben wurden mit der Kaplan-Meier-Methode geschätzt. In der univariaten Analyse wurden die verschiedenen klinischen, angiografischen und prozeduralen Variablen auf der Grundlage des Vorhandenseins oder Nichtvorhandenseins von schwerwiegenden unerwünschten Ereignissen am Ende der Nachbeobachtungszeit verglichen, die quantitativen Variablen wurden mit dem Student t-Test und die qualitativen Variablen mit dem Chi-Quadrat-Test verglichen. Darüber hinaus wurden die Kurven des ereignisfreien Überlebens mit dem Log-Rank-Test für die Variablen verglichen, die eine Tendenz zum Auftreten von Ereignissen zeigten (PP P
ERGEBNISSE
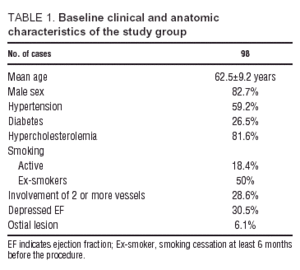
Baseline-Charakteristika
Die klinischen Merkmale der Patienten zum Zeitpunkt der Aufnahme in die Studie und die anatomischen Merkmale, die bei der Koronararteriographie festgestellt wurden, sind in Tabelle 1 dargestellt. Die meisten Patienten wurden wegen instabiler Angina pectoris überwiesen (87 Patienten mit instabiler Angina pectoris, 11 mit stabiler Anstrengungsangina). Zweiundzwanzig Patienten wiesen 3 oder mehr kardiovaskuläre Risikofaktoren auf; von ihnen waren 20 (91 %) Hypertoniker, 19 (86 %) Diabetiker und 21 (95 %) hatten Dyslipidämie, während nur 10 (55 %) aktive Raucher waren. Einundsiebzig Prozent (71%) der Patienten hatten eine einzelne Läsion der pAD und 70% von ihnen wiesen in der Ventrikulographie keine ventrikuläre Dysfunktion auf.
Verfahren
Die Variablen des Verfahrens sind in Tabelle 2 dargestellt. Siebenundsiebzig Prozent (77 %) der Patienten hatten kurze Läsionen der pAVK, was sich im Prozentsatz der verwendeten kurzen Stents widerspiegelt (

Verlauf
Die mittlere Nachbeobachtungszeit betrug 38 ± 11 Monate, wobei sie bei nur 2 Patienten, die verstarben (2 und 9 Monate nach Einschluss), weniger als 24 Monate betrug. Im Verlauf der Studie kam es zu keinem Verlust der Nachbeobachtung, wie in Abbildung 1 grafisch dargestellt. Während der Studie bis zum Abschluss blieben 68 Patienten (69,4 %) frei von Angina pectoris und wiesen während der Nachbeobachtung keine MACE auf. Fünfundzwanzig Patienten (25,5 %) hatten Angina pectoris und wurden zu einer erneuten Koronariographie überwiesen. Bei 7 Patienten wurde eine angiografische Restenose festgestellt, aber es wurde kein neues perkutanes oder chirurgisches Revaskularisationsverfahren beschlossen (4 Patienten hatten nicht überbrückbare distale Gefäße und anatomische Läsionen, die für eine neue PTCA ungünstig waren, und die anderen 3 hatten eine Restenose von weniger als 70 % und eine ausreichende klinische Kontrolle mit antianginösen Medikamenten). Zwölf Patienten erforderten eine erneute Revaskularisierung der Zielläsion: 6 durch eine Koronararterienoperation und einen IMA-Bypass 3, 6, 6, 9, 13 bzw. 14 Monate nach der Stentimplantation (bei einem Patienten wurde die Operation nach einer erneuten PTCA der pAD wegen einer frühen Restenose nach 3 Monaten durchgeführt) und 6 durch eine erneute PTCA zwischen Monat 5 und 34 der Nachbeobachtung (in einem Fall wurde der Stent aufgrund einer intrastentalen Restenose entfernt). Die anderen 7 Patienten mit persistierender Angina pectoris wurden zu einer erneuten Revaskularisation durch PTCA und Stentimplantation in anderen Gefäßen als der pAD überwiesen, wobei bei 3 von ihnen 2 Gefäße behandelt wurden (3 Revaskularisationen der rechten Koronararterie, 3 der mittleren anterioren absteigenden und 4 der stumpfen marginalen). Zwei Patienten erlitten 2 bzw. 4 Monate nach dem Eingriff einen anterioren AMI (einer davon stumm). Eine Koronariographie wurde später nicht durchgeführt, da die Tests auf Restischämie negativ waren.
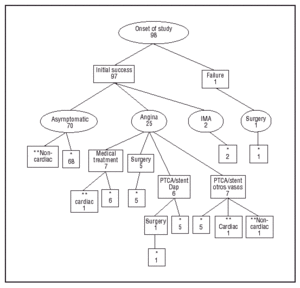
Abb. 1. Diagramm der Entwicklung der Patienten (*asymptomatisch am Ende der Studie, **Tod).
Fünf Todesfälle traten auf, 2 mit kardialem Ursprung 2 und 38 Monate nach Einschluss in die Studie und 3 mit nicht-kardialem Ursprung (1 wegen einer neoplastischen Erkrankung 38 Monate nach Einschluss in die Studie, 1 wegen eines akuten Abdomens mit rektaler Blutung 9 Monate später und 1 wegen eines ischämischen Schlaganfalls 24 Monate später).
Nach dem Kaplan-Meier-Test betrug die Wahrscheinlichkeit, nach 60 Monaten Nachbeobachtung frei von MACE zu bleiben, 83,7 % (Abbildung 2), und die Gesamtwahrscheinlichkeit, keinen kardialen oder nicht-kardialen Tod zu erleiden, lag bei 98 % bzw. 94,8 % (Abbildung 3).
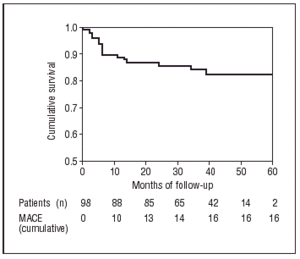
Abb. 2. Kaplan-Meier-Kurve des Überlebens ohne größere kardiale Ereignisse.
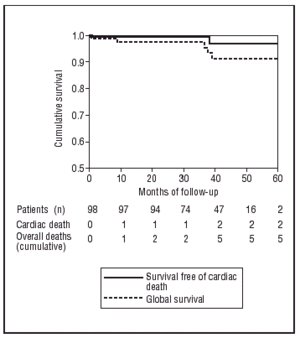
Abb. 3. Kaplan-Meier-Kurven des Überlebens ohne Tod und ohne Tod kardialen Ursprungs.
Die klinischen, anatomischen und verfahrensspezifischen Variablen und ihr Zusammenhang mit dem Auftreten von MACE sind in Tabelle 3 dargestellt. Die univariate Analyse zeigte, dass die Verwendung von 2 Stents mit einer höheren Inzidenz von MACE (PP=.021) und der AHT-DM-Dyslipidämie-Interaktion (OR=3,7; 95% CI, 1,3-10,3; P=.011) verbunden war. Ostiale Stenosen (OR=3,7; 95% CI, 0,8-16,6; P=.09) zeigten eine größere Tendenz zum Auftreten von Ereignissen.
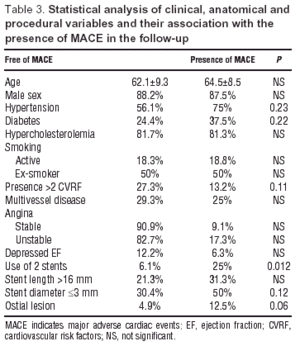
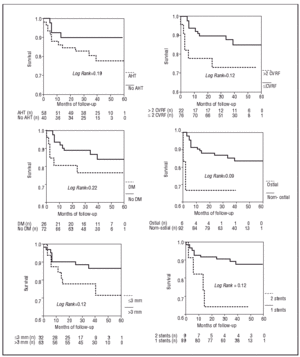
Abb. 4. Kaplan-Meier-Kurven des Überlebens ohne schwerwiegende kardiale Ereignisse in Abhängigkeit vom Vorhandensein verschiedener klinischer Faktoren und dem Verfahren. CVRF steht für kardiovaskuläre Risikofaktoren.
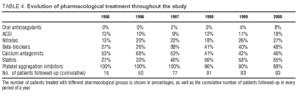
Die pharmakologischen Behandlungen, die die Patienten während der Studie erhielten, sind in Tabelle 4 aufgeführt. Thrombozytenaggregationshemmer (Acetylsalicylsäure und/oder Ticlopidin) wurden während der Nachbeobachtung häufig eingesetzt, zusätzlich zu Kalziumantagonisten und Betablockern, die von 48 % bzw. 46 % der Patienten am Ende der Studie eingenommen wurden. Der Einsatz von Statinen stieg beträchtlich an, und zwar von 27 % zu Beginn der Nachbeobachtung auf 65 % bei Abschluss der Studie.
DISKUSSION
Die Langzeitergebnisse (mittlere und maximale Nachbeobachtungszeit von 38 bzw. 60 Monaten) dieser prospektiven Beobachtungsstudie über Stenosen des proximalen Abschnitts der pAVK, die mit einer Stentimplantation behandelt wurden, zeigten, dass das Verfahren eine hohe Erfolgsrate (98.9 %), eine niedrige Rate neuer Revaskularisationen (12,2 %), eine hohe Wahrscheinlichkeit, frei von MACE zu bleiben (83,7 %), und eine niedrige Mortalität. Es ist anzumerken, dass ein großer Prozentsatz der Patienten kurze, eingefäßige Läsionen und keine eingeschränkte linksventrikuläre Funktion hatte.
Vergleich mit früheren Studien
Vorangegangene Studien haben gezeigt, dass eine interventionelle Behandlung bei schwerer Erkrankung der pAD oder eingefäßiger koronarer Herzkrankheit mehr Vorteile bringt als eine pharmakologische medikamentöse Behandlung.5,6 Dennoch zeigt der Vergleich der beiden wichtigsten Revaskularisationstechniken (PTCA und IMA-Graft), dass in der mit PTCA behandelten Gruppe häufiger neue Revaskularisationen auftreten, mehr antianginöse Medikamente benötigt werden und die körperliche Belastbarkeit schlechter ist, wobei die Raten für Reinfarkte und Mortalität in beiden Gruppen ähnlich sind.4,7-12 Diese höhere Inzidenz neuer Revaskularisationen nach PTCA ist auf das Phänomen der Restenose zurückzuführen, die hauptsächlich im ersten Jahr nach der PTCA auftritt.13,14 Die Inzidenz der Restenose nach isolierter PTCA variiert in verschiedenen Serien zwischen 40 % und 66 %. Zu den Faktoren, die eine Restenose begünstigen, gehören das Vorhandensein proximaler Läsionen und die Beteiligung der absteigenden vorderen Koronararterie.15 Die Einführung der Stentimplantation hat diese Ergebnisse deutlich verändert und das Restenoserisiko um fast die Hälfte reduziert,9,16-19 bei einer sehr geringen Inzidenz von Sofortkomplikationen und einer äußerst günstigen kurz- und mittelfristigen klinischen Entwicklung (ähnlich wie bei der IMA-Graft-Implantation). Frühere Studien haben eine Häufigkeit des Implantatversagens bei Stents, die manuell auf den Ballon montiert werden, von 1,5 % bis 6,9 % beim Palmaz-Schatz-Stent und von 1,5 % bis 3,1 % beim NIR-Stent gezeigt.20,21 Neuere Studien zu Stents der zweiten Generation, wie z. B. das SPORT-NIR-Register,22 berichten von Implantatversagensraten von nur 0,4 %. In unserer Studie kam es nur zu einem Ausfall bei der Implantation des Palmaz-Schatz-Stents, der manuell auf den Angioplastieballon montiert wurde. Diese Misserfolgsrate von 1 % stimmt mit den in früheren Studien berichteten Ergebnissen überein.
Die Raten der Restenose und der Notwendigkeit einer erneuten Stentrevaskularisation schwanken in verschiedenen Serien zwischen 19 % und 31 %.10,16,19,23 Unsere Ergebnisse bestätigen, dass neue Revaskularisationen der pAD bis zu zweieinhalb Jahre nach dem Eingriff auftreten können, obwohl die meisten Reinterventionen in den ersten 12 Monaten nach der Stentimplantation stattfanden (66,6 % der Fälle). Wir fanden eine Inzidenz neuer Revaskularisationen der pAVK von 12,2 %, obwohl die tatsächliche Inzidenz signifikanter Restenosen und die Geschwindigkeit ihres Auftretens in unserer Serie nicht bekannt ist, da wir die Patienten nicht systematisch angiografisch ausgewertet haben.
Prädiktoren der Entwicklung
Unter den analysierten Faktoren war nur die Verwendung von zwei Stents während des Eingriffs ein unabhängiger Risikofaktor für eine ungünstigere klinische Entwicklung, was mit dem Bericht der Gruppe von Bauters et al.24 übereinstimmt
Faktoren, die traditionell auf eine schlechtere Prognose nach Stentimplantation hindeuten, wie DM, Multigefäßerkrankung, Bluthochdruck oder linksventrikuläre Dysfunktion in der Langzeitnachbeobachtung25 , wurden in der univariaten Analyse nicht bestätigt. Bei DM wurde festgestellt, dass das Phänomen der Restenose im Wesentlichen auf einen Prozess der übermäßigen Intimahyperplasie zurückzuführen ist, im Vergleich zu nicht-diabetischen Patienten,26 bei denen sich dieser Prozess weniger aggressiv entwickelt. Dieses Phänomen äußert sich in höheren Raten von Restenosen und der Notwendigkeit neuer Revaskularisationsverfahren.27 Von den 23 Diabetikern in unserer Studie waren die meisten (20 von 23) nicht insulinabhängig, was erklären könnte, warum DM kein unabhängiger Prädiktor war, da neuere Studien einen Unterschied in der Entwicklung der Stentpermeabilität in Abhängigkeit vom Diabetestyp nachgewiesen haben. Die Prognose ist bei insulinabhängiger DM schlechter.28,29 Dennoch wurde in der multivariaten Analyse eine Assoziation von DM, AHT und Dyslipidämie mit einer schlechteren klinischen Entwicklung festgestellt. Dies zeigt, dass diese Faktoren zwar nicht eindeutig mit der Prognose im Einzelnen verbunden sind (zumindest bei Stichproben der hier untersuchten Größe), das Zusammentreffen von Faktoren bei einem Patienten jedoch als prädiktiv für eine ungünstigere Entwicklung angesehen werden muss, wie dies bei atherosklerotischen Erkrankungen im Allgemeinen der Fall ist.
Während der gesamten Nachbeobachtungszeit wurden viele Medikamente eingenommen, was im Wesentlichen auf die hohe Prävalenz klassischer kardiovaskulärer Risikofaktoren wie Hypercholesterinämie und AHT in der Studienpopulation zurückzuführen ist, sowie auf eine Mehrgefäßerkrankung, die zum Zeitpunkt der Aufnahme (31 %) und während der Entwicklung (7 Patienten wiesen eine Progression der koronaren Herzkrankheit auf, die eine Revaskularisierung anderer Gefäße erforderte) auftrat.
Klinische Implikationen
Die Ergebnisse unserer Studie bestätigen die Sicherheit der Stentimplantation bei Läsionen mit Beteiligung der pAD und ein gutes langfristiges klinisches Ansprechen, das bei einigen Patienten 5 Jahre Follow-up erreichte. Die Überlebensrate und das Ausbleiben von MACE stimmen mit früheren Studien zur Stentimplantation bei pAVK überein30 und sind vergleichbar mit den Ergebnissen anderer Studien, in denen eine koronare Revaskularisierung mit IMA-Transplantation durchgeführt wurde.7,31
In der klinischen Praxis8,32 muss die Entscheidung für eine IMA-Bypass-Operation gegenüber einer PTCA und einer Stent-Implantation individuell für jeden Patienten getroffen werden, wobei die Meinung des Patienten zu berücksichtigen ist, nachdem er Informationen über beide therapeutischen Alternativen, ihre Ergebnisse und Risiken erhalten hat, und die perkutane Alternative als erste Wahl in Fällen mit einer günstigen Koronaranatomie und bei Patienten, bei denen die Notwendigkeit künftiger Revaskularisationen absehbar ist (z. B,
Studieneinschränkungen
Die wichtigste Einschränkung der Studie war das Fehlen einer Randomisierung, was eine direkte vergleichende Analyse mit anderen Revaskularisierungsstrategien ausschloss. Die Tatsache, dass die Koronararteriographie während der Nachbeobachtung nicht systematisch durchgeführt wurde, erlaubt es uns nicht, die tatsächliche Rate der angiographischen Restenose in der Studiengruppe zu bestimmen. Die eingesetzte Technologie war auf dem Stand von 1995. Die Verwendung neuer Materialien und Designs bei den Stents der neueren Generation sowie neue Aggregationshemmer mit Antagonisten der IIb-IIIa-Plättchenrezeptoren dürften die Kurz- und Langzeitergebnisse verbessern. Die in unserer Studie mit diesen Wirkstoffen erzielten Ergebnisse sprechen jedoch aufgrund des hohen Kosten-Nutzen-Verhältnisses nicht für ihren allgemeinen Einsatz bei der Stentimplantation.
ZUSAMMENFASSUNG
Die Behandlung der Stenose des proximalen Abschnitts der vorderen absteigenden Koronararterie mit einer Stentimplantation ist bei Patienten mit einer für dieses Verfahren günstigen Koronaranatomie sicher. Der Prozentsatz der Komplikationen ist gering und geht bei einer längeren Nachbeobachtungszeit, die in einigen Fällen in unserer Studie 5 Jahre beträgt, mit einer geringen Inzidenz neuer Revaskularisierungsverfahren und einer hohen Überlebensrate einher.
HINWEISE
Wir möchten unseren aufrichtigen Dank an Drs. V. Climent und J. Sánchez von den Abteilungen für Kardiologie bzw. Präventivmedizin des Hospital General Universitario von Alicante für ihre Unterstützung und Beratung bei der Erstellung dieses Artikels danken.