Krebs ist eine Folge des Zusammenbruchs der Kontrollmechanismen, die die Zellen regulieren. Zu den Ursachen für den Zusammenbruch gehören immer Veränderungen in wichtigen Genen. Diese Veränderungen sind oft das Ergebnis von Mutationen, d.h. Veränderungen in der DNA-Sequenz der Chromosomen. Bei Mutationen kann es sich um sehr kleine Veränderungen handeln, die nur wenige Nukleotide betreffen, oder sie können sehr groß sein und zu großen Veränderungen in der Struktur der Chromosomen führen.
Sowohl kleine als auch große Mutationen können das Verhalten der Zellen beeinflussen. Kombinationen von Mutationen in wichtigen Genen können zur Entstehung von Krebs führen. Das auf dieser Seite behandelte Material beschreibt den Zusammenhang zwischen Mutation und Krebs, die verschiedenen Arten von Mutationen und deren Ursachen. Weitere Informationen zu den Themen auf dieser Seite finden Sie auch in den meisten einführenden Biologie-Lehrbüchern, wir empfehlen Campbell Biology, 11. Auflage.1
Themen auf dieser Seite:
- Mutation und Krebs
- Erbliche Mutationen und Krebs
- Mutationsarten
- Punktmutationen
- Translokationen
- Genamplifikation
- Inversionen, Deletionen und Duplikationen
- Aneuploidie
- Epigenetische Veränderungen
- Ursachen von Mutationen
- Zusammenfassung von Mutationen
- Kennen Sie den Ablauf: Mutation
Mutation und Krebs
Die abnormen Verhaltensweisen von Krebszellen sind das Ergebnis einer Reihe von Mutationen in wichtigen Regulationsgenen. Je mehr Gene geschädigt werden, desto abnormaler werden die Zellen. Oft werden die Gene, die für die DNA-Reparatur zuständig sind, selbst geschädigt, was die Zellen noch anfälliger für ein immer größeres genetisches Chaos macht.
Unten sehen Sie eine Animation, die die Beziehung zwischen Chromosomen, Genen und DNA veranschaulicht.
Man geht davon aus, dass die meisten Krebsarten aus einer einzigen mutierten Vorläuferzelle entstehen. Wenn sich diese Zelle teilt, können die entstehenden „Tochterzellen“ im Laufe der Zeit verschiedene Mutationen und Verhaltensweisen annehmen. Diejenigen Zellen, die einen Vorteil bei der Teilung oder der Resistenz gegen den Zelltod erlangen, neigen dazu, die Population zu übernehmen. Auf diese Weise sind die Tumorzellen in der Lage, ein breites Spektrum an Fähigkeiten zu erlangen, die normalerweise in der gesunden Version des dargestellten Zelltyps nicht vorkommen.
Mutationen in wichtigen regulatorischen Genen (Tumorsuppressoren und Proto-Onkogene) verändern das Verhalten von Zellen und können zu dem unkontrollierten Wachstum führen, das man bei Krebs beobachten kann.
Bei fast allen bisher untersuchten Krebsarten scheint der Übergang von einer normalen, gesunden Zelle zu einer Krebszelle ein schrittweiser Prozess zu sein, der viele genetische Veränderungen erfordert, die sich zu einer Krebszelle summieren. Diese Mutationen treten sowohl an Onkogenen als auch an Tumorsuppressoren auf. Dies ist einer der Gründe, warum Krebs bei älteren Menschen viel häufiger vorkommt. Um eine Krebszelle zu erzeugen, muss eine Reihe von Mutationen in ein und derselben Zelle auftreten. Da die Wahrscheinlichkeit, dass ein beliebiges Gen mutiert, sehr gering ist, liegt es auf der Hand, dass die Wahrscheinlichkeit, dass mehrere verschiedene Mutationen in ein und derselben Zelle auftreten, wirklich sehr unwahrscheinlich ist. Aus diesem Grund hatten die Zellen in einem 70 Jahre alten Körper mehr Zeit, die zur Bildung von Krebszellen erforderlichen Veränderungen zu akkumulieren, während es bei den Zellen eines Kindes viel unwahrscheinlicher ist, dass sie die erforderlichen genetischen Veränderungen erworben haben. Natürlich erkranken auch einige Kinder an Krebs, doch ist er bei älteren Menschen viel häufiger. Die folgende Grafik zeigt die Darmkrebsraten in den Vereinigten Staaten in Abhängigkeit vom Alter. Die Grafik stammt vom National Cancer Institute. 2
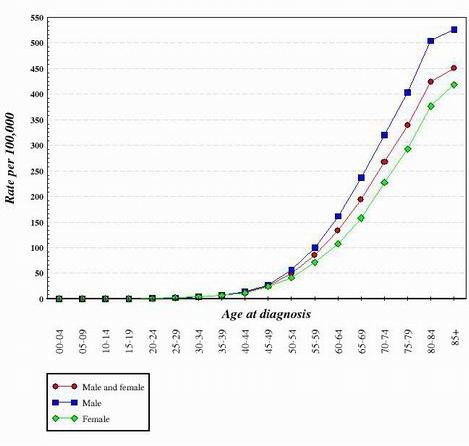
Bei Betrachtung der Form von Kurven wie der oben gezeigten ist man zu dem Schluss gekommen, dass mehrere genetische Veränderungen erforderlich sind, um Zellen zu erzeugen, die zu Krebs werden.
Im Labor haben Forscher versucht, Tumorzellen zu erzeugen, indem sie wichtige regulatorische Proteine verändert oder eingeführt haben. In mehreren Studien wurde versucht, die minimale Anzahl der genetischen Veränderungen zu bestimmen, die für die Entstehung einer Krebszelle erforderlich sind, mit verblüffenden Ergebnissen.3
In der Natur können sich Mutationen im Laufe der Zeit in Zellen ansammeln, und wenn die „richtige“ Gruppe von Genen mutiert ist, kann Krebs entstehen. Eine Studie aus dem Jahr 2012 hat gezeigt, dass sich in den Stammzellen des Knochenmarks eines gesunden Menschen mit zunehmendem Alter viele Mutationen ansammeln. Schon wenige weitere Veränderungen an Schlüsselgenen können Krebs auslösen. Die Ergebnisse deuten darauf hin, dass sich „normale“ Zellen und Krebszellen in vielen Fällen gar nicht so sehr unterscheiden.4
Vererbte Mutationen bei Krebs
Erschwerend kommt hinzu, dass die Veränderungen, die zur Entstehung einer Krebszelle erforderlich sind, auf viele verschiedene Arten erreicht werden können. Obwohl alle Krebsarten dasselbe Spektrum an Regulierungsfunktionen überwinden müssen, um zu wachsen und sich weiterzuentwickeln, können sich die beteiligten Gene unterscheiden. Auch die Reihenfolge, in der die Gene de-reguliert werden oder verloren gehen, kann variieren. So können beispielsweise bei Darmkrebstumoren von zwei verschiedenen Personen sehr unterschiedliche Gruppen von Tumorsuppressoren und Onkogenen beteiligt sein, auch wenn das Ergebnis (Krebs) dasselbe ist.
Die große Heterogenität von Krebserkrankungen, selbst wenn sie dasselbe Organ betreffen, macht Diagnose und Behandlung kompliziert. Die derzeitigen Fortschritte bei der molekularen Klassifizierung von Tumoren dürften eine rationelle Gestaltung von Behandlungsprotokollen auf der Grundlage der in einem bestimmten Fall tatsächlich beteiligten Gene ermöglichen. Neue diagnostische Tests können das Screening von Hunderten oder Tausenden von Genen umfassen, um ein individuelles Profil des Tumors einer Person zu erstellen. Diese Informationen dürften es ermöglichen, Krebsbehandlungen auf die jeweilige Person zuzuschneiden. Weitere Informationen hierzu finden Sie im Abschnitt Genomik/Proteomik.
Die genetischen Veränderungen, die zu unkontrolliertem Zellwachstum führen, können auf zwei verschiedene Arten erworben werden. Es ist möglich, dass die Mutation allmählich über mehrere Jahre hinweg auftritt und zur Entwicklung einer „sporadischen“ Krebserkrankung führt. Alternativ dazu ist es möglich, funktionsgestörte Gene zu vererben, was zur Entwicklung einer familiären Form einer bestimmten Krebsart führt. Einige Beispiele für Krebsarten mit bekannter erblicher Komponente sind:
- Brustkrebs- Die Vererbung von mutierten Versionen der BRCA1- und BRCA2-Gene sind bekannte Risikofaktoren. Obwohl viele, wenn nicht sogar die meisten, an Brustkrebs erkrankten Personen keine nachweisbaren Veränderungen in diesen Genen haben, erhöht eine mutierte Form die Wahrscheinlichkeit, an Brustkrebs zu erkranken.
- Dickdarmkrebs- Defekte in DNA-Reparaturgenen wie MSH2 prädisponieren bekanntermaßen für erblichen nicht-polypösen Dickdarmkrebs (HNPCC).
- Retinoblastom- Defekte im Rb-Tumorsuppressor-Gen sind als Ursache für diesen Augenkrebs und verschiedene andere Krebsarten bekannt. Mehr über diese spezielle Krankheit finden Sie im Abschnitt über Rb
Dies ist eine unvollständige Liste der bekannten vererbten Krebsarten, und es ist sicher, dass weitere vererbte Krebsformen identifiziert werden, wenn die Genetik verschiedener Krebsarten geklärt ist.
Weitere Informationen zu diesem Thema finden Sie in den Kapiteln 2 und 4 von The Biology of Cancer von Robert A. Weinberg.
Arten von Mutationen
Der Prozess, durch den Proteine hergestellt werden, die Translation, basiert auf dem „Lesen“ der mRNA, die durch den Prozess der Transkription erzeugt wurde. Jede Veränderung der DNA, die für ein Gen kodiert, führt zu einer Veränderung der produzierten mRNA. Die veränderte mRNA kann wiederum zur Produktion eines Proteins führen, das nicht mehr richtig funktioniert. Selbst die Veränderung eines einzigen Nukleotids entlang der DNA eines Gens kann zu einem völlig funktionsunfähigen Protein führen.
Es gibt verschiedene Möglichkeiten, wie die DNA verändert werden kann. Im folgenden Abschnitt werden die verschiedenen Arten von genetischen Veränderungen näher beschrieben.
Punktmutationen
Genetische Veränderungen können in zwei allgemeine Kategorien eingeteilt werden. Die erste Kategorie umfasst Veränderungen, die nur ein oder wenige Nukleotide entlang eines DNA-Strangs verändern. Diese Arten von Veränderungen werden als Punktmutationen bezeichnet.
Wenn Ribosomen ein Boten-RNA-Molekül lesen, werden alle drei Nukleotide als eine Aminosäure interpretiert. Diese Drei-Buchstaben-Codes werden Codons genannt. Um eine Analogie zu einem englischen Satz herzustellen: „The fat cat ate the rat“ würde 6 Codons enthalten. Die durch Mutation verursachten Veränderungen können zu Sätzen wie „Die fette Fledermaus fraß die Ratte“ oder „Die fette Katze fraß die Ratte“ oder „Die fette Katze fraß die Ratte…“ führen. Die Auswirkungen auf das Protein hängen davon ab, wo die Veränderung auftritt und welche Art von Veränderung vorliegt.
Die von den Ribosomen gelesenen Drei-Buchstaben-Codons können durch Mutation auf eine von drei Arten verändert werden:
Nonsense-Mutationen
Das neue Codon führt dazu, dass das Protein vorzeitig beendet wird, wodurch ein Protein entsteht, das verkürzt ist und oft nicht richtig oder gar nicht funktioniert.
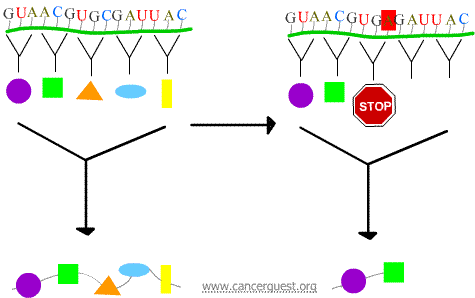
Missense-Mutationen
Das neue Codon bewirkt, dass eine falsche Aminosäure in das Protein eingebaut wird. Die Auswirkungen auf die Funktion des Proteins hängen davon ab, was anstelle der normalen Aminosäure eingefügt wird.

Frameshift-Mutationen
Der Verlust oder Gewinn von 1 oder 2 Nukleotiden führt dazu, dass das betroffene Codon und alle darauf folgenden Codons falsch gelesen werden. Dies führt zu einem sehr unterschiedlichen und oft nicht funktionsfähigen Proteinprodukt.
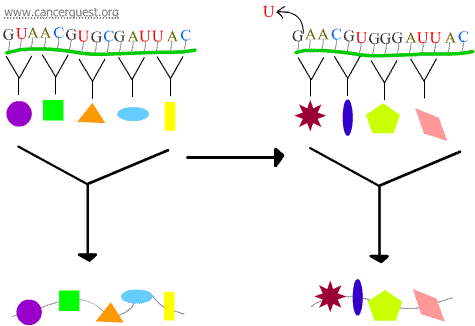
Transkriptionsfehler
Ein Teil der DNA-Schäden führt zu einem veränderten Nukleotid oder einer kleinen Gruppe von Nukleotiden, die von der RNA-Polymerase nicht „gelesen“ werden können. Wenn der RNA-Polymerase-Komplex diese Stellen erreicht, umgeht er manchmal den Schaden, indem er Nukleotide hinzufügt, um weiterzumachen, auch wenn das bedeutet, dass er die falschen Nukleotide einfügt. Dieser Prozess wird als transkriptionelle Mutagenese bezeichnet und kann bei der Entstehung von Krebs eine wichtige Rolle spielen.5
Translokationen
Eine weitere Kategorie von Mutationen umfasst Veränderungen größerer DNA-Mengen, oft auf der Ebene des Chromosoms. Dabei handelt es sich um Translokationen, bei denen Chromosomenfragmente gebrochen und verschoben werden. Oft ermöglichen Brüche in zwei verschiedenen Chromosomen die Bildung von zwei „neuen“ Chromosomen mit neuen Genkombinationen.
Auch wenn es den Anschein hat, dass dies keine großen Probleme verursachen würde, da alle Gene noch vorhanden sind, kann der Prozess auf verschiedene Weise zu einem gestörten Zellwachstum führen-
1. Die Gene werden am neuen Ort möglicherweise nicht richtig transkribiert und translatiert.
2. Die Verschiebung eines Gens kann zu einer Zunahme oder Abnahme seiner Transkription führen.
3. Der Bruch und die Wiedervereinigung können auch innerhalb eines Gens auftreten (wie oben in grün dargestellt), was zu seiner Inaktivierung führt.
Bei einigen Krebsarten sind bestimmte Translokationen sehr häufig und können sogar zur Diagnose der Krankheit herangezogen werden. Translokationen kommen häufig bei Leukämien und Lymphomen vor, während sie bei Krebserkrankungen des festen Gewebes weniger häufig festgestellt werden. Ein Beispiel ist ein Austausch zwischen den Chromosomen 9 und 22, der bei über 90 % der Patienten mit chronischer myeloischer Leukämie (CML) auftritt. Der Austausch führt zur Bildung einer verkürzten Form des Chromosoms 22, die als Philadelphia-Chromosom (nach dem Ort seiner Entdeckung) bezeichnet wird. Diese Translokation führt zur Bildung eines Onkogens aus dem abl-Proto-Onkogen.67
Andere Krebsarten, die häufig (oder immer) mit bestimmten Translokationen in Verbindung gebracht werden, sind das Burkitt-Lymphom, B-Zell-Lymphome und verschiedene Leukämiearten.
Genamplifikation
Bei diesem sehr ungewöhnlichen Prozess ist der normale DNA-Replikationsprozess stark gestört. Das Ergebnis ist, dass statt einer einzigen Kopie einer Chromosomenregion viele Kopien hergestellt werden. Dies führt dazu, dass viele Kopien der Gene entstehen, die sich in diesem Bereich des Chromosoms befinden. Manchmal werden so viele Kopien der amplifizierten Region hergestellt, dass sie sogar ihre eigenen kleinen Pseudochromosomen, die so genannten Doppelminutenchromosomen, bilden können.
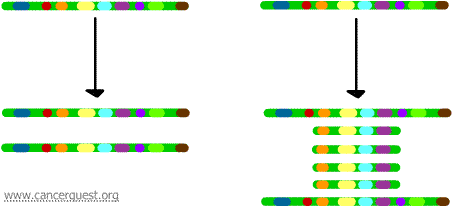
Die Gene auf jeder der Kopien können transkribiert und übersetzt werden, was zu einer Überproduktion der mRNA und des Proteins führt, die den amplifizierten Genen entsprechen, wie unten dargestellt. Die verschnörkelten Linien stellen die mRNA dar, die durch die Transkription jeder Kopie des Gens produziert wird.
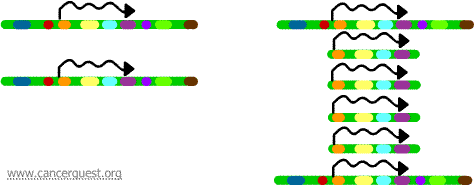
Während dieser Prozess in normalen Zellen nicht zu beobachten ist, tritt er in Krebszellen recht häufig auf. Wenn ein Onkogen in der amplifizierten Region enthalten ist, kann die daraus resultierende Überexpression dieses Gens zu einem deregulierten Zellwachstum führen. Beispiele hierfür sind die Amplifikation des Myc-Onkogens in einer Vielzahl von Tumoren und die Amplifikation des ErbB-2- oder HER-2/neu-Onkogens bei Brust- und Eierstockkrebs. Im Falle des HER-2/neu-Onkogens wurden klinische Behandlungen entwickelt, die auf Zellen abzielen, die das Proteinprodukt überexprimieren.
Genamplifikation trägt auch zu einem der größten Probleme bei der Krebsbehandlung bei: der Arzneimittelresistenz. Medikamentenresistente Tumore können selbst bei Vorhandensein von Chemotherapeutika weiter wachsen und sich ausbreiten. Ein häufig betroffenes Gen ist das MDR-Gen (Multiple Drug Resistance). Das Proteinprodukt dieses Gens wirkt wie eine Pumpe, die sich in der Zellmembran befindet. Es ist in der Lage, selektiv Moleküle aus der Zelle herauszuschleusen, darunter auch Chemotherapeutika. Durch diese Entfernung werden die Medikamente unwirksam.
Dies wird im Abschnitt über Medikamentenresistenz ausführlicher behandelt. Die Verstärkung verschiedener Gene kann andere Chemotherapeutika unwirksam machen.
Inversionen, Duplikationen und Deletionen
Inversionen
Bei diesen Veränderungen werden DNA-Abschnitte aus einem Chromosom herausgelöst und dann in umgekehrter Richtung wieder eingefügt. Wie in den vorangegangenen Beispielen kann diese Umlagerung zu einer anormalen Genexpression führen, entweder durch Aktivierung eines Onkogens oder durch Deaktivierung eines Tumorsuppressorgens.
Duplikationen/Löschungen
Durch Replikationsfehler kann ein Gen oder eine Gruppe von Genen mehr als einmal innerhalb eines Chromosoms kopiert werden. Dies unterscheidet sich von der Genamplifikation dadurch, dass die Gene nicht außerhalb des Chromosoms repliziert werden und sie nur ein einziges Mal zusätzlich kopiert werden, nicht hunderte oder tausende Male. Gene können auch durch ein Versagen des Replikationsprozesses oder andere genetische Schäden verloren gehen.

Aneuploidie
Aneuploidie ist eine genetische Veränderung, die den Verlust oder die Zunahme ganzer Chromosomen beinhaltet. Aufgrund von Problemen bei der Zellteilung kann es vorkommen, dass sich die replizierten Chromosomen nicht korrekt auf die Tochterzellen aufteilen. Dies kann zu Zellen führen, die zu viele oder zu wenige Chromosomen haben. Ein Beispiel für einen recht häufigen aneuploiden Zustand, der nichts mit Krebs zu tun hat, ist das Down-Syndrom, bei dem eine zusätzliche Kopie des Chromosoms 21 in allen Zellen des betroffenen Individuums vorhanden ist.
In der folgenden Animation werden Kopien von zwei Chromosomen hergestellt, aber wenn sich die Zelle teilt, werden die Chromosomen nicht gleichmäßig auf die beiden entstehenden Zellen (Tochterzellen) verteilt. Das Ergebnis ist, dass eine der Zellen zu viele Chromosomen hat und eine nicht genug.
Krebszellen sind sehr oft aneuploid. Der Mensch hat normalerweise 46 Chromosomen in seinen Zellen, aber Krebszellen haben oft viel mehr, manchmal mehr als 100. Das Vorhandensein der zusätzlichen Chromosomen macht die Zellen instabil und stört die Kontrolle der Zellteilung erheblich. Derzeit wird darüber diskutiert, ob alle Krebsarten aneuploid sind oder nicht. Unabhängig davon, ob dies der Fall ist, steht fest, dass Aneuploidie ein häufiges Merkmal von Krebszellen ist.
Epigenetische Veränderungen
Neben den eigentlichen Veränderungen der DNA-Sequenz kann die Genexpression durch Veränderungen der DNA und des Chromatins, die die Sequenz nicht verändern, verändert werden. Da diese Veränderungen nicht die Sequenz der DNA in den Genen verändern, werden sie als epigenetische Veränderungen bezeichnet. Im Folgenden werden zwei Arten von epigenetischen Veränderungen beschrieben.
Methylierung
Bei dieser Veränderung werden einige Nukleotide in der DNA durch Anhängen einer Methylgruppe (-CH3) an die Base modifiziert. Die Methylierung der DNS ist mit der Inaktivierung dieses bestimmten Bereichs der DNS verbunden. Abnormale DNA-Methylierungsmuster wurden in Krebszellen festgestellt. Wie die beschriebenen Veränderungen verändert die Methylierung die Expression der betroffenen Gene.
Acetylierung
Bei dieser epigenetischen Veränderung werden die Histonproteine, um die die DNA gewickelt ist, durch das Hinzufügen von Acetylgruppen (-CH3CHO) verändert. Diese Veränderung führt zu einer Lockerung der Wechselwirkung zwischen DNA und Histon und ist mit einer erhöhten Genexpression verbunden. Die Modifizierung der Prozesse des Hinzufügens und Entfernens von Acetylgruppen an der DNA ist ein aktiver Bereich der Krebsbehandlungsforschung.
Mehr über epigenetische Veränderungen und Krebsbehandlungen.
Ursachen von Mutationen
Wie wir gesehen haben, entstehen Krebszellen aus normalen Vorläuferzellen durch eine Anhäufung von genetischen Schäden. Die Mechanismen, durch die die Veränderungen hervorgerufen werden, sind vielfältig. Im weitesten Sinne lassen sich die Auslöser genetischer Veränderungen (Mutationen) vor allem in die nachstehend beschriebenen Kategorien einteilen, auf die im folgenden Abschnitt näher eingegangen wird.
Spontanmutationen
Spontanmutationen: Die Basen (A, T, G, C) in der DNA werden aufgrund von nicht reparierten Replikationsfehlern oder zufälligen molekularen Ereignissen verändert oder gehen verloren. So führt beispielsweise der Verlust einer Aminogruppe von Cytosin, einer normalen Base in der DNA, zur Bildung von Uracil, einer Base, die normalerweise nicht in der DNA vorkommt. Wenn diese Veränderung nicht erkannt und rückgängig gemacht wird, kann eine Mutation entstehen. Gelegentlich kann eine ganze Base verloren gehen, wenn die Bindung zwischen dem DNA-Rückgrat und der Base gespalten wird. Dies führt zu einer Lücke in der DNA-Doppelhelix, die, wenn sie nicht repariert wird, beim nächsten Kopieren der DNA (d. h. bei der Replikation) zu einer Mutation führen kann.
Induzierte Mutationen
Induzierte Mutationen: Mutationen können ausgelöst werden, indem Organismen (oder Zellen) einer Vielzahl von Behandlungen ausgesetzt werden. Einige der häufigsten sind:
Strahlung- Als eines der ersten bekannten Mutagene ist Strahlung ein starker Auslöser von Mutationen. Verschiedene Arten von Strahlung verursachen unterschiedliche Arten von genetischen Veränderungen. Ultraviolette (UV) Strahlung verursacht Punktmutationen. Röntgenstrahlen können Brüche in der DNA-Doppelhelix verursachen und zu Translokationen, Inversionen und anderen Arten von Chromosomenschäden führen. Die Exposition gegenüber UV-Strahlen im Sonnenlicht wird mit Hautkrebs in Verbindung gebracht. Die DNA-schädigenden Eigenschaften von Strahlung wurden bei verschiedenen strahlungsbasierten Krebsbehandlungen genutzt.
Die folgende Abbildung zeigt eine Art von Mutation, die durch ultraviolette Strahlung verursacht wird. In diesem Beispiel führt der Beschuss der DNA-Doppelhelix durch UV-Strahlen dazu, dass sich zwei Basen miteinander verbinden. Dies verändert die Struktur der DNS und kann zu dauerhaften Veränderungen führen, wenn sie nicht repariert werden.
Eine andere Art von Strahlung ist die Energie, die von natürlich vorkommenden radioaktiven Elementen (wie Radon und Uran) oder von künstlichen Quellen, wie sie in Kernreaktoren gefunden (und erzeugt) werden, abgegeben wird. Es gibt verschiedene Arten von Strahlung, die verschiedene Arten von Schäden an Zellen und Geweben verursachen können. Strahlung kann die DNA direkt schädigen oder die Bildung chemischer Stoffe (d. h. reaktiver Sauerstoffspezies oder ROS) verursachen, die dann die DNA oder andere Zellbestandteile schädigen können.
Die Exposition gegenüber Strahlung aus radioaktiven Materialien ist gut dokumentiert. Analysen von Überlebenden der Atombombenabwürfe auf Japan während des Zweiten Weltkriegs zeigten eine starke Zunahme von Leukämien kurz nach der Exposition und dann eine Zunahme anderer Krebsarten in den folgenden Jahrzehnten.8
Gefährliche Mengen radioaktiver Stoffe wurden auch versehentlich aus Kernkraftwerken freigesetzt. Die Strahlenbelastung durch die unbeabsichtigte Freisetzung radioaktiver Stoffe aus dem Kernreaktor von Tschernobyl wurde mit einer Zunahme von Schilddrüsenkrebs und anderen bösartigen Krebsarten in Verbindung gebracht.9
Medizinische Bildgebungsgeräte (wie Röntgengeräte und CT-Scanner) setzen Patienten ebenfalls Strahlung aus. Die Mengen, die für einen einzelnen Test verwendet werden, dürften keine signifikanten Mengen an Krebs verursachen, aber die langfristigen Auswirkungen vieler Tests über einen Zeitraum von Jahren sind nicht klar.10 Auch die Exposition von Flugpassagieren bei Ganzkörperscans auf Flughäfen dürfte kein Krebsrisiko darstellen.11 Passagiere in Flugzeugen sind ebenfalls der Strahlung aus dem Weltraum ausgesetzt, allerdings auf niedrigem Niveau, und es wird nicht davon ausgegangen, dass sie ein Krebsrisiko darstellen, auch nicht für Mitglieder des Flugpersonals.1112
Chemische Mutagene- Viele verschiedene Chemikalien sind dafür bekannt, Mutationen zu verursachen. Diese Chemikalien üben ihre Wirkung aus, indem sie sich an die DNA oder die Bausteine der DNA binden und die Replikations- oder Transkriptionsprozesse stören. Einige Beispiele für starke Mutagene sind Benzo-a-pyren, eine Chemikalie, die in Zigarettenrauch vorkommt, und Aflatoxin, ein Mutagen, das am häufigsten in unsachgemäß gelagerten landwirtschaftlichen Erzeugnissen vorkommt.
Chronische Entzündungen- Chronische Entzündungen können aufgrund der Produktion mutagener Chemikalien durch die Zellen des Immunsystems zu DNA-Schäden führen. Ein Beispiel ist die langfristige Entzündung, die durch eine Infektion mit dem Hepatitis-Virus verursacht wird. Erfahren Sie mehr über Viren und Krebs.
Sauerstoffradikale – Bei der Gewinnung von Energie aus der Nahrung, die in unseren Mitochondrien stattfindet, können Chemikalien entstehen, die sehr reaktiv sind und die Zellmembranen und die DNA selbst schädigen können. Diese reaktiven Sauerstoffzwischenprodukte (ROI) können auch entstehen, wenn die Zellen einer Strahlung ausgesetzt werden, wie unten gezeigt.
Die mutagene Aktivität von ROI steht im Zusammenhang mit der Entwicklung von Krebs sowie mit der Wirkung verschiedener Krebsbehandlungen, einschließlich Strahlen- und Chemotherapie. 131415
Abnormale Zellteilung
Während der Mitose ist es möglich, dass der Zellteilungsprozess die replizierten Chromosomen nicht korrekt auf zwei Tochterzellen aufteilt. Ein solcher Fehler führt zur Bildung von aneuploiden Zellen. Den Zellen fehlt entweder ein Gen, oder sie haben eine beträchtliche Anzahl von Genen hinzugewonnen. Durch diesen seltenen Prozess können Zellen entstehen, die anfälliger für eine unkontrollierte Zellteilung sind. Wie bereits erwähnt, ist ein großer Prozentsatz der beim Menschen isolierten Krebsarten aneuploid.
Wenn eine Zelle eine Mutation in einem Gen aufweist, dessen Proteinprodukt für die „Kontrolle“ des Teilungsprozesses verantwortlich ist, können die Dinge schnell außer Kontrolle geraten, und die Tochterzellen jeder Teilung können zunehmend abnormal werden.
Viren als Mutagene
Viren werden für einen erheblichen Prozentsatz der Krebsfälle verantwortlich gemacht. Viren können auf verschiedene Weise Krebs verursachen, und die Art und Weise, wie jeder Virustyp wirkt, ist wahrscheinlich etwas anders. Einige Viren (darunter viele Retroviren) können Mutationen verursachen, indem sie ihre Gene in das Genom der infizierten Zelle einfügen. Die eingefügte DNA kann die Aktivität der betroffenen Gene zerstören oder verändern.161718
Viren können auch auf indirekte Weise Mutationen verursachen. Ein Beispiel: Eine Infektion mit dem Hepatitis-Virus kann viele Jahre andauern. Während dieser Zeit versucht das körpereigene Abwehrsystem, das Virus loszuwerden, indem es giftige Chemikalien produziert. Diese Chemikalien können ansonsten gesunde Zellen schädigen und sie auf den Weg zu Krebs bringen. Es gibt zahlreiche weitere Möglichkeiten, wie Viren Krebs verursachen können.1920
Aufgrund der Bedeutung von Viren bei der Entstehung vieler Krebsarten haben wir einen Abschnitt über Viren und Krebs eingerichtet.
Transposons als Mutagene
Transposons sind kurze DNA-Sequenzen, die die Fähigkeit haben, sich von einem Ort in der DNA zu einem anderen Ort zu bewegen. Transposons kodieren ein Enzym, die Transposase, das das Transposon an neue Stellen im Genom spleißt (siehe Schema eines Transposons unten links). Transposons wurden von Barbara McClintock entdeckt, die für ihre Arbeit einen Nobelpreis erhielt.2122 Das menschliche Genom enthält viele inaktivierte Kopien von Transposons, die ihre Fähigkeit verloren haben, sich an neue Stellen zu bewegen oder zu „springen“. Etwa 50 % des menschlichen Genoms besteht aus „toten“ Transposons.23
Die Bewegung aktiver Transposons kann zu Mutationen führen, die die Aktivität von Genen verändern. Ein sichtbares Beispiel für die Bewegung von Transposons (Transposition genannt) ist die Färbung der Körner in indischem Mais (siehe unten rechts). Es wird angenommen, dass die Transposons, die beim Menschen aktiv sind, an menschlichen Krankheiten, einschließlich Krebs, beteiligt sind.242526


Mutation Zusammenfassung
Genetische Veränderung (Mutation) Einleitung
- Die abnormen Verhaltensweisen von Krebszellen sind das Ergebnis einer Reihe von Mutationen in wichtigen regulatorischen Genen (d.h. DNA-Reparaturgenen).
- Man geht davon aus, dass die meisten Krebsarten aus einer einzigen Vorläuferzelle entstehen, die genügend Mutationen erhält, um zu einer Krebszelle zu werden.
DNA-Mutationen
- Genetische Veränderungen können klein sein und nur ein oder wenige Nukleotide betreffen (Punktmutationen) oder sie können ziemlich groß sein und die Struktur eines oder mehrerer Chromosomen verändern.
- Punktmutationen
- Translation ist die Herstellung eines Proteins durch Enzyme, die drei Nukleotid-„Wörter“ (Codons) entlang einer Boten-RNA (mRNA) „lesen“.
- Auch die Veränderung eines einzigen Nukleotids entlang der DNA eines Gens kann zu einem völlig funktionsunfähigen Protein führen. Die Mutationen werden nach den Veränderungen gruppiert, die sie im resultierenden Proteinprodukt des betroffenen Gens hervorrufen.
- Nonsense-Mutationen – Das neue (mutierte) Codon führt zu einem vorzeitigen Stopp der Proteinsynthese.
- Missense-Mutationen – Das veränderte Codon führt zum Einbau einer falschen Aminosäure in das Protein.
- Frameshift-Mutationen – Der Verlust oder Gewinn von 1 oder 2 Nukleotiden in einer mRNA führt dazu, dass Codons falsch gelesen werden. Dies führt häufig zu verkürzten und nicht funktionsfähigen Proteinen.
- Chromosomenveränderungen
- Translokationen – Bruch und (manchmal) Austausch von Chromosomenfragmenten.
- Genamplifikation – Durch abnormale Replikation entstehen mehrere Kopien einer Region eines Chromosoms. Dies führt letztlich zu einer Überproduktion der entsprechenden Proteine.
- Inversionen – DNA-Abschnitte werden aus einem Chromosom herausgelöst und dann in der entgegengesetzten Richtung wieder eingefügt.
- Duplikationen/Löschungen – Ein Gen oder eine Gruppe von Genen kann ganz verloren gehen oder innerhalb eines Chromosoms mehrfach kopiert werden.
- Aneuploidie – Eine genetische Veränderung, die den Verlust oder die Zunahme ganzer Chromosomen beinhaltet.
- Spontane Mutationen können aufgrund nicht reparierter DNA oder zufälliger molekularer Ereignisse auftreten.
- Aneuploidie ist in Krebszellen sehr häufig.
Epigenetische Veränderungen
- Die Genexpression kann durch Veränderungen der DNA und des Chromatins verändert werden, die nicht die genetische Sequenz betreffen. Beispiele hierfür sind die DNA-Methylierung und die Acetylierung von Histonen.
- Methylierung – Einige Nukleotide in der DNA werden durch das Hinzufügen einer Methylgruppe verändert, was mit der Inaktivierung dieser DNA-Region verbunden ist
- Acetylierung – Das Hinzufügen von Acetylgruppen lockert die DNA und erhöht die Genexpression.
Induzierte Mutationen
- Mutationen können induziert werden, indem Organismen (oder Zellen) einer Vielzahl von Behandlungen ausgesetzt werden:
- Strahlung – UV-Strahlen verursachen Punktmutationen und Röntgenstrahlen verursachen mehrere Formen von Schäden.
- Chemische Mutagene – können sich an die DNA oder die Bausteine der DNA binden und die Replikations- oder Transkriptionsprozesse stören.
- Chronische Entzündungen – DNA-Schäden aufgrund der Produktion mutagener Chemikalien durch die Zellen des Immunsystems
- Sauerstoffradikale – entstehen bei der Energieproduktion einer Zelle und können die DNA schädigen.
Andere genetische Veränderungen
- Eine fehlerhafte Zellteilung, die zu einer falschen Teilung der Chromosomen führt, kann zu Aneuploidie führen.
- Viren können auf verschiedene Weise genetische Schäden verursachen und werden mit einer Vielzahl von Krebsarten in Verbindung gebracht.
Mutation und Krebs
- Es scheint, dass der Übergang von einer normalen, gesunden Zelle zu einer Krebszelle ein schrittweiser Prozess ist.
- Krebsentwicklung erfordert genetische Veränderungen in mehreren verschiedenen Onkogenen und Tumorsuppressoren.
- Alle Krebsarten müssen dasselbe Spektrum an regulatorischen Funktionen überwinden, um zu wachsen und voranzukommen, aber die beteiligten Gene können sich unterscheiden.
- Die Heterogenität von Krebs erschwert die Diagnose und Behandlung.
- Es ist möglich, dysfunktionale Gene zu vererben, die zur Entwicklung einer familiären Form einer bestimmten Krebsart führen.
Know the Flow: Mutation
Know the Flow ist ein interaktives Spiel, mit dem Sie Ihr Wissen testen können. So spielen Sie:
- Ziehen Sie die entsprechenden Auswahlmöglichkeiten aus der rechten Spalte und setzen Sie sie der Reihe nach in die Kästchen auf der linken Seite. Beachten Sie, dass Sie nur fünf der sechs Möglichkeiten nutzen können, um das Spiel abzuschließen.
- Klicken Sie anschließend auf „Prüfen“, um zu sehen, wie viele Antworten richtig waren.
- Klicken Sie bei falschen Antworten auf „Beschreibung“, um Informationen zu den Prozessen zu erhalten.
- Wenn Sie es noch einmal versuchen möchten, wählen Sie „Zurücksetzen“ und beginnen Sie von vorn.
-
1
-
2
-
3
-
4
-
5
-
Mehr erfahrenEine Zelle befindet sich im Prozess der DNA-Synthese
-
Mehr erfahrenViele Kopien einer Region eines Chromosoms werden hergestellt
-
Mehr erfahrenTranskription von amplifizierten Genen
-
Mehr erfahrenTranslation von amplifizierten Genen
-
Mehr erfahrenÜberproduktion eines Schlüssel Proteins führt zum Wachstum eines arzneimittelresistenten Tumors
-
Mehr erfahrenDuplizierung findet statt
Nochmals spielen
- 1. Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). Campbell Biology (11th ed.). Pearson.
- 2. Surveillance, Epidemioloy, and End Results (SEER) vertreten durch National Cancer Institute
- 3. Hahn WC, Counter CM, Lundberg AS, Beijerbergen RL, Brooks MW, Weinberg RA. „Erzeugung von menschlichen Tumorzellen mit definierten genetischen Elementen“. Nature 400: 464-468
- 4. Welch JS, Ley TJ, Link DC, Westervelt P, Walter MJ, Graubert TA, DiPersio JF, Ding L, Mardis ER, Wilson RK et al. The origin and evolution of mutations in acute myeloid leukemia. Cell, July 20, 2012
- 5. Brégeon D, Doetsch PW. Transkriptionsmutagenese: Ursachen und Beteiligung an der Tumorentwicklung. Nat Rev Cancer. 2011 Mar;11(3):218-27.
- 6. Nowell PC, Hungerford DA. „Chromosomenstudien an normalen und leukämischen menschlichen Leukozyten“. J Natl Cancer Inst (1960). 25: 85-100.
- 7. Rowley JD. „Eine neue konsistente Chromosomenanomalie bei chronischer myelogener Leukämie, identifiziert durch Quinacrin-Fluoreszenz und Giemsa-Färbung.“ Nature (1973). 243: 290-293.
- 8. Ozasa K, Shimizu Y, Sakata R, Sugiyama H, Grant EJ, Soda M, Kasagi F, Suyama A. RISK OF CANCER AND NON-CANCER DISEASES IN THE ATOMIC BOMB SURVIVORS. Radiat Prot Dosimetry. 2011 Apr 18.
- 9. Cardis E, Hatch M. The Chernobyl accident–an epidemiological perspective. Clin Oncol (R Coll Radiol). 2011;23(4):251-260. doi:10.1016/j.clon.2011.01.510 Mar 9.
- 10. Fazel R, Krumholz HM, Wang Y, Ross JS, Chen J, Ting HH, Shah ND, Nasir K, Einstein AJ, Nallamothu BK. Exposition gegenüber niedrig dosierter ionisierender Strahlung bei medizinischen Bildgebungsverfahren. N Engl J Med. 2009 Aug 27;361(9):849-57.
- 11. a. b. Mehta P, Smith-Bindman R. Airport Full-Body Screening: What Is the Risk? Arch Intern Med. 2011 Mar 28.
- 12. Bagshaw M. Kosmische Strahlung in der kommerziellen Luftfahrt. Travel Med Infect Dis. 2008 May;6(3):125-7. Epub 2007 Nov 26.
- 13. Kang DH. „Oxidativer Stress, DNA-Schäden und Brustkrebs“. AACN Clin Issues. (2002). 13:540-549
- 14. Athar M. „Oxidativer Stress und experimentelle Karzinogenese.“ Indian J. Exp. Biol. (2002). 40:656-667
- 15. Marnett LJ. „Oxy-Radikale, Lipidperoxidation und DNA-Schäden.“ (2002)181-182:219-222
- 16. Nair V. Retrovirus-induzierte Onkogenese und Sicherheit von retroviralen Vektoren. Curr Opin Mol Ther. 2008 Oct;10(5):431-8.
- 17. Brady G, Macarthur GJ, Farrell PJ. Epstein-Barr-Virus und Burkitt-Lymphom. Postgrad Med J. 2008 Jul;84(993):372-7.
- 18. Ruprecht K, Mayer J, Sauter M, Roemer K, Mueller-Lantzsch N. Endogenous retroviruses and cancer. Cell Mol Life Sci. 2008 Nov;65(21):3366-82.
- 19. Lupberger J, Hildt E. Hepatitis B virus-induced oncogenesis. World J Gastroenterol. 2007 Jan 7;13(1):74-81.
- 20. Castello G, Scala S, Palmieri G, Curley SA, Izzo F. HCV-related hepatocellular carcinoma: Von der chronischen Entzündung zum Krebs. Clin Immunol. 2010 Mar;134(3):237-50. Epub 2009 Nov 11.
- 21. McClintock B. The origin and behavior of mutable loci in maize. Proc Natl Acad Sci U S A. 1950 Jun;36(6):344-55.
- 22. McClintock, Barbara Nobelpreisvorlesung
- 23. Burns KH, Boeke JD. Human transposon tectonics. Cell. 2012 May 11;149(4):740-52.
- 24. Kozeretska IA, Demydov SV, Ostapchenko LI. Mobile genetische Elemente und Krebs. From mutations to gene therapy. Exp Oncol. 2011 Dec;33(4):198-205.
- 25. Solyom S, Kazazian HH Jr. Mobile Elemente im menschlichen Genom: Implikationen für Krankheiten. Genome Med. 2012 Feb 24;4(2):12.
- 26. Iskow RC, McCabe MT, Mills RE, Torene S, Pittard WS, Neuwald AF, Van Meir EG, Vertino PM, Devine SE. Natürliche Mutagenese von menschlichen Genomen durch endogene Retrotransposons. Cell. 2010 Jun 25;141(7):1253-61.