Aminoxide und die Cope-Eliminierung
Aminoxide werden durch Oxidation von 3º-Aminen oder Pyridinen mit Wasserstoffperoxid oder Persäuren (z.z. B. ZOOH, wobei Z=H oder Acyl).
\
Aminoxide sind relativ schwache Basen, pKa ca. 4,5, verglichen mit dem Stammamin. Die koordinative kovalente N-O-Funktion ist polar, wobei der Sauerstoff ein starker Wasserstoffbrückenbindungsakzeptor ist. Besteht einer der Alkylsubstituenten aus einer langen Kette, wie z. B. C12H25, ist das resultierende Aminoxid ein amphoteres Tensid und findet Verwendung in Shampoos und anderen milden Reinigungsmitteln.
Eine zur Hofmann-Eliminierung komplementäre Eliminierungsreaktion findet statt, wenn 3º-Aminoxide auf Temperaturen von 150 bis 200 ºC erhitzt werden. Diese Reaktion wird als Cope-Eliminierung bezeichnet. Sie wird in der Regel durch tropfenweise Zugabe einer Aminoxidlösung in ein beheiztes, mit kleinen Glaskügelchen gefülltes Rohr durchgeführt. Ein durch die Säule strömender Stickstoffgasstrom befördert die flüchtigen Alkenprodukte in einen gekühlten Behälter. Das stickstoffhaltige Produkt ist ein Hydroxylamin. Im Gegensatz zur Hofmann-Eliminierung findet diese Reaktion durch eine konzertierte zyklische Reorganisation statt, wie im folgenden Diagramm dargestellt. Bei einem solchen Mechanismus stehen die beta-Wasserstoff- und Aminoxidgruppen notwendigerweise in einer syn-Beziehung.
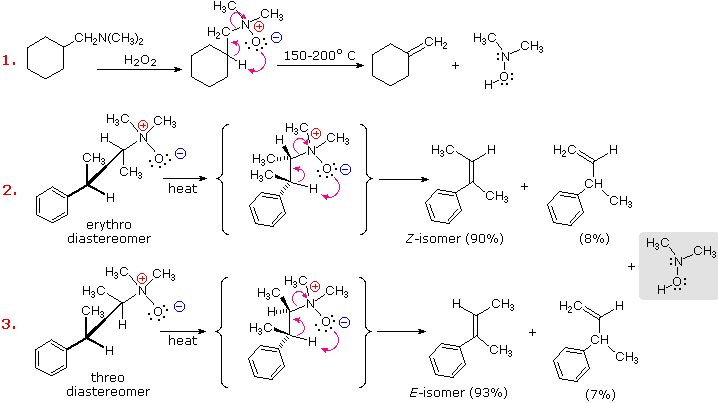
Die Cope-Eliminierung diastereomerer Aminoxide, wie sie in den obigen Beispielen Nr. 2 & 3 gezeigt wird, liefert den Beweis für die syn-Beziehung der beta-Wasserstoff- und Aminoxidgruppen. Diese Beispiele zeigen auch eine starke Regioselektivität zugunsten der stabileren Doppelbindung.
Pyrolytische syn-Eliminationen
Aminoxide sind nicht die einzigen Funktionen, die beim Erhitzen eine unimolekulare syn-Elimination durchlaufen. Um Beispiele für andere Fälle zu sehen, klicken Sie hier