US Pharm. 2018;43(12):HS-2-HS-6.
ABSTRACT: Gastrointestinale Blutungen (GIBs) sind eine bedeutende Ursache für Krankenhauseinweisungen in den Vereinigten Staaten. GIBs werden in zwei Typen eingeteilt: obere GI-Blutungen und untere GI-Blutungen. Beide Arten können unterschiedliche Symptome aufweisen und erfordern ein unterschiedliches Management. Obere GI-Blutungen sind von der endoskopischen Therapie abhängig und können in bestimmten Fällen von verschiedenen pharmakologischen Behandlungen wie Protonenpumpeninhibitoren und Makroliden profitieren. Das Management des unteren GIB konzentriert sich auf die Koloskopie und die mechanische Behandlung von Blutungen, mit wenig pharmakologischen Interventionen. Apotheker können diese Patienten an mehreren Punkten der Patientenversorgung effektiv betreuen.
Gastrointestinale Blutungen (GIB) sind ein relativ häufiges medizinisches Problem, das in den Vereinigten Staaten jährlich einen erheblichen Anteil an Morbidität, Krankenhausaufenthalten und sogar Todesfällen verursacht. Die geschätzte Rate an Krankenhausaufenthalten aufgrund von GIB jeglicher Art wird in den USA auf etwa 375 pro 100.000 Einwohner pro Jahr geschätzt.1-3 Für akute GIB-Ereignisse wird in einigen Studien eine 30-Tage-Sterblichkeitsrate von bis zu 14 % ermittelt, während andere Studien von einer Spanne zwischen 6 % und 10 % pro Jahr berichten, wobei die Raten bei Patienten mit zunehmendem Alter und einer höheren Anzahl an zugrundeliegenden Komorbiditäten steigen.4-7 Es wird geschätzt, dass jährlich mehr als 2,5 Milliarden Dollar für die stationäre Behandlung von GIB ausgegeben werden.8
Aufgrund der Art von GIB ist es wichtig, den Krankheitszustand zu differenzieren, da die Lokalisation der Blutung sowohl die Präsentation als auch die Behandlung bestimmen kann (TABELLEN 1-3). In der Vergangenheit basierte die Unterscheidung zwischen oberem GIB (UGIB) und unterem GIB (LGIB) auf der Lokalisation der Blutung in Bezug auf das Ligamentum Treitz.9,10 Nach dieser Definition wird eine Blutung proximal des Ligamentum Treitz als UGIB eingestuft, während eine Blutung distal des Ligamentum Treitz als LGIB eingestuft wird. In der Literatur gibt es zwar auch andere Definitionen, doch in der Praxis hat sich diese Definition durchgesetzt.11,12



Bei der Vorstellung ist die Untersuchung bei Verdacht auf GIB zunächst ähnlich, unabhängig vom Ursprung der Blutung. Die sofortige Untersuchung sollte sich auf die hämodynamische Stabilität des Patienten konzentrieren. Diese Priorität hat sich bei anderen Hämorrhagiemodellen bewährt und gilt auch bei GIB.16-18 Es sollte eine physische Beurteilung von Blutdruck, Herzfrequenz und orthostatischem Status durchgeführt und gegebenenfalls eine Wiederbelebung eingeleitet werden. Diese Wiederbelebung sollte mit intravenöser Flüssigkeitszufuhr beginnen, kann aber auch Transfusionen gepackter roter Blutkörperchen erfordern.
Zusätzliche Untersuchungen von Patienten mit GIB sollten eine gezielte Anamnese umfassen, um die Art, Dauer und mögliche Quelle der Blutung zu ermitteln, sowie Labortests (CBC, BMP, Gerinnungsuntersuchungen).17,18 Bei der Beurteilung dieser Patienten aus Sicht des Apothekers ist es wichtig, alle aktuellen oder kürzlich eingenommenen Medikamente zu beachten, die das Blutungsrisiko erhöhen können, einschließlich Wirkstoffe wie nichtsteroidale Entzündungshemmer, Thrombozytenaggregationshemmer und/oder Antikoagulanzien. Eine frühzeitige Identifizierung dieser Faktoren kann dazu beitragen, sowohl die Diagnose als auch eine angemessene Behandlung zu beschleunigen.
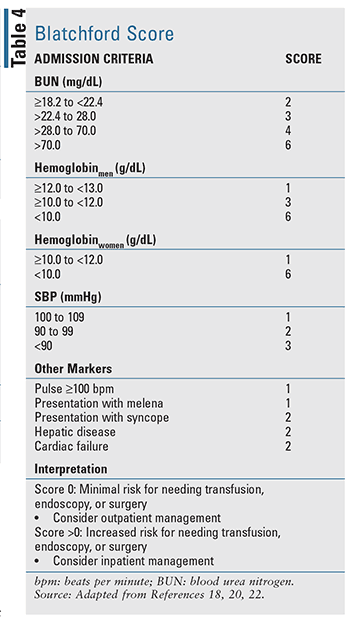
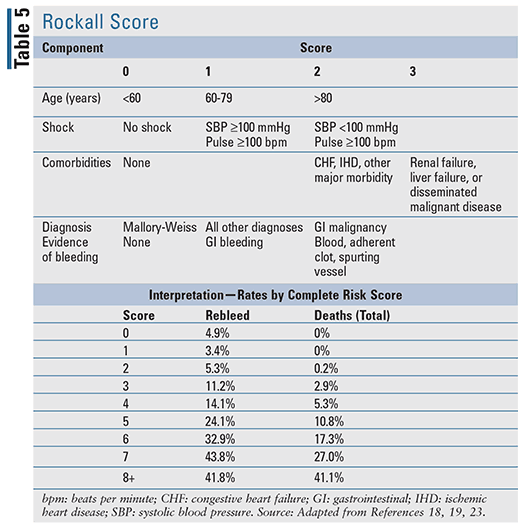
Risikobewertung und -schichtung sind klinisch nützlich, um Patienten mit hohem und niedrigem Risiko für unerwünschte Folgen zu unterscheiden.17,18 Durch die Schichtung von Patienten in bewertete Risikogruppen können erste fundierte Entscheidungen getroffen werden. Insbesondere kann die Stratifizierung Aufschluss über Faktoren wie den Zeitpunkt der Endoskopie oder Koloskopie, die erforderliche Pflegestufe und den Zeitpunkt der Entlassung geben. Für Patienten mit akuter UGIB wurden mehrere klinische Prognoseinstrumente entwickelt, darunter zwei gut bewertete Instrumente, die in evidenzbasierten Leitlinien genannt werden: der Blatchford-Score (TABELLE 4) und der Rockall-Score (TABELLE 5).17-20 Der Rockall-Score verwendet klinische Daten unmittelbar bei der Vorstellung.19 Faktoren zur Beurteilung der Schwere der Blutung, wie systolischer Blutdruck und Herzfrequenz, werden zusammen mit Patientenmerkmalen, wie Alter und Begleiterkrankungen, bewertet, wodurch ein Instrument zur Beurteilung der prognostischen Ergebnisse und möglicherweise der Mortalität entsteht. In ähnlicher Weise verwendet der Blatchford-Score sowohl klinische als auch Labordaten, um die Vorhersage des Interventions- und Sterblichkeitsrisikos zu unterstützen.20 Für akute LGIB sind die verfügbaren Prognoseregeln zur Risikobewertung begrenzt und im Vergleich zu UGIB weniger validiert.22
Pharmakotherapie von Blutungen des oberen Gastrointestinaltrakts
Protonenpumpeninhibitoren (PPI) sind die Medikamentenklasse, die am häufigsten zur Behandlung von UGIB eingesetzt wird. Bei einem UGIB-Patienten kann die Magensäure die Thrombozytenaggregation hemmen und die potenzielle Gerinnung schwächen, was zu einer Beeinträchtigung der Blutstillung führt. Um diesen Prozess zu hemmen, kann die Hemmung der Magensäuresekretion mit dem Ziel, den pH-Wert des Magens auf 6 oder höher anzuheben, dazu beitragen, Gerinnsel zu stabilisieren und die klinischen Ergebnisse zu verbessern.24
PPIs sind insofern einzigartig, als sie sowohl vor als auch nach der Endoskopie eingesetzt werden können. Für die Anwendung vor der Endoskopie gibt es in den Leitlinien keinen Konsens, aber sie können den Anteil der Patienten mit hohem Blutungsrisiko zum Zeitpunkt des Eingriffs verringern.25 Trotz des potenziellen Nutzens in dieser Population gibt es Hinweise darauf, dass die Anwendung von PPI keinen Einfluss auf erneute Blutungen, notwendige Operationen oder die Sterblichkeit hat, was zu einer gewissen klinischen Kontroverse über ihre Anwendung führt. Bei Patienten, bei denen eine Endoskopie nicht durchgeführt werden kann oder verzögert wird, hat sich jedoch gezeigt, dass das Risiko einer erneuten Blutung durch den Einsatz von PPI verringert werden kann. Es gibt Hinweise darauf, dass PPI die Inzidenz von Hochrisiko-Stigmata einer Blutung zum Zeitpunkt der Endoskopie verringern, aber keinen Einfluss auf eine erneute Blutung, einen notwendigen chirurgischen Eingriff oder die Sterblichkeit haben.17,26 Nach der endoskopischen Therapie können PPI sowohl akut als auch chronisch eingesetzt werden.17
Kontinuierliche Infusion gegenüber intermittierendem PPI
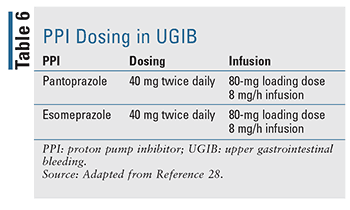
Die angemessene Dosierung und Verabreichung von PPI wurde in den letzten Jahren genau untersucht (TABELLE 6). Eine intravenöse Bolusdosis mit anschließender Infusion war lange Zeit der normale Therapieverlauf und ist in den derzeit verfügbaren Leitlinien nach wie vor die Behandlung der Wahl, aber die Daten deuten darauf hin, dass eine zweimal tägliche intravenöse Bolusdosis in Bezug auf Nachblutungen, Sterblichkeit und Dauer des Krankenhausaufenthalts nicht unterlegen ist.17,27 Die neuere Literatur hat gezeigt, dass die intermittierende Anwendung von PPI nicht unterlegen war und einen klaren Vorteil in Bezug auf die Medikamentendosis, die Kosten und den Ressourcenverbrauch bietet. Die Autoren schlagen vor, die Leitlinien zu aktualisieren, um eine intermittierende PPI-Therapie bei endoskopisch behandeltem GIB zu empfehlen.27 In der Praxis bevorzugen viele Einrichtungen inzwischen eine intermittierende Dosierung, um den Ressourcenverbrauch und die Gesamtkosten zu senken.
Intravenöse PPI versus intravenöse H2-Antagonisten
In Anbetracht der Tatsache, dass H2-Antagonisten (H2As) mit ähnlicher Absicht bei anderen Erkrankungen eingesetzt werden, wurde ihr Einsatz bei UGIB neben PPIs untersucht. Eine Metaanalyse aus dem Jahr 2015, in der die beiden Wirkstoffklassen bei UGIB untersucht wurden, ergab, dass der Unterschied in der Sterblichkeit nicht signifikant war, während Ergebnisse wie die Wiederholungsblutungsrate und die Operationsrate einen klaren Vorteil für PPIs zeigten. Dieses Defizit ist wahrscheinlich auf die Unterlegenheit von H2As bei der Aufrechterhaltung des Magen-pH-Wertes über 6,0 zurückzuführen, dem ungefähren pH-Wert, bei dem Gerinnungsprozesse funktionieren können.29
Makrolide
In dem Bestreben, die Visualisierung während der Endoskopie zu verbessern und damit die Notwendigkeit einer erneuten Endoskopie zu verringern, wird häufig intravenöses Erythromycin, ein antimikrobielles Makrolid, das auch als prokinetisches Mittel wirkt, eingesetzt. Eine Einzeldosis von 250 mg oder 3 mg/kg wird im Allgemeinen gut vertragen.17,30 Eine Metaanalyse aus dem Jahr 2016 kam zu dem Schluss, dass die Anwendung von Erythromycin vor der Endoskopie die Notwendigkeit einer zweiten Endoskopie und die Dauer des Krankenhausaufenthalts signifikant verringert, weshalb es in den Leitlinien der Europäischen Gesellschaft für gastrointestinale Endoskopie empfohlen wird.30,31
Es stellt sich die Frage, ob ein möglicher Nutzen ein Klasseneffekt oder spezifisch für Erythromycin ist. Azithromycin, ein im Allgemeinen häufiger verwendetes Makrolid, wurde untersucht und scheint eine nicht unterlegene Alternative zu Erythromycin zu sein. Azithromycin hat möglicherweise einige logistische Vorteile, wie z. B. die Tatsache, dass es nicht rekonstituiert werden muss und aufgrund seiner Verwendung bei der empirischen Behandlung von Lungenentzündungen im Allgemeinen besser verfügbar ist.32
H pylori-Behandlung
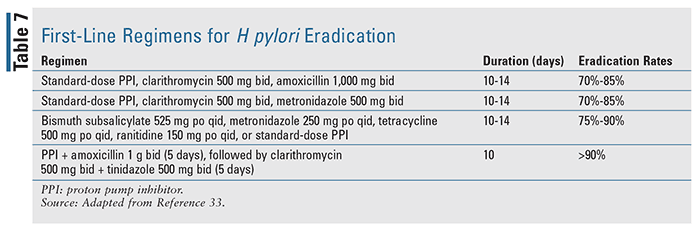
Patienten, bei denen Blutungen im Zusammenhang mit einer Helicobacter pylori-Infektion diagnostiziert werden, sollten mit einer leitliniengerechten Eradikationstherapie behandelt werden, wobei das Ziel die vollständige Beseitigung der Infektion ist.17 Die verfügbare Literatur zeigt, dass die Eradikation von H. pylori bei Patienten mit UGIB deutlich wirksamer ist als eine alleinige antisekretorische Behandlung. Die Erstlinientherapien zur Eradikation von H. pylori sind in TABELLE 7 auf der Grundlage der Leitlinien des American College of Gastroenterology zur Behandlung von H. pylori-Infektionen aufgeführt.33 Sobald die Infektion abgeklungen ist, muss diese Patientengruppe in der Regel keine antisekretorische Erhaltungstherapie erhalten, es sei denn, sie benötigen nichtsteroidale entzündungshemmende Medikamente oder eine antithrombotische Therapie, bei denen eine langfristige antisekretorische Therapie erforderlich ist, da ihre Anwendung das Risiko einer erneuten Blutung erheblich erhöhen kann.17,18
Übersicht über die Behandlung
Nach der anfänglichen Beurteilung und Risikostratifizierung und sobald der Patient hämodynamisch stabil ist, ist die Koloskopie mit anschließender Darmreinigung das erste diagnostische Verfahren für die meisten Patienten, die sich mit einem LGIB vorstellen.21 Das Management von LGIB umfasst meist nicht-pharmakologische Interventionen; es gibt jedoch immer noch Möglichkeiten für Apotheker, in die Patientenversorgung einbezogen zu werden.
PPI-Anwendung bei LGIB
Im Gegensatz zu UGIB zeigt die verfügbare Literatur zur Bewertung der PPI-Anwendung bei LGIB keinen Nutzen. Studien, in denen UGIB und LGIB untersucht wurden, haben gezeigt, dass PPIs zwar keine besseren Ergebnisse bei LGIB zeigen, dass sie aber das Risiko für LGIB erhöhen können.34 Theoretische Mechanismen für dieses erhöhte Risiko konzentrieren sich oft auf mögliche Veränderungen der Mikrobiota und könnten somit ein mögliches Risiko durch NSAIDs verstärken. Diese Ergebnisse sind umstritten; sie sind jedoch ein Beleg dafür, dass Patienten mit LGIB nicht von einer PPI-Therapie profitieren. Dieses potenzielle Risiko sollte bei Patienten, insbesondere bei solchen mit UGIB-Risiko, sorgfältig abgewogen werden, da eine sorgfältige Risiko-Nutzen-Abwägung erforderlich sein kann.34
Die Rolle des Apothekers
Apotheker vieler Fachrichtungen sind in einer einzigartigen Position, um bei der Behandlung und dem Management von GIB-Patienten zu helfen. Ambulante Apotheker sind in einer hervorragenden Position, um proaktiv auf potenzielle Risikofaktoren bei Patienten zu achten, einschließlich hochdosierter NSAIDs und Antikoagulanzien, und das Risiko von GIB an vorderster Front zu verringern. Darüber hinaus können sie Patienten sowohl vor als auch nach einer GIB-Diagnose wichtige Ratschläge geben und die Dosis optimieren. In ähnlicher Weise können auch stationäre klinische Pharmazeuten eine wichtige Rolle bei der Behandlung von GIB spielen. Sie können bei der anfänglichen Bewertung und Behandlung in mehreren Bereichen helfen. Der anfängliche Medikamentenabgleich kann Details aufzeigen, die für die Diagnose und Behandlung der Patienten relevant sind, wie z. B. die Identifizierung der ambulanten Einnahme von NSAID oder Antikoagulantien. Apotheker können dem Behandlungsteam auch Empfehlungen geben, welche Medikamente für jeden GIB-Fall von Nutzen sein können.
1. El-Tawil A. Trends bei gastrointestinalen Blutungen und Mortalität: Wo stehen wir? World J Gastroenterol. 2012;18(11):1154-1158.
2. Zhao Y, Encinosa W. Hospitalizations for gastrointestinal bleeding in 1998 and 2006. Statistical Brief #65. Healthcare Cost and Utilization Project (HCUP) Statistical Briefs. Dezember 2008.
3. Whelan CT, Chen C, Kaboli P, et al. Obere versus untere gastrointestinale Blutungen: ein direkter Vergleich der klinischen Präsentation, der Ergebnisse und des Ressourcenverbrauchs. J Hosp Med. 2010;5(3):141-147.
4. Wilcox CM, Cryer BL, Henk HJ, et al. Mortality associated with gastrointestinal bleeding events: comparing short-term clinical outcomes of patients hospitalized for upper GI bleeding and acute myocardial infarction in a US managed care setting. Clin Exp Gastroenterol. 2009;2:21-30.
5. Garcia Rodriguez LA, Ruigómez A, Hasselgren G, et al. Comparison of mortality from peptic ulcer bleed between patients with or without peptic ulcer antecedents. Epidemiologie. 1998;9(4):452-456.
6. Wilcox CM, Clark WS. Ursachen und Folgen von Blutungen im oberen und unteren Gastrointestinaltrakt: die Erfahrungen des Grady Hospital. South Med J. 1999;92:44-50.
7. Yavorski RT, Wong RK, Maydonovitch C, et al. Analysis of 3,294 cases of upper gastrointestinal bleeding in military medical facilities. Am J Gastroenterol. 1995;90:568-573.
8. Johanson JF. Eindämmung der Kosten von GI-Blutungen. Am J Gastroenterol. 1998;93:1384-1385.
9. Scottish Intercollegiate Guidelines Network (SIGN). Management von akuten oberen und unteren gastrointestinalen Blutungen. September 2008. www.sign.ac.uk/assets/sign105.pdf.
10. Kim, SK, Cho CD, Wojtowycz AR. Das Ligamentum Treitz (das Ligamentum suspensum des Duodenums): anatomische und röntgenologische Korrelation. Abdom Imaging. 2008;33:395-397.
11. Matthew B, et al. Diagnosis of gastrointestinal bleeding: a practical guide for clinicians. World J Gastrointest Pathophysiol. 2014;5(4):467-478.
12. Raju GS, et al. American Gastroenterological Association (AGA) Institute medical position statement on obscure gastrointestinal bleeding. Gastroenterology. 2007;133(5):1694-1696.
13. Tielleman T, Bujanda D, Cryer B, et al. Epidemiologie und Risikofaktoren für obere gastrointestinale Blutungen. Gastrointest Endosc Clin N Am. 2015;25(3):415-428.
14. Rodriguez-Hernandez H, Rodríguez-Morán M, González JL, et al. Risk factors associated with upper gastrointestinal bleeding and with mortality. Rev Med Inst Mex Seguro Soc. 2009;47(2):179-184.
15. Strate L. Lower GI bleeding: epidemiology and diagnosis. Gastroenterol Clin North Am. 2005;34(4):643-664.
16. Cocchi MN, Kimlin E, Walsh M, et al. Identifizierung und Wiederbelebung des Traumapatienten im Schock. Emerg Med Clin N Am. 2007;25:623-642.
17. Laine L, Jensen DM. Management von Patienten mit Ulkusblutungen. Am J Gastroenterol. 2012;107:345-360.
18. Siau K, Chapman W, Sharma N, et alManagement von akuten oberen gastrointestinalen Blutungen: ein Update für den Allgemeinarzt. J R Coll Physicians Edinb. 2017;47:218-230.
19. Rockall T, Logan R, Devlin H, et al. Risikobewertung nach akuter oberer gastrointestinaler Blutung. Gut. 1996;38:316-321.
20. Blatchford O, Murray W, Blatchford M. A risk score to predict need for treatment for upper gastrointestinal haemorrhage. Lancet. 2000;356:1318-1321.
21. Recio-Ramirez, JM, Sánchez-Sánchez Mdel P, Peña-Ojeda JA, et al. Die Vorhersagekraft des Glasgow-Blatchford-Scores für die Risikostratifizierung von Blutungen im oberen Gastrointestinaltrakt in einer Notaufnahme. Revista Española de Enfermedades Digestivas. 2015;107(5):262-267.
22. Strate L, Grainek IM. ACG Clinical Guideline: Management of Patients With Acute Lower Gastrointestinal Bleeding. Am J Gastroenterol. Advance online publication March 1, 2016. 2016;111:459-474.
23. Bessa X, O’Callaghan E, Balleste B, et al. Applicability of the Rockall score in patients undergoing endoscopic therapy for upper gastrointestinal bleeding. Dig Liver Dis. 2006;38:12-17.
24. Chaimoff C, Creter D, Djaldetti M. The effect of pH on platelet and coagulation factor activities. Am J Surg. 1978;136(2):257-259.
25. Sreedharan A, Martin J, Leontiadis GI, et al. Protonenpumpeninhibitor-Behandlung, die vor der endoskopischen Diagnose bei oberen gastrointestinalen Blutungen eingeleitet wird. Cochrane Database Syst Rev. 2010(7):CD005415.
26. Leontiadis GI , Sharma VK , Howden CW. Protonenpumpeninhibitor-Therapie bei Blutungen aus Magengeschwüren: Cochrane collaboration meta-analysis of randomized controlled trials. Mayo Clin Proc. 2007;82:286-296.
27. Sachar H, Vaidya K, Laine L, et al. Intermittierende vs. kontinuierliche Protonenpumpeninhibitor-Therapie bei blutenden Hochrisiko-Geschwüren: eine systematische Übersichtsarbeit und Meta-Analyse. JAMA Intern Med. 2014;174(11):1755-1762.
28. Cheng H, Sheu B. Intravenous proton pump inhibitors for peptic ulcer bleeding: clinical benefits and limits. World J Gastrointest Endosc. 2011;3(3):49-56.
29. Zhang YS, Li Q, He BS, et al. Protonenpumpeninhibitoren-Therapie vs. H2-Rezeptor-Antagonisten-Therapie für obere gastrointestinale Blutungen nach Endoskopie: eine Meta-Analyse. World J Gastroenterol. 2015;21(20):6341-6351.
30. Rahman R, Nguyen D, Sohail U, et al. Pre-endoscopic erythromycin administration in upper gastrointestinal bleeding: an updated meta-analysis and systematic review. Ann Gastroenterol. 2016,29:312-317.
31. Gralnek IM, Dumonceau JM, Kuipers EJ, et al. Diagnosis and management of nonvariceal upper gastrointestinal hemorrhage: Leitlinie der Europäischen Gesellschaft für Gastrointestinale Endoskopie (ESGE). Endoscopy. 2015;47:1-46.
32. Issa D, Solomon S, Di Pace B, et al. A Comparison of Azithromycin to Erythromycin Infusions in Improving Visualization of Endoscopy for Upper Gastrointestinal Bleeding. World Congress at ACG2017. Session 2A.
33. Chey WD, Wong BC. Practice Parameters Committee of the American College of Gastroenterology. American College of Gastroenterology guideline on the management of Helicobacter pylori infection. Am J Gastroenterol. 2007; 102:1808-1825.
34. Luée A, Lanas A. Protons pump inhibitor treatment and lower gastrointestinal bleeding: balancing risks and benefits. World J Gastroenterol. 2016;22(48):10477-10481.