US Pharm.2008;33(11):Epub.
Weibliche sexuelle Dysfunktion (FSD) ist eine weit verbreitete Störung, die die Lebensqualität von Frauen über die gesamte Lebensspanne und weltweit beeinträchtigt. In den Vereinigten Staaten leiden nach den Ergebnissen der National Health and Social Life Survey fast 43 % der Frauen unter 60 Jahren an einer Art sexueller Funktionsstörung.1 Es ist bekannt, dass Störungen der Sexualfunktion mit dem Alter und nach Einsetzen der Menopause zunehmen. Etwa 52,4 % der Frauen in der natürlichen Menopause – schätzungsweise 16 Millionen Frauen im Alter von 50 Jahren und älter – sind wahrscheinlich von geringem sexuellem Verlangen und den Symptomen von FSD betroffen.2 Zu den weiteren medizinischen Begleiterkrankungen, die eine Rolle spielen können, gehören Diabetes, Bluthochdruck, Herz-Kreislauf-Erkrankungen, Krebs, chirurgische Eingriffe (insbesondere Operationen am Beckenboden) und die Einnahme bestimmter Medikamente.3 Ein umfassendes Verständnis des Kontinuums der Erscheinungsformen von FSD ist unerlässlich, um die Funktionen der verschiedenen Behandlungsmöglichkeiten zu verstehen, die Apotheker Patienten mit dieser komplexen Erkrankung empfehlen können.
Klassifizierung weiblicher Sexualstörungen
Nach Angaben der American Foundation for Urologic Disease und der American Psychiatric Association können weibliche Sexualstörungen in vier große Kategorien eingeteilt werden: Störungen des verminderten Verlangens und der sexuellen Abneigung, der Erregung, des Orgasmus und der sexuellen Schmerzen, die zu persönlichem Leid führen.4,5 Anhaltende Abwesenheit von sexuellen Vorstellungen, Fantasien und Empfänglichkeit oder völlige Vermeidung sexueller Aktivitäten kennzeichnen die Störungen des verminderten Verlangens und der sexuellen Abneigung. Die Unfähigkeit, sexuelle Erregung zu erreichen oder aufrechtzuerhalten (Symptome wie verminderte oder fehlende vaginale Lubrikation, Empfindung und vaginale Muskelentspannung) sind mit Störungen der sexuellen Erregung verbunden. Wiederkehrende oder anhaltende Verzögerung des Orgasmus oder die Unfähigkeit, trotz ausreichender Stimulation einen Orgasmus zu erreichen, definieren Orgasmusstörungen. Dyspareunie (Schmerzen im Genitalbereich beim Geschlechtsverkehr) und Vaginismus (unwillkürliche Muskelkrämpfe in der Vagina, die die Penetration behindern) sind Kennzeichen von Störungen des sexuellen Schmerzes bei einigen Frauen. Wichtig ist, dass diese Erscheinungsformen von FSD auf verschiedene psychologische, physische und medizinische Ursachen zurückzuführen sind, die vor einer wirksamen Behandlung ermittelt werden müssen.
Ursachen von FSD
Die Ätiologie von FSD ist multifaktoriell. Der allgemeine körperliche und geistige Zustand, frühere sexuelle Erfahrungen, das Ausmaß an Stress, Bildung und Beschäftigung, der sozioökonomische Status, die kulturelle und ethnische Identität, die Beziehungsdynamik sowie das Vorhandensein und der Gesundheitszustand des Partners tragen alle zur sexuellen Identität einer Frau bei und bestimmen das übliche Sexualverhalten. Eine kurze Auflistung der Faktoren, die mit den verschiedenen Arten von FSD in Verbindung gebracht werden, findet sich in TABELLE 1.6,20
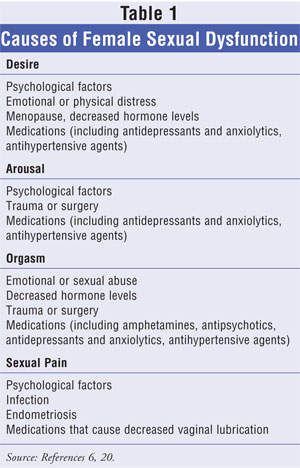
Psychologische Faktoren im Zusammenhang mit emotionalen oder Beziehungsproblemen, Depressionen und die Einnahme von Antidepressiva sowie ein geringes Selbstwertgefühl und eine schlechte Selbstwahrnehmung sind die häufigsten und oft am schwierigsten zu behandelnden Ursachen von FSD.6,7 Diese psychogenen Auslöser können mit jeder der Erscheinungsformen von FSD in Verbindung gebracht werden. Darüber hinaus können sich psychiatrische Erkrankungen und unerwünschte Wirkungen von Antipsychotika manchmal als Symptome von FSD manifestieren.
Der Körper einer Frau ist während ihres gesamten Lebens hormonellen Einflüssen und Ungleichgewichten ausgesetzt, die sich auf ihre Sexualphysiologie auswirken, insbesondere während der Schwangerschaft und der Menopause. Während die Schwangerschaft selbst im Allgemeinen mit einem verminderten Interesse an Sex in Verbindung gebracht wird, berichten 23 % bis 57 % der Frauen über eine verminderte Libido drei Monate nach der Geburt und fast 40 % über eine solche nach sechs Monaten.8,9 Frauen, die stillen, berichten häufig über eine erhöhte vaginale Trockenheit als Folge der verminderten Östrogenproduktion während dieser Zeit, und Dyspareunie kann mit dem natürlichen Geburtsvorgang selbst in Verbindung gebracht werden.10 Wenn der Körper einer Frau in die Wechseljahre kommt, geht die Einstellung der Östrogenproduktion in den Eierstöcken mit einer urogenitalen Atrophie und einer verminderten sexuellen Reaktion einher.11 Diese körperlichen Veränderungen werden häufig von vasomotorischen Symptomen, Stimmungsschwankungen, emotionaler Labilität und einem verminderten Wohlbefinden begleitet, die sich negativ auf die sexuelle Funktion und die Lebensqualität auswirken.12
Gefäßerkrankungen wie Diabetes, Bluthochdruck, Hyperlipidämie, Nierenerkrankungen, Atherosklerose und traumatische Verletzungen werden mit einer verminderten vaginalen und klitoralen Durchblutung und einer Beeinträchtigung der sexuellen Funktion in Verbindung gebracht.13,14 Rauchen wird sowohl bei Männern als auch bei Frauen mit einer verminderten genitalen Durchblutung in Verbindung gebracht.15 Sexuelle Funktionsstörungen sind eine häufige Erscheinung bei Frauen, die an urologischen Infektionen und Erkrankungen wie interstitieller Zystitis, Harninkontinenz, Blasenentleerungsstörungen, sexuell übertragbaren Krankheiten und entzündlichen Beckenerkrankungen leiden.16 Physiologische Störungen der Vagina und der Gebärmutter wie Vaginalfissuren und Endometriose werden mit sexuellen Schmerzstörungen in Verbindung gebracht.17 Beckenchirurgie, Erkrankungen des zentralen Nervensystems und Rückenmarksverletzungen verursachen autonome Nervenfunktionsstörungen und wurden mit Erregungs- und Orgasmusstörungen in Verbindung gebracht.18,19
Zahlreiche Medikamente wurden als Auslöser sexueller Funktionsstörungen ermittelt. Einige der häufigsten Wirkstoffe sind in TABELLE 2 aufgeführt.20 Informationen von Patientinnen, die sexuelle Nebenwirkungen im Zusammenhang mit Medikamenten erfahren, sind spärlich und beruhen oft auf Fallberichten und anekdotischer Evidenz. Darüber hinaus können die zugrundeliegende Krankheitsmanifestation und das Fortschreiten der Krankheit nicht von einer unerwünschten Folge der Arzneimitteltherapie unterschieden werden, wie dies bei blutdrucksenkenden Mitteln und koronaren Herzkrankheiten der Fall ist.

Nicht-pharmakologische Interventionen
Zurzeit gibt es keine Behandlungsrichtlinien oder Konsenserklärungen, die die Behandlung von Frauen mit FSD vorschreiben. Aufgrund der Vielfalt der ursächlichen Faktoren, die mit den Symptomen von FSD in Verbindung gebracht werden, sind die Änderung des Lebensstils, die Behebung physischer und psychischer Ursachen und die Änderung von Verhaltensgewohnheiten im Zusammenhang mit dem Geschlechtsverkehr die bevorzugten ersten Schritte bei der Behandlung von FSD, die bei angemessener Behandlung zu einer Umkehr der Symptome führen können. Der Verzicht auf Rauchen und Alkohol, eine veränderte Ernährung, die Anwendung stressreduzierender Techniken, regelmäßige körperliche Bewegung und die Behandlung von Krankheiten wie Diabetes und Bluthochdruck, die Frauen für FSD prädisponieren können, sind wesentliche Änderungen der Lebensweise, die Berichten zufolge die sexuelle Funktionsfähigkeit der Frau verbessern.21,22 Die Identifizierung und das Absetzen von Medikamenten, die mit symptomatischen Beschwerden in Zusammenhang stehen, kann gerechtfertigt sein, wenn therapeutische Alternativen bestehen. Je nach Ursache und Symptomen der sexuellen Funktionsstörung einer Frau können physische Modifikationen im Zusammenhang mit dem Geschlechtsverkehr – einschließlich der Verwendung von Vibratoren oder elektrischen Stimulationsgeräten, Gleitmitteln, Übungen zur Stärkung des Beckenbodens und Variation der Sexualposition – dazu beitragen, die Zufriedenheit zu steigern.23,24 Frauen mit physiologischen Erregungsstörungen, die durch eine unzureichende Durchblutung der Genitalien verursacht werden, berichteten über signifikante Verbesserungen der Erregung, des Empfindens, des Orgasmus und des allgemeinen sexuellen Vergnügens, wenn sie das Eros Clitoral Therapy Device, ein nicht-pharmakologisches Vakuumgerät zur Stimulation der Klitoris, verwendeten.25,26 Psychotherapie und Beratung durch einen Sexualtherapeuten sind besonders wichtig für Frauen, deren Funktionsstörungen auf Beziehungskonflikte, frühere sexuelle Erfahrungen, emotionale Probleme, Angst oder Depressionen zurückzuführen sind.27 In einer klinischen Studie zur Bewertung der Wirksamkeit eines kognitiv-behavioralen Modifikationsprogramms bei FSD-Patientinnen berichteten die Frauen über eine verbesserte Einstellung, empfanden ein größeres sexuelles Vergnügen und gaben nach der Therapie seltener sexuelle Funktionsstörungen an.28 Aufgrund der vielfältigen, komplexen und häufig koexistierenden Faktoren, die mit den Symptomen der sexuellen Dysfunktion bei Frauen in Verbindung stehen, werden nicht-pharmakologische und pharmakologische Maßnahmen häufig kombiniert, um den Therapieerfolg zu optimieren.
Pharmakologische Interventionen
Historisch gesehen waren Frauen mit FSD darauf beschränkt, sich auf eine Hormonersatztherapie und vaginale Gleitmittel zu verlassen, um die sexuelle Funktionalität zu verbessern. In jüngerer Zeit wurden Medikamente, die erfolgreich zur Behandlung der erektilen Dysfunktion bei Männern eingesetzt werden, einschließlich Sildenafil und Alprostadil, auch bei Frauen untersucht.29,30 Die klinische Wirksamkeit dieser Mittel ist im Allgemeinen gering, obwohl sie manchmal off-label eingesetzt werden. Bis vor kurzem gab es keine von der FDA zugelassenen Medikamente für die Behandlung sexueller Funktionsstörungen bei Frauen. Im April 2007 erweiterte die FDA die Indikationen für synthetische konjugierte Östrogene, B(Enjuvia), um die Behandlung von mittelschwerer bis schwerer vaginaler Trockenheit, Dyspareunie sowie vulvärer und vaginaler Atrophie im Zusammenhang mit der Menopause.31 Neuere Wirkstoffe, die auf die Neurotransmitter Dopamin, Serotonin und Melanocortin – das Neuropeptid, das für die physiologische sexuelle Reaktion bei Männern und Frauen verantwortlich ist – abzielen, werden derzeit in klinischen Studien untersucht.32 Ein Vergleich der Wirkstoffe, die zur Behandlung der verschiedenen Störungen der FSD eingesetzt werden, ist in TABELLE 3 dargestellt.
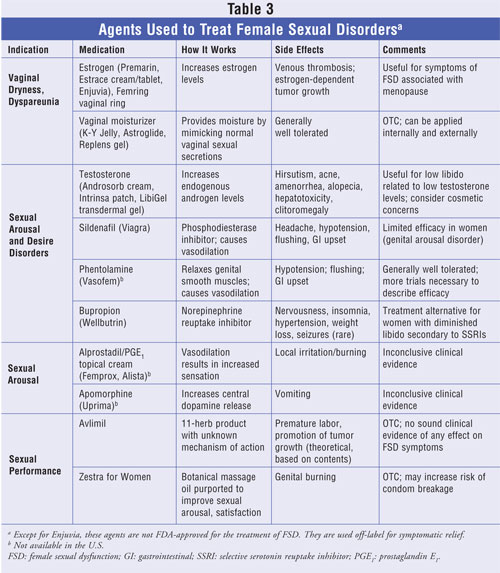
Hormonelle Ergänzungstherapien mit Östrogen oder Testosteron wurden eingesetzt, um die verminderten Spiegel aufzufüllen, von denen man annimmt, dass sie mit sexuellen Funktionsstörungen verbunden sind, insbesondere bei Frauen in der Perimenopause und nach der Menopause.33 Die Östrogenersatztherapie (ERT) wird mit signifikanten Verbesserungen des sexuellen Verlangens, des Orgasmus, der Dyspareunie-Symptome und der vaginalen Trockenheit in Verbindung gebracht. Neben der Verbesserung der vaginalen Symptome werden auch vasomotorische Symptome, einschließlich Hitzewallungen, durch diese Therapieform gelindert.34,35 Trotz ihrer gut beschriebenen Wirksamkeit ist die ERT im Allgemeinen nicht für Frauen indiziert, deren Symptome nicht mit vaginalen oder vasomotorischen Funktionsstörungen zusammenhängen. Die mit der ERT verbundenen Risiken, einschließlich venöser Thrombosen, sind allgemein bekannt. Da der Androgenspiegel mit dem Alter ebenfalls abnimmt, können Frauen, die über ein vermindertes sexuelles Verlangen und eine geringere sexuelle Befriedigung berichten – Symptome, die mit Testosteronmangel oder niedrigen Serumtestosteronspiegeln zusammenhängen -, von einer Testosteronersatztherapie profitieren, obwohl neuere Erkenntnisse darauf hindeuten, dass es keine Beweise dafür gibt, dass niedrige Serumtestosteronspiegel tatsächlich mit sexuellen Funktionsstörungen verbunden sind.36-38 Die Daten zur langfristigen Wirksamkeit und Sicherheit der Testosteronersatztherapie sind nicht bekannt. Östrogen-Testosteron-Kombinationsprodukte, einschließlich veresterter Östrogene und Methyltestosteron (Estratest; Estratest HS), wurden ebenfalls eingesetzt und sind für Wechseljahresbeschwerden zugelassen, die durch eine Östrogenergänzung allein nicht behoben werden können; sie können auch außerhalb der Zulassung für bestimmte Störungen der sexuellen Funktionsfähigkeit eingesetzt werden.
Vasoaktive Medikamente, insbesondere Phosphodiesterase-Hemmer, haben im Bereich der männlichen sexuellen Dysfunktion viel Aufmerksamkeit erregt. Bei Frauen wirkt Sildenafil durch eine Verringerung des zyklischen Guanosinmonophosphat-Stoffwechsels, was zu einer Stickoxid-vermittelten Vasodilatation und Entspannung der glatten Vaginalmuskulatur und der Klitoris führt. Die Daten aus klinischen Studien mit prä- und postmenopausalen Frauen sind widersprüchlich, wobei jüngere Frauen eine Verbesserung der Erregung, des Orgasmus, der sexuellen Fantasie und der Aktivität und ältere Frauen eine minimale, nicht signifikante Verbesserung der Zufriedenheit und der allgemeinen sexuellen Funktion erfahren.39,40 Phentolamin, ein alpha-adrenerger Rezeptorantagonist mit gefäßerweiternden Eigenschaften, erhöht Berichten zufolge die Erregung und verbessert die vaginale Lubrikation.41,42 Orale Tabletten und topische Lösungen sind in den USA nicht erhältlich.
Für Frauen, deren sexuelle Dysfunktion mit der Einnahme von Antidepressiva zusammenhängt, kann die Umstellung auf Bupropion – ein Wirkstoff, der seine Wirkung durch die Blockierung der Wiederaufnahme von Noradrenalin und Dopamin entfaltet – Linderung verschaffen. Bupropion wurde bei der Behandlung von durch selektive Serotonin-Wiederaufnahmehemmer verursachten sexuellen Funktionsstörungen untersucht und wurde mit einer statistisch signifikanten Verbesserung der Erregung und der sexuellen Zufriedenheit in Verbindung gebracht.43,44 Apomorphin, ein kurz wirksamer, nicht selektiver Dopaminagonist, wurde als Sublingualtablette zur Behandlung von FSD untersucht. Der Wirkstoff wurde in einer kleinen klinischen Studie mit einer Verbesserung des klitoralen Blutflusses, der Erregung, der Lubrikation und des Orgasmus in Verbindung gebracht; sein Nutzen ist jedoch durch dosisbegrenzende Übelkeit, Erbrechen und Schwindel eingeschränkt.45,46
Alprostadil, ein Prostaglandin-Analogon, das in injizierbarer Form zur Verwendung bei Männern mit Erektionsstörungen erhältlich ist, wurde als topische Genitalcreme zur Behandlung sexueller Erregungsstörungen bei Frauen untersucht. Trotz gemischter klinischer Studienergebnisse wird der Wirkstoff im Allgemeinen gut vertragen. Es wird mit vorübergehenden lokalen Reizungen in Verbindung gebracht.30
Schlussfolgerung
Sexuelle Dysfunktion betrifft Millionen von Frauen in den USA und weltweit. Apotheker können dazu beitragen, eine funktionierende Beziehung zu weiblichen Patienten aufzubauen, die unter dieser Störung leiden, indem sie eine Kommunikation eröffnen, die für sie möglicherweise schwierig ist. Apotheker können auch eine wichtige Rolle bei der Aufklärung von Patientinnen über nicht-pharmakologische und pharmakologische Interventionen bei FSD spielen.
1. Laumann EO, Paik A, Rosen RC. Sexuelle Dysfunktion in den Vereinigten Staaten: Prävalenz und Prädiktoren. JAMA. 1999;281:537-544.
2. West SL, D’Aloisio AA, Agans RP, et al. Prävalenz von geringem sexuellem Verlangen und hypoaktivem sexuellen Verlangen in einer national repräsentativen Stichprobe von US-Frauen. Arch Intern Med. 2008;168:1441-1449.
3. Modelska K, Milian ML. Behandlung der weiblichen sexuellen Dysfunktion bei postmenopausalen Frauen – was ist die Beweislage? Rev Gynaecological Pract. 2004;4:121-131.
6. Berman JR, Berman L, Goldstein I. Weibliche sexuelle Dysfunktion: Häufigkeit, Pathophysiologie, Bewertung und Behandlungsmöglichkeiten. Urology. 1999;54:385-391.
7. Basson R. Sexuelles Verlangen und Erregungsstörungen bei Frauen. N Engl J Med. 2006;354:1497-1506.
8. Barrett G, Pendry E, Peacock J, et al. Die Sexualität von Frauen nach der Geburt: eine Pilotstudie. Arch Sex Behav. 1999;28:179-191.
9. Robson KM, Brant HA, Kumar R. Maternal sexuality during first pregnancy and after childbirth. Br J Obstet Gynaecol. 1981;88:882-889.
10. Barrett G, Pendry E, Peacock J, et al. Women’s sexual health after childbirth. Br J Obstet Gynaecol. 2000;107:186-195.
11. Goldstein I, Traish A, Kim N, Munarriz R. The role of sex steroid hormones in female sexual function and dysfunction. Clin Obstet Gynecol. 2004;47:471-484.
12. Cawood EH, Bancroft J. Steroidhormone, die Wechseljahre, Sexualität und Wohlbefinden von Frauen. Psychol Med.1996;26:925-936.
13. Palmer BF. Sexuelle Dysfunktion bei Männern und Frauen mit chronischer Nierenerkrankung und Nierenerkrankung im Endstadium. Adv Ren Replace Ther. 2003;10:48-60.
14. Brassil DF, Keller M. Weibliche sexuelle Dysfunktion: Definitionen, Ursachen und Behandlung. Urol Nurs. 2002;22:237-244,284.
15. Harte CB, Meston CM. Die hemmende Wirkung von Nikotin auf die physiologische sexuelle Erregung bei nicht rauchenden Frauen: Ergebnisse einer randomisierten, doppelblinden, placebokontrollierten Cross-over-Studie. J Sex Med.2008;5:1184-1197.
16. Bump RC, Norton PA. Epidemiologie und natürlicher Verlauf der Beckenbodendysfunktion. Obstet Gynecol Clin North Am. 1998;25:723-746.
17. Heim LJ. Bewertung und Differentialdiagnose der Dyspareunie. Am Fam Physician. 2001;63:1535-1544.
18. Zippe CD, Nandipati KC, Agarwal A, Raina R. Female sexual dysfunction after pelvic surgery: the impact of surgical modifications. BJU Int. 2005;96:959-963.
19. Sipski ML, Alexander CJ, Rosen RC. Sexuelle Reaktionen bei Frauen mit Rückenmarksverletzungen: Implikationen für unser Verständnis der Nichtbehinderten. J Sex Marital Ther. 1999;25:11-22.
20. Medikamente, die sexuelle Dysfunktion verursachen: ein Update. Med Lett Drugs Ther. 1992;34:73-78.
21. Perkins BA, Greene DA, Bril V. Glycemic control is related to the morphological severity of diabetic sensorimotor polyneuropathy. Diabetes Care. 2001;24:748-752.
22. Pauls RN, Kleeman SD, Karram MM. Weibliche sexuelle Dysfunktion: Prinzipien der Diagnose und Therapie. Obstet Gynecol Surv. 2005;60:196-205.
23. Feldman J, Striepe M. Women’s sexual health. Clin Fam Pract. 2004;6:839-861.
24. Beji NK, Yalcin O, Erkan HA. Die Wirkung des Beckenbodentrainings auf die sexuelle Funktion der behandelten Patienten. Int Urogynecol J Pelvic Floor Dysfunct. 2003;14:234-238.
25. Wilson SK, Delk JR, Billups KL. Die Behandlung von Symptomen der weiblichen sexuellen Erregungsstörung mit dem Eros-Clitoral Therapy Device. J Gend Specif Med. 2001;4:54-58.
26. Billups KL, Berman L, Berman J, et al. A new non-pharmacological vacuum therapy for female sexual dysfunction. J Sex Marital Ther. 2001;27:435-441.
27. Heiman JR. Psychologische Behandlungen für weibliche sexuelle Dysfunktion: sind sie wirksam und brauchen wir sie? Arch Sex Behav. 2002;31:445-450.
28. McCabe MP. Evaluierung eines kognitiven Verhaltenstherapieprogramms für Menschen mit sexueller Dysfunktion. J Sex Marital Ther. 2001;27:259-271.
29. Basson R, McInnes R, Smith MD, et al. Efficacy and safety of sildenafil citrate in women with sexual dysfunction associated with female sexual arousal disorder. J Womens Health Gend Based Med. 2002;11:367-377.
30. Kielbasa LA, Daniel KL. Topische Alprostadil-Behandlung der weiblichen sexuellen Erregungsstörung. Ann Pharmacother. 2006;40:1369.
31. Enjuvia (synthetische konjugierte Östrogene, B) Packungsbeilage. Pomona, NY: Duramed Pharmaceuticals, Inc; April 2007.
32. Brown AD, Blagg J, Reynolds DS. Designing drugs for the treatment of female sexual dysfunction. Drug Discov Today. 2007;12:757-766.
33. Cardozo L, Bachmann G, McClish D, et al. Meta-Analyse der Östrogentherapie bei der Behandlung der urogenitalen Atrophie bei postmenopausalen Frauen: zweiter Bericht des Hormones and Urogenital Therapy Committee. Obstet Gynecol. 1998;92:722-727.
34. Sarrel PM. Sexualität und Menopause. Obstet Gynecol. 1990;75(suppl 4):26S-30S.
35. Myers LS, Dixen J, Morrissette D, et al. Effects of estrogen, androgen, and progestin on sexual psychophysiology and behavior in postmenopausal women. J Clin Endocrinol Metab. 1990;70:1124-1131.
36. Shifren JL, Braunstein GD, Simon JA, et al. Transdermale Testosteronbehandlung bei Frauen mit eingeschränkter Sexualfunktion nach Oophorektomie. N Engl J Med. 2000;343:682-688.
37. Braunstein GD, Sundwall DA, Katz M, et al. Sicherheit und Wirksamkeit eines Testosteronpflasters zur Behandlung des hypoaktiven sexuellen Verlangens: eine randomisierte, placebokontrollierte Studie. Arch Intern Med. 2005;165:1582-1589.
38. Davis SR, Davison SL, Donath S, Bell RJ. Zirkulierende Androgenspiegel und selbstberichtete sexuelle Funktion bei Frauen. JAMA. 2005;294:91-96.
39. Caruso S, Intelisano G, Lupo L, Agnello C. Prämenopausale Frauen mit sexueller Erregungsstörung, behandelt mit Sildenafil: eine doppelblinde, cross-over, placebokontrollierte Studie. Br J Obstet Gynaecol. 2001;108:623-628.
40. Kaplan SA, Reis RB, Kohn IJ, et al. Safety and efficacy of sildenafil in postmenopausal women with sexual dysfunction. Urology. 1999;53:481-486.
41. Rosen RC, Phillips NA, Gendrano NC, Ferguson DM. Orales Phentolamin und weibliche sexuelle Erregungsstörung: eine Pilotstudie. J Sex Marital Ther. 1999;25:137-144.
42. Rubio-Aurioles E, Lopez M, Lipezker M, et al. Phentolamin-Mesylat bei postmenopausalen Frauen mit weiblicher sexueller Erregungsstörung: eine psychophysiologische Studie. J Sex Marital Ther. 2002;28(suppl 1):205-215.
43. Clayton AH, Warnock JK, Kornstein SG, et al. A placebo-controlled trial of bupropion SR as an antidote for selective serotonin reuptake inhibitor-induced sexual dysfunction. J Clin Psychiatry. 2004;65:62-67.
44. Segraves RT, Clayton A, Croft H, et al. Bupropion sustained release for the treatment of hypoactive sexual desire disorders in premenopausal women. J Clin Psychopharmacol. 2004;24:339-342.
45. Bechara A, Bertolino MV, Casabé A, Fredotovich N. A double-blind randomized placebo controlled study comparing the objective and subjective changes in female sexual response using sublingual apomorphine. J Sex Med. 2004;1:209-214.
46. Montorsi F. Verträglichkeit und Sicherheit von Apomorphin SL. Int J Impot Res. 2003;15(suppl 2):S7-S9.
Für Kommentare zu diesem Artikel wenden Sie sich bitte an [email protected].