Nøgleord
Irritabel tarmsyndrom; Sertralin; Psykosomatisk
Introduktion
En af de mest almindelige funktionelle gastrointestinale lidelser er irritabel tarmsyndrom (IBS), da dens globale prævalens er omkring 5-20%, afhængigt af Rom III-kriterier. Det er mere almindeligt hos yngre personer, især hos kvinder . Patienter med IBS er mere tilbøjelige til at have sygdomsrelateret fravær end patienter uden tarmsymptomer . I en nyere undersøgelse af byrden af IBS i USA blev det anslået, at de direkte omkostninger er næsten 1 mia. dollars og de indirekte omkostninger er på yderligere 50 mio. dollars . Desuden er forbruget af sundhedsressourcer hos patienter med IBS ca. >50 % . Derfor er en effektiv behandling af IBS afgørende, hvad enten det er for den enkelte eller for sundhedssystemerne og hele samfundet.
Den nøjagtige årsag til IBS er fortsat ukendt, hvilket betyder, at der ikke findes nogen samlet forklaring på tarmsymptomerne, som en behandling kan målrettes mod. Patienter med IBS viser unormal central behandling af smerte , visceral overfølsomhed , og højere niveauer af psykologisk comorbiditet sammenlignet med raske kontroller uden tarmsymptomer . Som følge heraf er antidepressiva blevet introduceret som behandlinger for IBS, da de har smertemodificerende egenskaber . Serotonin (5-HT) spiller via 5-HT3- og 5-HT4-receptorerne en afgørende rolle i kontrollen af gastrointestinal motilitet, sekretion og følelse. Desuden har nylige observationer vist, at plasma 5-HT-koncentrationerne er reduceret hos IBS-patienter .
Flere undersøgelser har vist, at IBS-patienter har unormal personlighed samt højere score for angst og depression . Mange undersøgelser har imidlertid evalueret antidepressiva effektivitet på IBS; deres kliniske beviser er stadig kontroversielle. De mest almindeligt anvendte antidepressiva er selektive serotonin-genoptagelseshæmmere (SSRI) såsom fluoxetin og citalopram og tricykliske antidepressiva (TCA) såsom imipramin og amitriptylin.
Som selektiv serotonin-genoptagelseshæmmer virker sertralin ved at blokere genoptagelsen af serotonin i CNS synaptiske kløfter og øger således serotoninniveauet i hjernen, hvilket er forbundet med dets psykiatriske virkninger. Sertralin blev godkendt til brug i USA i 1991, og det er fortsat meget anvendt med næsten 40 millioner recepter, der udfyldes årligt. Det er velkendt til behandling af depression og angstlidelser. Det betragtes også som en af selektive serotonin genoptagelseshæmmere, der har en smerteregulerende mekanisme, så det bruges også ofte ved psykosomatiske lidelser .
Denne undersøgelse sammenlignede effektiviteten af sertralin med placeboeffekt (konventionel behandling som antispasmodiske og antidiarrhoiske lægemidler) med hensyn til deres virkning på tarmsymptomer ved irritabel tyktarm samt angst og depressive symptomer i forbindelse med.
Metoder
Denne undersøgelse var et prospektivt sertralin, placebo randomiseret klinisk forsøg af 1 måneds varighed med enkeltblind behandling og blindede resultatmålinger. Den bestod af 55 patienter, der for nylig blev diagnosticeret som irritabel tarmsyndrom (IBS) i henhold til Rom III-kriterierne, som blev rekrutteret inden for 4 uger fra ambulatorier på Assiut Universitetshospitaler.
Samplestørrelse
I case-kontrolundersøgelser om IBS observeres der ofte et 50% respons på placebo. Desuden er der observeret responsrater på antidepressiva på op til 89 % i åbne undersøgelser. Ved hjælp af disse tal og med en power på 80 % blev der opnået en stikprøvestørrelse på for hver gruppe.
Subjekter og undersøgelsesdesign
De var i aldersgruppen mellem 18-40 år. Vi inkluderede kun patienter, der for nylig blev diagnosticeret som IBS, og sygdomsvarigheden var ikke mere end 5 år. Desuden blev alle patienterne ikke tidligere behandlet med andre selektive serotonin-genoptagelseshæmmere. Alle rutineundersøgelser blev foretaget for alle patienterne, herunder komplet blodtælling, nyre- og leverfunktion samt måling af elektrolytterne. Hamilton rating scale for anxiety (HAM-A) og Hamilton rating scale for depression (HAM-D) blev udført for alle patienter ved baseline før behandlingsstart. Patienterne blev inddelt i to grupper, første gruppe, som var 30 patienter, der fik sertralin 50 mg, og anden gruppe, som var 25 patienter, der fik placebo. Blinding var skjult i hele det randomiserede kliniske forsøg. Patienterne blev fulgt op i en måned efter behandlingen. Der blev foretaget en revurdering af patienterne med hensyn til deres tarmmanifestationer. Forbedring af tarmmanifestationen blev betragtet som en forbedring, når der var tilstrækkelig lindring af symptomer rapporteret af patienterne efter 4 ugers behandling med et lægemiddel. Desuden blev Hamilton rating scale for anxiety (HAM-A) og Hamilton rating scale for depression (HAM-D) foretaget for alle patienterne en måned efter behandlingen.
Udelukkelseskriterier
1. Patienter, der havde tarmsymptomer, men som ikke opfyldte Rom III-kriterierne for diagnosen irritabel tyktarm.
2. Patienter, der havde irritabel tyktarm i mere end 5 års varighed.
3. Patienter, der har svær angst og/eller depression i henhold til henholdsvis HAM-A og HAM-D.
4. Patienter, der ikke opfyldte aldersgruppen.
5. Patienter, der modtog anden medicin.
6. Patienter, der havde kroniske medicinske tilstande.
Dataanalyse
Den SPSS version 16-pakke blev anvendt i denne undersøgelse. Der blev anvendt beskrivende statistik til at sammenligne effekten af sertralin og placebo på tarmmanifestationer. Parrede prøver T-test blev anvendt til at sammenligne effekten af sertralin og placebo på henholdsvis Hamilton rating scale for anxiety (HAM-A) og Hamilton rating scale for depression (HAM-D).
Resultater
Denne undersøgelse bestod af 55 patienter med irritabel tyktarm, som blev diagnosticeret i henhold til Rom III-kriterierne. Med hensyn til patienternes demografiske data var patienternes gennemsnitsalder 26 ± 2,1 år, og forholdet mellem kvinder og mænd var 1,7/1, da der var 32 kvindelige patienter mod 18 mandlige patienter.
Den mest almindelige GIT-manifestation var abdominal ubehag, som fandtes hos alle patienter (100 %), efterfulgt af abdominal oppustethed og distension, som fandtes hos 36 patienter (65,45 %). Den tredje almindelige manifestation var forbedring af symptomerne ved afføring, som fandtes hos 32 patienter (58,18 %), og endelig var de mindst almindelige symptomer skiftende afføringsvaner, som fandtes hos 29 patienter (52,7 %). Patienter med IBS-C var mere tilbøjelige til at opleve abdominal oppustethed og forbedring af symptomerne ved afføring, mens patienter med IBS-D var mere tilbøjelige til at opleve vekslende tarmvaner (figur 1).
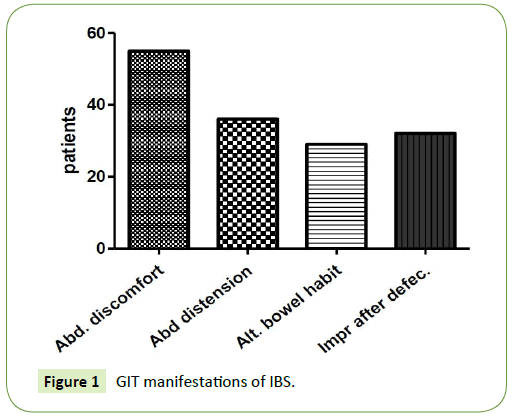
Figur 1: GIT manifestationer af IBS.
Patienterne blev inddelt i to grupper. 30 patienter fik sertralin 50 mg og 25 patienter fik placebo. 20 patienter, der fik sertralin 50 mg, viste en forbedring af deres tarmsymptomer (7 patienter havde irritabel tyktarm med fremherskende diarré og 13 patienter havde irritabel tyktarm med fremherskende forstoppelse), mens 10 patienter (4 patienter havde irritabel tyktarm med fremherskende diarré og 6 patienter havde irritabel tyktarm med fremherskende forstoppelse) ikke viste nogen tilfredsstillende forbedring af deres tarmsymptomer.
På den anden side viste 8 patienter, der fik placebo, en forbedring af deres tarmsymptomer (5 patienter havde irritabel tyktarm med fremherskende diarré og 3 patienter havde irritabel tyktarm med fremherskende forstoppelse), mens 17 patienter (12 patienter havde irritabel tyktarm med fremherskende diarré og 5 patienter havde irritabel tyktarm med fremherskende forstoppelse) ikke viste nogen forbedring af deres tarmsymptomer (tabel 1 og figur 2).
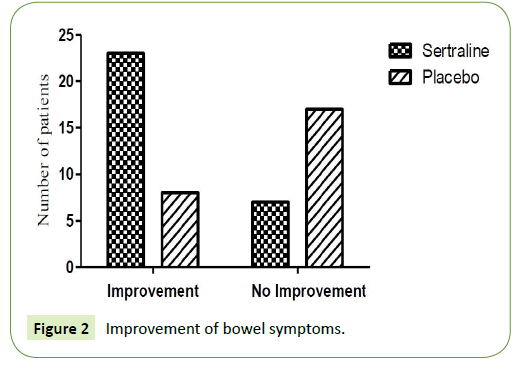
Figur 2: Forbedring af tarmsymptomer.
Note: IBS-D: irritabel tarmsyndrom med fremherskende diarré, IBS-C: irritabel tarmsyndrom med fremherskende forstoppelse
Tabel 1:Antal patienter viste forbedring af tarmsymptomer efter en måneds medicinering.
De to undersøgelsesgrupper blev sammenlignet med hensyn til Hamilton rating scale for henholdsvis angst og depression. Der var en signifikant reduktion i Hamilton rating scale for angst (HAM-A) og Hamilton rating scale for depression (HAM-D) efter en måned i den patientgruppe, der blev behandlet med sertralin 50 mg. Som gennemsnit var HAM-A 18,8 ± 3,9 før behandlingen og nåede 11,67 ± 1,9 efter en måneds behandling med sertralin. Endvidere var middelværdien af HAM-D 15,67 ± 3,9 før behandlingen og nåede 11,6 ± 4,2 efter en måneds behandling med sertralin (P=0,001). Derimod var der ingen signifikant reduktion i Hamilton rating scale for anxiety (HAM-A) og Hamilton rating scale for depression (HAM-D) efter en måned i den patientgruppe, der blev behandlet med placebo. Som gennemsnit var HAM-A 18,5 ± 2,6 før behandlingen og nåede 18,2 ± 2,4 efter en måneds behandling med placebo (P=0,12) (tabel 2). Desuden var gennemsnitlig HAM-D 13,4 ± 2,1 før behandlingen og nåede 13 ± 1,7 efter en måneds behandling med placebo (P=0,15) (figur 3 og 4) (P=0,15).
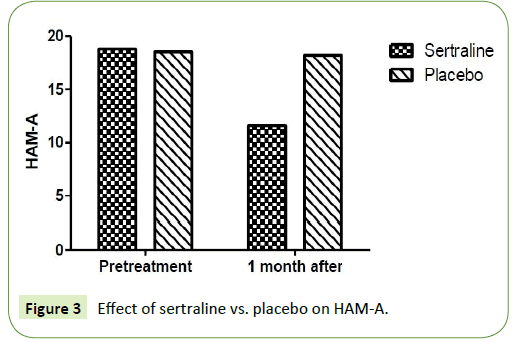
Figur 3: Effekt af sertralin vs. placebo på HAM-A.

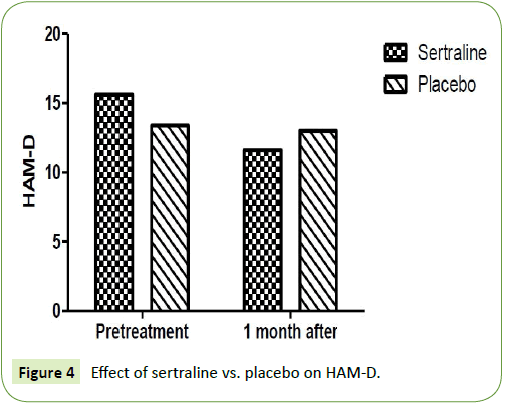
Figur 4: Effekt af sertralin vs. placebo på HAM-A.

Figur 4: Effekt af sertralin vs. placebo på HAM-D.
Tabel 2: Effekten af sertralin Vs placebo på HAM-A og HAM-D.
Diskussion
I litteraturen diskuterede seks studier effekten af selektive serotonin genoptagelseshæmmere (SSRI) i behandling af IBS med modstridende resultater. Fire undersøgelser af paroxetin , fluoxetin og citalopram rapporterede en beskeden fordel, mens to undersøgelser af fluoxetin og citalopram ikke gjorde det.
En metaanalyse af disse undersøgelser fandt en relativ risiko for uforbedrede symptomer på irritabel tarmsyndrom (IBS) er 0,62 (95% CI, 0,45 til 0,87) for SSRI’er vs. placebo, med betydelig heterogenitet mellem disse undersøgelser . Metaanalysen analyserede data fra 113 personer behandlet med SSRI og 117 kontroller.
Differencerne i resultaterne mellem disse seks forsøg kan tilskrives forskellene i undersøgelsesdesign samt patienternes population. Kuiken et al. rekrutterede 40 IBS-patienter af alle undertyper fra et tertiært center til en 6-ugers undersøgelse af fluoxetin eller placebo, patienter med depression blev udelukket i denne undersøgelse . Tabas et al. randomiserede 81 patienter med IBS af alle undertyper til en 12-ugers undersøgelse af en fiberrig kost med paroxetin eller placebo, patienter med depression blev ikke udelukket i denne undersøgelse . Vahedi et al. randomiserede 44 patienter med IBS med fremherskende forstoppelse til fluoxetin eller placebo i et 12 ugers studie, men kun patienter med svær depression blev ekskluderet . Tack et al. indskrev 23 IBS-patienter fra et tertiært behandlingscenter til et crossover-studie, der sammenlignede citalopram vs. placebo, patienter med depression blev udelukket i denne undersøgelse .
Ladabaum et al. randomiserede 27 patienter med IBS, der fik citalopram 20 mg/dag i 4 uger og derefter citalopram 40 mg/dag i yderligere 4 uger, men psykiatriske symptomer blev ikke vurderet for disse patienter .
Talley et al. randomiserede 51 patienter med IBS af alle typer til citalopram (17 forsøgspersoner), imipramin eller placebo (16 forsøgspersoner) i 12 uger, de udelukkede også patienter med depression fra dette forsøg .
Kendetegn ved de forsøg, hvor der blev påvist en vis fordel, omfatter manglende udelukkelse for depression , inklusion af kun forstoppelsesprædominante IBS-patienter , og et crossover-design med patienter fra tertiær pleje .
Det specifikke lægemiddel, dosis og varighed anvendt i hvert forsøg kunne være vigtige faktorer, men der tegner sig ikke noget klart mønster. Undersøgelsen af Tack et al. er den eneste, der viste fordel for citalopram , mens undersøgelsen af Talley et al. rapporterede identiske responsrater for citalopram og placebo , og Ladabaum et al. fandt beviser mod enhver væsentlig fordel af citalopram ved behandling af tarmsymptomer ved IBS . Forsøgene anvendte forskellige definitioner af klinisk respons, og dette kan forklare en stor del af konflikten i konklusionerne.
Nogle af dem anvendte tilstrækkelig lindring af IBS-symptomer som det primære resultat som Talley et al. I modsætning hertil vurderede de andre forsøg det globale symptomrespons, det generelle velbefindende eller effekten på specifikke symptomer.
Vores undersøgelse er det første forsøg, der diskuterede effekten af sertralin ved behandling af IBS. Vi fandt, at sertralin har en signifikant effekt på tarmsymptomerne ved irritabel tarmsyndrom (IBS) sammenlignet med placebo. Forbedringen af sertralin var ca. 66,67 % sammenlignet med placebo, som var 32 %. Vores undersøgelse viste, at effekten af sertralin på IBS med fremherskende forstoppelse er bedre end dets effekt IBS med fremherskende diarré, dette kunne forklares ved at øge tarmtransitten med serotonin, hvilket kan øge diarrésymptomerne ved IBS . Desuden viste denne undersøgelse en signifikant reduktion af angst og depressive symptomer i sertralin-gruppen sammenlignet med placebogruppen, hvilket blev vurderet ved henholdsvis Hamilton Rating scale for anxiety (HAM-A) og Hamilton Rating scale for depression (HAM-D).
Sertralin kunne være effektivt i behandlingen af IBS på grund af den høje forekomst af komorbiditet af IBS og psykiatriske lidelser, da dets oprindelse kan involvere fysiologiske såvel som psykologiske processer. Stress er normalt forbundet med symptomdebut og sværhedsgrad hos IBS-patienter, da mave-tarmkanalen er et følsomt mål for stress. Desuden påvirkes behandlingsresultater, hospitalsbesøg og sygdomserfaring negativt af stress, angst og depressive lidelser samt maladaptive copingmekanismer.
Sanselige forstyrrelser, især visceral hypersensitivitet (VHS) – som er en klinisk markør for IBS – er også blevet betragtet som patofysiologi for IBS . VHS er repræsenteret ved den øgede smertefornemmelse, når bækkenet colon er distenderet med en oppustet rektal ballon . Hazlett-Stevens et al. som fandt, at angst, der er specifik for viscerale fornemmelser, var en stærk prædiktor for IBS . Personer med angst var tilbøjelige til at katastrofe deres bekymringer konsekvenser og på den anden side, den hypokondriske tendens hos mennesker med angst . Disse fysiske symptomer på IBS kan forstærke deres angst og manglende evne til at tolerere og håndtere disse ubehageligheder og derved danne en ond cirkel mellem disse fysiske og psykologiske symptomer .
Så sertralin kan tilskrives dets antidepressive og anxiolytiske virkninger. Desuden ændrer sertralin den spinale modulation af nociceptive stimuli, samt påvirker amygdalaaktiviteten og Brain-Gut Axis-processen ved de hæmmende nedadgående smertemodulationssystemer .
Slutning
Sertralin er effektivt til behandling af irritabel tarm, især på dem, der har comorbid depression og/eller angst. Det anbefales at anvendes til nyligt diagnosticerede patienter og til patienter med fremherskende forstoppelse IBS. Yderligere forsøg er nødvendige for at diskutere sertralinets rolle i IBS med udelukkelse af depression og angst. Det er også nødvendigt at overveje længere varighed og større stikprøvestørrelse i yderligere forsøg for at påvise fuldstændig lindring af symptomer og tilbagefald af symptomer, hvis det sker.
Interessekonflikt
Ingen interessekonflikt kunne anmeldes.
- Lovell RM, Ford AC (2012) Global prevalence of and risk factors for irritable bowel syndrome: a meta-analysis. Clin Gastroenterol Hepatol 10: 712-721.
- Lovell RM, Ford AC (2012) Prævalens af gastroøsofageale refluks-type symptomer hos personer med irritabel tyktarm i samfundet: En meta-analyse. Am J Gastroenterol 107: 1793.
- Drossman DA (1993) US householder survey of functional gastrointestinal disorders. Dig Dis Sci 38: 1569-1580.
- Everhart JE, Ruhl CE (2009) Burden of digestive diseases in the United States part I: overall and upper gastrointestinal diseases. Gastroenterology 136: 376-386.
- Inadomi J, Fennerty MB, Bjorkman D (2003) The economic impact of irritable bowel syndrome. Aliment Pharmacol Ther 18: 671-682.
- Tillisch K, Mayer EA, Labus JS (2011) Kvantitativ metaanalyse identificerer hjerneområder, der aktiveres under rektal distension ved irritabel tyktarm. Gastroenterology 140: 91-100.
- Moriarty KJ, Dawson AM (1982) Functional abdominal pain: further evidence that whole gut is affected. Br Med J (Clin Res Ed) 284: 1670-1672.
- Trimble K (1995) Heightened visceral sensation in functional gastrointestinal disease is not site-specific. Dig Dis Sci 40: 1607-1613.
- Osterberg E (2000) A population study on irritable bowel syndrome and mental health. Scand J Gastroenterol 35: 264-268.
- Whitehead WE, Palsson O, Jones KR (2002) Systematic review of the comorbidity of irritable bowel syndrome with other disorders: what are the causes and implications? Gastroenterology 122: 140-1156.
- McQuay H (1996) A systematic review of antidepressants in neuropathic pain. Pain 68: 217-227.
- Saarto T, Wiffen PJ (2007) Antidepressiva til neuropatiske smerter. Cochrane Database Syst Rev CD005454.
- Mayer EA, Bradesi S (2003) Alosetron and irritable bowel syndrome (Alosetron og irritabel tarm). Expert Opin Pharmacother 4: 2089-2098.
- Deechakawan W (2014) Anxiety, depression and catecholamine levels after self-management intervention in irritable bowel syndrome. Gastroenterol Nurs 37: 24-32.
- Pinto C (2000) Stressende livsbegivenheder, angst, depression og coping hos patienter med irritabel tyktarm. J Assoc Physicians India 48: 589-93.
- Iii GRL (2004) Psychosocial factors are linked to functional gastrointestinal disorders: En befolkningsbaseret nested case-control undersøgelse. Am J Gastroenterol 99: 350.
- McLeod AL (2015) Effekter af angstdæmpende lægemidler og andre antropogene forurenende stoffer på fathead minnow adfærd og hjernekemi. Afhandling indsendt til Graduate School of Clemson University, USA.
- Tabas G (2004) Paroxetine to treat irritable bowel syndrome not responding to high-fiber diet: a double-blind, placebo-controlled trial. Am J Gastroenterol 99: 914.
- Vahedi H (2005) Effekten af fluoxetin hos patienter med smerte- og forstoppelsesprædominant irritabel tyktarm: En dobbeltblind randomiseret randomiseret undersøgelse. Aliment Pharmacol Ther 22: 381-385.
- Tack J (2006) A controlled crossover study of the selective serotonin reuptake inhibitor citalopram in irritable bowel syndrome. Gut 55: 095-1103.
- Ladabaum U (2010) Citalopram er ikke effektiv terapi til ikke-deprimerede patienter med irritabel tarm. Clin Gastroenterol Hepatol 81: 42.
- Kuiken SD, Tytgat GN, Boeckxstaens GE (2003) The selective serotonin reuptake inhibitor fluoxetine does not change rectal sensitivity and symptoms in patients with irritable bowel syndrome: a double blind, randomized, placebo-controlled study. Clin Gastroenterol Hepatol 1: 219-228.
- Talley NJ (2008) Antidepressiv behandling (imipramin og citalopram) for irritabel tarmsyndrom: et dobbeltblindet, randomiseret, placebokontrolleret forsøg. Dig Dis Sci 53: 108-115.
- Ford AC (2009) Efficacy of antidepressants and psychological therapies in irritable bowel syndrome: systematic review and meta-analysis. Gut 58: 367-378.
- Longstreth GF (2006) Functional bowel disorders. Gastroenterology 130: 1480-1491.
- Drossman DA (2000) What determines severity among patients with painful functional bowel disorders & quest. The Am J Gastroenterol 95: 974-980.
- Wilder-Smith C (2004) Brain functional magnetic resonance imaging of rectal pain and activation of endogenous inhibitory mechanisms in irritable bowel syndrome patient subgroups and healthy controls. Gut 53: 1595-1601.
- Hazlett-Stevens H (2003) Prævalens af irritabel tarmsyndrom blandt universitetsstuderende: rollerne af bekymring, neuroticisme, angstfølsomhed og visceral angst. J Psychosom Res 55: 501-505.
- Keefer L (2005) Towards a better understanding of anxiety in irritable bowel syndrome: a preliminary look at worry and intolerance of uncertainty. J Cogn Psychother 19: 163-172.