Keywords
Irritable bowel syndrome; Sertraline; Psychosomatic
Introduction
Az egyik leggyakoribb funkcionális gasztrointesztinális zavar az irritábilis bél szindróma (IBS), mivel világszerte 5-20%-os a prevalenciája, a Róma III kritériumoktól függően . Gyakoribb a fiatalabb egyéneknél, különösen a nőknél . Az IBS-ben szenvedő betegek hajlamosabbak a betegséggel összefüggő hiányzásokra, mint azok, akiknek nincsenek bélrendszeri tüneteik . A közelmúltban az Egyesült Államokban az IBS terhét becsülték meg, és megállapították, hogy a közvetlen költség közel 1 milliárd dollár, a közvetett költség pedig további 50 millió dollár . Ezenkívül az IBS-ben szenvedő betegek egészségügyi erőforrás-felhasználása körülbelül >50% . Ezért az IBS hatékony kezelése kulcsfontosságú akár az egyének, akár az egészségügyi ellátórendszerek és az egész társadalom számára.
Az IBS pontos oka továbbra sem ismert, ami azt jelenti, hogy nincs egyetlen egységes magyarázat a bélrendszeri tünetekre, amelyre a terápia irányulhatna. Az IBS-ben szenvedő betegek abnormális központi fájdalomfeldolgozást , zsigeri túlérzékenységet és magasabb szintű pszichológiai komorbiditást mutatnak a bélrendszeri tünetek nélküli egészséges kontrollokhoz képest. Ennek eredményeképpen az antidepresszánsokat bevezették az IBS kezelésére, mivel fájdalommódosító tulajdonságokkal rendelkeznek. A szerotonin (5-HT) az 5-HT3 és 5-HT4 receptorokon keresztül létfontosságú szerepet játszik a gasztrointesztinális motilitás, szekréció és érzékelés szabályozásában. Továbbá, a legújabb megfigyelések szerint a plazma 5-HT-koncentrációja csökken az IBS-betegeknél .
Más vizsgálatok kimutatták, hogy az IBS-betegek abnormális személyiséggel, valamint magasabb szorongási és depressziós értékekkel rendelkeznek . Azonban számos tanulmány értékelte az antidepresszánsok hatékonyságát az IBS-re; klinikai bizonyítékaik még mindig ellentmondásosak. A leggyakrabban alkalmazott antidepresszánsok a szelektív szerotonin visszavétel gátlók (SSRI), mint a fluoxetin és a citalopram, valamint a triciklikus antidepresszánsok (TCA), mint az imipramin és az amitriptilin.
A szelektív szerotonin visszavétel gátlóként a szertralin a szerotonin visszavételének blokkolásával hat a CNS szinaptikus hasadékaiban, így növeli a szerotoninszintet az agyban, ami pszichiátriai hatásaival jár. A szertralint 1991-ben engedélyezték az Egyesült Államokban, és ma is széles körben alkalmazzák, évente közel 40 millió receptet váltanak ki rá. Jól ismert a depresszió és a szorongásos zavarok kezelésére. Emellett a szelektív szerotonin visszavétel gátlók egyikének tekinthető, amely fájdalomszabályozó mechanizmussal rendelkezik, ezért gyakran alkalmazzák pszichoszomatikus zavarokban is .
Ez a vizsgálat összehasonlította a szertralin hatékonyságát a placebohatással (hagyományos terápia, mint görcsoldó és hasmenés elleni gyógyszerek) az irritábilis bél szindróma bélrendszeri tüneteire, valamint a szorongásos és depressziós tünetekkel kapcsolatos hatásukat illetően.
Módszerek
A jelen vizsgálat egy prospektív, szertralin, placebo randomizált klinikai vizsgálat volt, 1 hónapos időtartamú, egyszeri vak kezeléssel és vak eredményméréssel. A vizsgálat 55 olyan betegből állt, akiknél a Róma III. kritériumoknak megfelelően nemrégiben irritábilis bél szindrómát (IBS) diagnosztizáltak, és akiket 4 héten belül toboroztak az Assiut Egyetemi Kórházak ambulanciáiról.
Mintaméret
Az IBS-sel kapcsolatos esetkontroll vizsgálatokban gyakran megfigyelhető 50%-os válasz a placebóra. Továbbá nyílt vizsgálatokban akár 89%-os antidepresszáns válaszadási arányt is megfigyeltek. Ezeket a számokat felhasználva és 80%-os teljesítmény mellett minden csoportra vonatkozóan 80%-os mintaméretet kaptunk.
Alanyok és a vizsgálat felépítése
A korcsoport 18-40 év közötti volt. Csak olyan betegeket vontunk be, akiknél nemrégiben diagnosztizálták az IBS-t, és a betegség időtartama nem haladta meg az 5 évet. Ezenkívül valamennyi beteget korábban nem kezeltek más szelektív szerotonin visszavétel gátlóval. Minden betegnél elvégeztünk minden rutinvizsgálatot, beleértve a teljes vérképet, a vese- és májfunkciókat, valamint az elektrolitok mérését. A kezelés megkezdése előtt minden betegnél elvégeztük a szorongás Hamilton-értékelő skáláját (HAM-A) és a depresszió Hamilton-értékelő skáláját (HAM-D). A betegeket két csoportra osztották, az első csoportba 30 beteg tartozott, akik 50 mg sertralint kaptak, a második csoportba pedig 25 beteg, akik placebót kaptak. A randomizált klinikai vizsgálat során a vakítást elrejtették. A betegeket a kezelés után egy hónapig követték nyomon. A betegek újraértékelése a bélrendszeri megnyilvánulásaik tekintetében történt. A bélműködés javulását akkor tekintették javulásnak, ha a betegek 4 hetes gyógyszeres kezelés után a tünetek megfelelő enyhüléséről számoltak be. A kezelés után egy hónappal minden betegnél elvégezték a Hamilton-féle szorongásértékelő skálát (HAM-A) és a Hamilton-féle depresszióértékelő skálát (HAM-D) is.
Kizárási kritériumok
1. Olyan betegek, akiknek béltünetei voltak, de nem feleltek meg az irritábilis bél szindróma diagnózisának Róma III. kritériumainak.
2. Olyan betegek, akiknek irritábilis bél szindrómája több mint 5 éve fennállt.
3. Olyan betegek, akiknek a HAM-A, illetve a HAM-D szerint súlyos szorongásuk és/vagy depressziójuk volt.
4. Olyan betegek, akik nem feleltek meg a korcsoportnak.
5. Olyan betegek, akik nem feleltek meg a korcsoportnak. Azok a betegek, akik bármilyen más gyógyszert kaptak.
6. Azok a betegek, akiknek bármilyen krónikus egészségügyi problémájuk volt.
Adatok elemzése
A vizsgálatban az SPSS 16-os verziójú csomagot használták. Leíró statisztikákat használtunk a sertralin és a placebo bélmegnyilvánulásokra gyakorolt hatásának összehasonlítására. Páros mintás T-próbát használtunk a szertralin és a placebo hatásának összehasonlítására a Hamilton rating scale for anxiety (HAM-A), illetve a Hamilton rating scale for depression (HAM-D) értékelési skálán.
Eredmények
A vizsgálatban 55 irritábilis bél szindrómás beteg vett részt, akiket a Róma III. kritériumoknak megfelelően diagnosztizáltak. Ami a betegek demográfiai adatait illeti, a betegek átlagéletkora 26 ± 2,1 év volt, a nők és férfiak aránya 1,7/1 volt, mivel 32 női beteg állt szemben 18 férfi beteggel.
A leggyakoribb GIT-manifesztáció a hasi diszkomfortérzés volt, amelyet minden betegnél (100%) találtak, ezt követte a hasi puffadás és puffadás, amelyet 36 betegnél (65,45%) találtak. A harmadik leggyakoribb megnyilvánulás a tünetek javulása székletürítéssel, ami 32 betegnél (58,18%) fordult elő, végül a legkevésbé gyakori tünet a váltakozó székelési szokások, ami 29 betegnél (52,7%) fordult elő. Az IBS-C-ben szenvedő betegeknél gyakrabban fordult elő hasi puffadás és a tünetek javulása székeléssel, míg az IBS-D-ben szenvedő betegeknél gyakrabban fordult elő váltakozó székelési szokások (1. ábra).
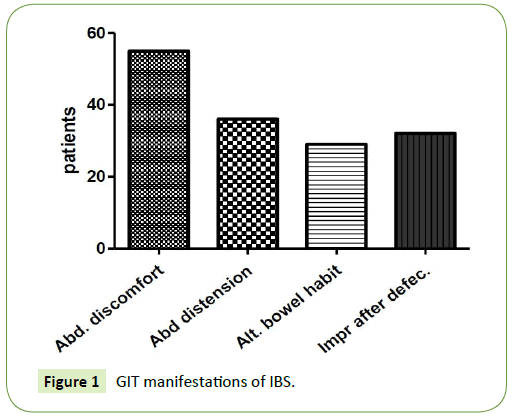
1. ábra: Az IBS GIT-megnyilvánulásai.
A betegeket két csoportra osztottuk. A 30 beteg 50 mg szertralint, 25 beteg pedig placebót kapott. Az 50 mg szertralint kapó 20 betegnél javultak a bélrendszeri tünetek (7 betegnél volt túlnyomórészt hasmenéssel járó irritábilis bél szindróma, 13 betegnél pedig túlnyomórészt székrekedéssel járó irritábilis bél szindróma), míg 10 betegnél (4 betegnél volt túlnyomórészt hasmenéssel járó irritábilis bél szindróma, 6 betegnél pedig túlnyomórészt székrekedéssel járó irritábilis bél szindróma) nem mutatkozott kielégítő javulás a bélrendszeri tünetekben.
Másrészt, 8 betegnél, akik placebót kaptak, a bélrendszeri tünetek javulását tapasztalták (5 betegnél az irritábilis bél szindróma dominált hasmenéssel és 3 betegnél az irritábilis bél szindróma dominált székrekedéssel), míg 17 betegnél (12 betegnél az irritábilis bél szindróma dominált hasmenéssel és 5 betegnél az irritábilis bél szindróma dominált székrekedéssel) a bélrendszeri tünetek nem javultak (1. táblázat és 2. ábra).
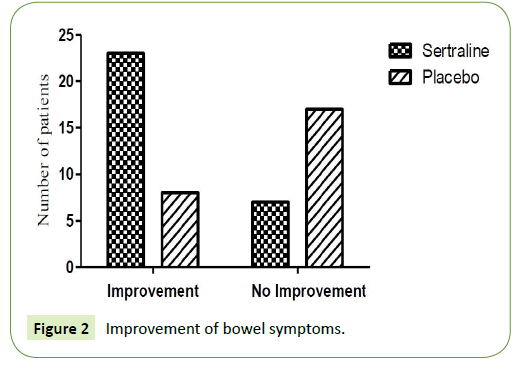
2. ábra: A bélrendszeri tünetek javulása.
Jegyzet: IBS-D: irritábilis bélszindróma túlsúlyos hasmenéssel, IBS-C: irritábilis bélszindróma túlsúlyos székrekedéssel
1. táblázat: A betegek száma a bélrendszeri tünetek javulását mutatta egy hónapos gyógyszeres kezelés után.
A két vizsgálati csoportot a szorongás, illetve a depresszió Hamilton-értékelő skála tekintetében hasonlították össze. Egy hónap elteltével szignifikáns csökkenés mutatkozott a Hamilton rating scale for anxiety (HAM-A) és a Hamilton rating scale for depression (HAM-D) értékelési skálán a sertralin 50 mg-mal kezelt betegcsoportban. A HAM-A átlaga 18,8 ± 3,9 volt a kezelés előtt, és 11,67 ± 1,9 volt a sertralin egy hónapos kezelés után. Továbbá, a HAM-D átlaga 15,67 ± 3,9 volt a kezelés előtt, és 11,6 ± 4,2 értéket ért el a sertralinnal történő egy hónapos kezelés után (P=0,001). Míg a placebóval kezelt betegcsoportban egy hónap után nem volt szignifikáns csökkenés a Hamilton rating scale for anxiety (HAM-A) és a Hamilton rating scale for depression (HAM-D) értékében. A HAM-A átlaga a kezelés előtt 18,5 ± 2,6 volt, és a placebóval történő egy hónapos kezelés után elérte a 18,2 ± 2,4 értéket (P=0,12) (2. táblázat). Ezenkívül a HAM-D átlaga 13,4 ± 2,1 volt a kezelés előtt, és 13 ± 1,7-et ért el az egy hónapos placebóval történő kezelés után (P=0,15) (3. és 4. ábra).
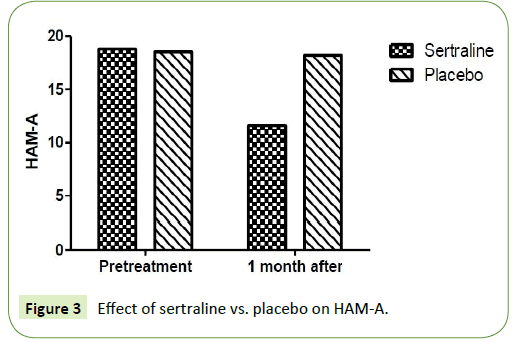
3. ábra: A szertralin vs. placebo hatása a HAM-A-ra.
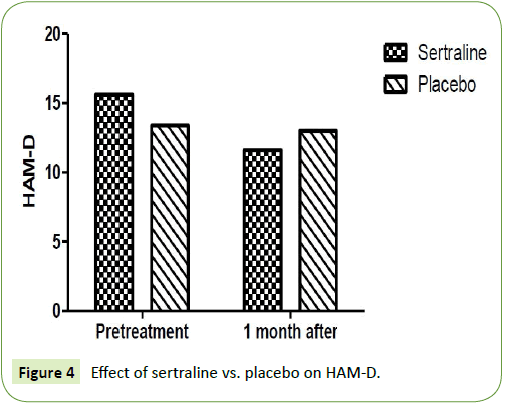
4. ábra: A szertralin hatása a HAM-A-ra. Placebo a HAM-D-re.
Táblázat: A sertralin Vs placebo hatása a HAM-A-ra és a HAM-D-re.
Diszkusszió
A szakirodalomban hat tanulmány tárgyalta a szelektív szerotonin visszavétel gátlók (SSRI) hatását az IBS kezelésében, ellentmondásos eredményekkel. Négy vizsgálat a paroxetinnel , fluoxetinnel és citaloprammal kapcsolatban szerény előnyről számolt be, míg két vizsgálat a fluoxetinnel és citaloprammal kapcsolatban nem.
Ezek a vizsgálatok metaanalízise szerint az irritábilis bél szindróma (IBS) tüneteinek nem javuló relatív kockázata 0,62 (95% CI, 0,45-0,87) az SSRI-k esetében a placebóval szemben, a vizsgálatok közötti jelentős heterogenitással . A metaanalízis 113 SSRI-vel kezelt és 117 kontrollszemély adatait elemezte.
A hat vizsgálat eredményeinek eltérései a vizsgálati terv, valamint a betegek populációjának különbségeire vezethetők vissza. Kuiken és munkatársai 40, minden altípusba tartozó IBS-beteget toboroztak egy tercier központból egy 6 hetes fluoxetin vagy placebo vizsgálathoz, a depressziós betegeket kizárták ebből a vizsgálatból . Tabas és munkatársai 81, minden altípusú IBS-ben szenvedő beteget randomizáltak egy 12 hetes, magas rosttartalmú diétával és paroxetinnel vagy placebóval végzett vizsgálatra, a depressziós betegeket nem zárták ki ebből a vizsgálatból . Vahedi és munkatársai 44, túlnyomórészt székrekedésben szenvedő IBS-es beteget randomizáltak fluoxetinnel vagy placebóval egy 12 hetes vizsgálatra, de csak a súlyos depresszióban szenvedő betegeket zárták ki . Tack és munkatársai 23 IBS-beteget vontak be egy tercier ellátó központból egy crossover vizsgálatba, amelyben a citalopramot és a placebót hasonlították össze, a depressziós betegeket kizárták ebből a vizsgálatból .
Ladabaum és munkatársai 27 IBS-beteget randomizáltak, akik 4 hétig 20 mg/nap citalopramot kaptak, majd további 4 hétig 40 mg/nap citalopramot, de a pszichiátriai tüneteket nem értékelték ezeknél a betegeknél .
Talley és munkatársai . 51, bármilyen típusú IBS-ben szenvedő beteget randomizáltak citalopramra (17 alany), imipraminra vagy placebóra (16 alany) 12 héten keresztül, ebből a vizsgálatból is kizárták a depressziós betegeket .
Azoknak a vizsgálatoknak a jellemzői, amelyekben némi előnyt észleltek, többek között a depresszió kizárásának hiánya , a kizárólag székrekedés domináns IBS-betegek bevonása , és a keresztirányú tervezés a tercier ellátásból származó betegekkel .
Az egyes vizsgálatokban alkalmazott konkrét gyógyszer, dózis és időtartam fontos tényezők lehetnek, de nem rajzolódik ki egyértelmű minta. A Tack és munkatársai által végzett vizsgálat az egyetlen, amely a citalopram előnyét mutatta ki , míg a Talley és munkatársai által végzett vizsgálat a citalopram és a placebo azonos válaszadási arányáról számolt be , Ladabaum és munkatársai pedig bizonyítékot találtak a citalopram jelentős előnye ellen az IBS bélrendszeri tüneteinek kezelésében . A vizsgálatok különböző definíciókat használtak a klinikai válaszra, és ez magyarázhatja a következtetések közötti ellentmondás nagy részét.
Egy részük az IBS tüneteinek megfelelő enyhülését használta elsődleges kimenetként, mint Talley és munkatársai. Ezzel szemben a többi vizsgálat a globális tüneti választ, az általános jóllétet vagy a specifikus tünetekre gyakorolt hatást értékelte.
A mi vizsgálatunk az első olyan vizsgálat, amely a szertralin IBS kezelésében kifejtett hatását tárgyalta. Azt találtuk, hogy a szertralin a placebóhoz képest szignifikáns hatással van az irritábilis bél szindróma (IBS) bélrendszeri tüneteire. A szertralin javulása 66,67%-os volt a placebóhoz képest, amely 32%-os volt. Vizsgálatunk kimutatta, hogy a sertralin hatása a túlnyomórészt székrekedéssel járó IBS-re jobb, mint a túlnyomórészt hasmenéssel járó IBS-re, ez azzal magyarázható, hogy a szerotonin növeli a bélmozgást, ami fokozhatja az IBS hasmenéses tüneteit. Ezenkívül ez a vizsgálat a szorongásos és depressziós tünetek szignifikáns csökkenését mutatta ki a sertralin csoportban a placebocsoporthoz képest, amit a Hamilton Rating scale for anxiety (HAM-A) és a Hamilton Rating scale for depression (HAM-D) értékelt.
A sertralin hatékony lehet az IBS kezelésében, mivel az IBS és a pszichiátriai rendellenességek komorbiditása igen gyakori, mivel a betegség eredete fiziológiai és pszichológiai folyamatokat is magában foglalhat. A stressz általában összefüggésbe hozható az IBS-betegek tüneteinek megjelenésével és súlyosságával, mivel a GI-traktus érzékeny célpont a stresszre. Továbbá a kezelés eredményét, a kórházi látogatásokat, valamint a betegségélményt kedvezőtlenül befolyásolja a stressz, a szorongás és a depressziós zavarok, valamint a maladaptív megküzdési mechanizmusok .
A szenzoros zavarokat, különösen a zsigeri túlérzékenységet (VHS) – amely az IBS klinikai markere – szintén az IBS patofiziológiájának tekintik. A VHS-t a kismedencei vastagbél felfújt rektális ballonnal történő kitágításakor fellépő fokozott fájdalomérzet jelenti . Hazlett-Stevens et al. akik megállapították, hogy a zsigeri érzésekre jellemző szorongás az IBS erős előrejelzője . A szorongó egyének hajlamosak voltak arra, hogy katasztrofizálják aggodalmaik következményeit, és másrészt a szorongó emberek hipochondriás hajlama . Ezek a fizikai tünetek az IBS megerősíthetik a szorongásukat és képtelenek elviselni és megbirkózni ezekkel a kellemetlenségekkel, ezáltal ördögi kört alkotva e fizikai és pszichológiai tünetek között .
A szertralin hatása tehát antidepresszáns és anxiolitikus hatásainak tulajdonítható. Továbbá a szertralin megváltoztatja a nociceptív ingerek gerincvelői modulációját, valamint befolyásolja az amygdala aktivitását és az agy-bél tengely folyamatát a gátló leszálló fájdalommodulációs rendszereken keresztül .
Következtetés
A szertralin hatékony az irritábilis bél szindróma kezelésében, különösen azoknál, akiknek komorbid depressziója és/vagy szorongása van. Alkalmazása javasolt a nemrégiben diagnosztizált betegeknél és a túlsúlyos székrekedéses IBS-ben szenvedőknél. További vizsgálatokra van szükség a szertralin szerepének megvitatásához az IBS-ben a depresszió és a szorongás kizárásával. Továbbá hosszabb időtartamot és nagyobb mintanagyságot kell figyelembe venni a további vizsgálatokban a tünetek teljes enyhülésének és a tünetek esetleges visszaesésének kimutatásához.
Conflict of Interest
No conflict of interest could be declared.
- Lovell RM, Ford AC (2012) Global prevalence of and risk factors for irritable bowel syndrome: a meta-analysis. Clin Gastroenterol Hepatol 10: 712-721.
- Lovell RM, Ford AC (2012) A gastrooesophagealis reflux típusú tünetek prevalenciája irritábilis bél szindrómában szenvedő egyéneknél a közösségben: A meta-analysis. Am J Gastroenterol 107: 1793.
- Drossman DA (1993) US householder survey of functional gastrointestinal disorders. Dig Dis Sci 38: 1569-1580.
- Everhart JE, Ruhl CE (2009) Burden of digestive diseases in the United States part I: overall and upper gastrointestinal diseases. Gastroenterology 136: 376-386.
- Inadomi J, Fennerty MB, Bjorkman D (2003) The economic impact of irritable bowel syndrome. Aliment Pharmacol Ther 18: 671-682.
- Tillisch K, Mayer EA, Labus JS (2011) Quantitative meta-analysis identifies brain regions activated during rectal distension in irritable bowel syndrome. Gastroenterology 140: 91-100.
- Moriarty KJ, Dawson AM (1982) Funkcionális hasi fájdalom: további bizonyíték arra, hogy az egész bélrendszer érintett. Br Med J (Clin Res Ed) 284: 1670-1672.
- Trimble K (1995) Heased visceral sensation in functional gastrointestinal disease is not site-specific. Dig Dis Sci 40: 1607-1613.
- Osterberg E (2000) A population study on irritable bowel syndrome and mental health. Scand J Gastroenterol 35: 264-268.
- Whitehead WE, Palsson O, Jones KR (2002) Systematic review of the comorbidity of irritable bowel syndrome with other disorders: what are the causes and implications? Gastroenterology 122: 140-1156.
- McQuay H (1996) A systematic review of antidepressants in neuropathic pain. Pain 68: 217-227.
- Saarto T, Wiffen PJ (2007) Antidepressants for neuropathic pain. Cochrane Database Syst Rev CD005454.
- Mayer EA, Bradesi S (2003) Alosetron and irritable bowel syndrome. Expert Opin Pharmacother 4: 2089-2098.
- Deechakawan W (2014) Anxiety, depression, and catecholamine levels after self-management intervention in irritable bowel syndrome. Gastroenterol Nurs 37: 24-32.
- Pinto C (2000) Stresszes életesemények, szorongás, depresszió és megküzdés irritábilis bél szindrómás betegeknél. J Assoc Physicians India 48: 589-93.
- Iii GRL (2004) Psychosocial factors are linked to functional gastrointestinal disorders: A population based nested case-control study. Am J Gastroenterol 99: 350.
- McLeod AL (2015) A szorongásoldó gyógyszerek és más antropogén szennyezőanyagok hatása a kövérfejű pinty viselkedésére és agyi kémiájára. Thesis submitted to the Graduate School of Clemson University, USA.
- Tabas G (2004) Paroxetine to treat irritable bowel syndrome not responding to high-fiber diet: a double-blind, placebo-kontrollált trial. Am J Gastroenterol 99: 914.
- Vahedi H (2005) A fluoxetin hatása fájdalomban és székrekedésben szenvedő, irritábilis bél szindrómában szenvedő betegeknél: Egy kettős vak, randomizált és kontrollált vizsgálat. Aliment Pharmacol Ther 22: 381-385.
- Tack J (2006) A controlled crossover study of the selective serotonin reuptake inhibitor citalopram in irritable bowel syndrome. Gut 55: 095-1103.
- Ladabaum U (2010) A citalopram nem hatékony terápia nem depressziós betegeknél irritábilis bél szindrómában. Clin Gastroenterol Hepatol 81: 42.
- Kuiken SD, Tytgat GN, Boeckxstaens GE (2003) The selective serotonin reuptake inhibitor fluoxetine does not change rectal sensitivity and symptoms in patients with irritable bowel syndrome: a double blind, randomized, placebo-controlled study. Clin Gastroenterol Hepatol 1: 219-228.
- Talley NJ (2008) Antidepresszáns terápia (imipramin és citalopram) irritábilis bél szindrómában: kettős vak, randomizált, placebokontrollos vizsgálat. Dig Dis Sci 53: 108-115.
- Ford AC (2009) Az antidepresszánsok és pszichológiai terápiák hatékonysága irritábilis bél szindrómában: szisztematikus áttekintés és metaanalízis. Gut 58: 367-378.
- Longstreth GF (2006) Functional bowel disorders. Gastroenterology 130: 1480-1491.
- Drossman DA (2000) What determines severity among patients with painful functional bowel disorders & quest. The Am J Gastroenterol 95: 974-980.
- Wilder-Smith C (2004) A rektális fájdalom agyi funkcionális mágneses rezonancia képalkotása és az endogén gátló mechanizmusok aktiválása irritábilis bél szindrómás betegek alcsoportjaiban és egészséges kontrollcsoportokban. Gut 53: 1595-1601.
- Hazlett-Stevens H (2003) Az irritábilis bél szindróma prevalenciája egyetemi hallgatók körében: az aggodalom, a neuroticizmus, a szorongásos érzékenység és a zsigeri szorongás szerepe. J Psychosom Res 55: 501-505.
- Keefer L (2005) Towards a better understanding of anxiety in irritable bowel syndrome: a preliminary look at worry and intolerance of uncertainty. J Cogn Psychother 19: 163-172.